Una olla de presión molecular ablanda los trozos duros de proteína y ayuda a morder
Las proteínas están compuestas por aminoácidos conectados por enlaces amídicos. El enlace amídico exhibe una alta estabilidad química y tiene una estructura plana alrededor del enlace. Aunque la alta estabilidad del enlace de amida es indispensable para mantener las funciones de las proteínas, es problemático convertir el bloque de construcción en algunas otras especies moleculares mediante la disociación selectiva de un enlace de amida relevante. Se ha intentado controlar la reactividad de un enlace de amida específico con la torsión selectiva del enlace mediante complicadas modificaciones químicas. Algunos compuestos modelo con enlaces amídicos retorcidos han sido producidos por síntesis orgánica de múltiples pasos y se ha demostrado su alta reactividad. Se presume que la alta reactividad de estos enlaces de amida retorcida también se utiliza in vivo. Algunas proteínas parecen ser cortadas selectivamente al retorcerse los enlaces de amida específicos durante la autolisis y el empalme. Estas proteínas, a diferencia de los compuestos modelo sintetizados artificialmente, se supone que utilizan interacciones no covalentes para retorcer sus enlaces amídicos. Los investigadores de la Universidad de Tokio y del Instituto de Ciencias Moleculares han fabricado durante muchos años sus jaulas moleculares, que se autoensamblan por las interacciones no covalentes. Aplicaron sus jaulas moleculares para confinar las moléculas de amida, que pueden considerarse análogas a pequeños trozos de proteínas, y exprimieron los enlaces de amida presurizándolos dentro de su jaula.
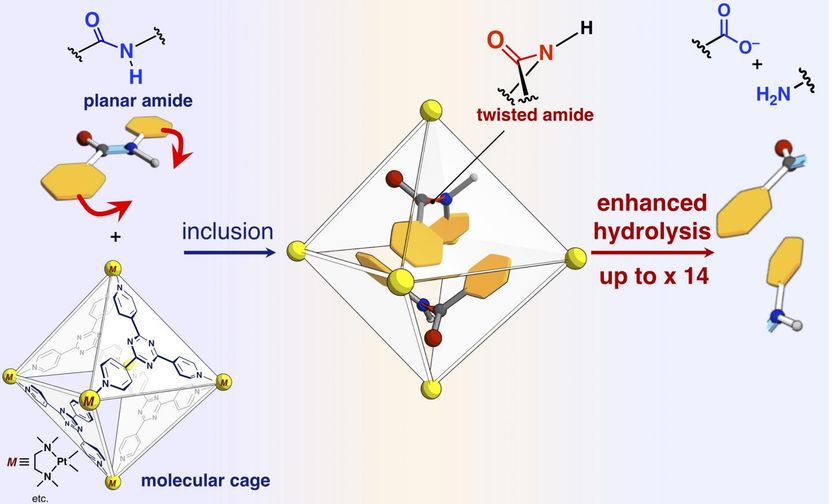
Se trata de un esquema de aceleración de la velocidad de reacción de la hidrólisis de la amida mediante su inclusión en la jaula molecular autoensamblada.
NINS/IMS
Los investigadores han informado en el presente documento que los enlaces de amida, que tienen estructuras planas y son inertes en el espacio libre, pueden retorcerse y los compuestos de amida pueden activarse confinándolos en su jaula molecular. Cuando los compuestos de amida objetivo y la jaula molecular se mezclan y calientan en una solución acuosa, la jaula confina los compuestos de amida. El análisis de la estructura de rayos X de un solo cristal reveló que dos compuestos de amida con estructuras retorcidas están confinados en la jaula. Se encontró que el ángulo de torsión alrededor de los enlaces de amida alcanzaba los 34 grados. La velocidad de reacción de hidrólisis del blanco retorcido se aceleró en un factor de cinco. Los investigadores lograron crear una nueva enzima artificial de mecanismo no explotado que confina y retuerce las moléculas del objetivo para activar un enlace químico específico.
Los investigadores también lograron alterar la reactividad de las moléculas objetivo confinando las "moléculas de relleno", que no participan en la reacción, junto con los objetivos en la jaula, controlando así con precisión el grado de torsión de los enlaces de la amida. Sin la molécula de relleno, las dos de las amidas objetivo están confinadas en una jaula. Uno de los dos objetivos se tuerce y el otro permanece plano. Por el contrario, cuando el material cónico se mezcla y luego se envuelve junto con el objetivo en una jaula, el objetivo permanece plano. Cuando una molécula de relleno plana se involucra con el objetivo, la materia cambia la forma del objetivo en una estructura retorcida. Los investigadores investigaron las tasas de reacción de la hidrólisis en los dos casos y encontraron que la materia plana (blanco retorcido) aceleraba la tasa en 14 veces, mientras que la materia cónica (blanco plano) aceleraba la tasa en tres veces. Las moléculas del relleno nos permiten ajustar la velocidad de reacción con precisión. Este es un logro sin precedentes que nunca se ha encontrado en investigaciones anteriores. Esta investigación nos da un método novedoso para la activación de las moléculas inertes y puede aplicarse a una variedad de reacciones orgánicas.
Los investigadores demostraron que las moléculas de amida pueden activarse retorciéndose dentro de la jaula sin engorrosos procesos de modificación química. "Estamos buscando un nuevo tipo de jaulas que puedan activar los objetivos con mayor eficiencia y aplicarlos a otras categorías de moléculas objetivo. Con nuestras nuevas jaulas, desarrollaremos el novedoso método de activación de moléculas inertes. En el futuro, nuestras jaulas se utilizarán como catalizadores, que exprimen y activan selectivamente un enlace específico de una molécula objetivo, y también como agentes de activación para los pro-drogas que trabajan en nuestro cuerpo", dijo Fujita.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.