Double attaque pathogène
Plus de 85 % des décès survenus au cours de la pandémie de grippe espagnole n'étaient pas dus au virus de la grippe, mais à une infection bactérienne secondaire.
Selon les estimations, environ 50 millions de personnes sont mortes de la grippe espagnole qui a éclaté en 1918. Cette pandémie a été déclenchée par une souche hautement infectieuse du virus de la grippe. Sur la base de données historiques et cliniques, nous savons aujourd'hui que dans une grande partie des cas, la cause du décès n'était pas la maladie virale elle-même, mais une pneumonie résultant d'une infection bactérienne. Ces infections secondaires ou surinfections se développent sur le foyer d'une infection virale antérieure et restent préoccupantes, même à l'ère des antibiotiques. Les scientifiques estiment qu'environ un quart des personnes décédées lors de la pandémie de grippe de 2009 (connue sous le nom de "grippe porcine") souffraient d'une co-infection bactérienne. Des chercheurs de l'Université des ressources naturelles et des sciences de la vie appliquées de Vienne (BOKU) viennent de démontrer qu'une vaccination antigrippale offre également une protection contre les infections bactériennes secondaires. Un groupe de recherche dirigé par Reingard Grabherr et le chercheur principal Miriam Klausberger se sont penchés sur la question dans le cadre d'un projet intitulé "A VLP approach to combat post-influenza bacterial infections" (Approche VLP pour lutter contre les infections bactériennes post-grippales). La recherche du groupe s'est appuyée sur un format de vaccin prometteur à la pointe de la technologie.
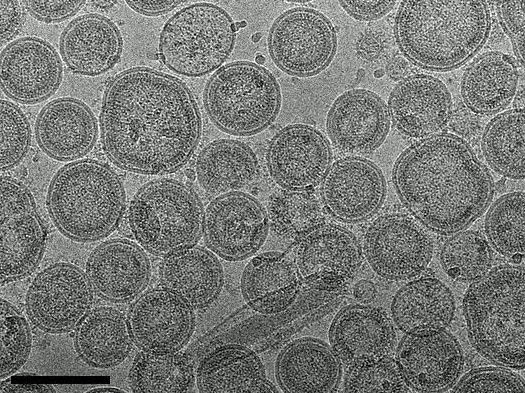
Les particules apparentées à des virus (VLP) peuvent être rendues visibles grâce à la microscopie électronique cryogénique. Sous-produits du cycle de réplication de nombreuses espèces de virus, ces enveloppes vides de virus présentent un grand potentiel pour le développement de vaccins. (Échelle : barre noire = 100 nm)
M. Klausberger
Les virus facilitent le démarrage
"Une infection grippale crée dans l'organisme des conditions qui permettent aux bactéries de s'implanter plus facilement", explique Miriam Klausberger. L'effet est particulièrement marqué dans les trois à sept jours qui suivent l'infection virale. Dans ce laps de temps, même une faible dose de bactéries peut déclencher une infection grave qui serait autrement inoffensive. L'affaiblissement du système immunitaire n'est cependant pas la seule explication. "Après une infection virale, la réponse immunitaire perd des éléments importants. De plus, pour combattre le virus, le système immunitaire active des composants qui sont contre-productifs face à une infection bactérienne", note Klausberger. Ces composants comprennent des substances messagères du système immunitaire, telles que l'interféron de type I (α/β) et de type II (γ). Ils offrent une protection contre les infections virales mais entravent le recrutement et le fonctionnement de certaines cellules immunitaires nécessaires pour combattre efficacement les infections bactériennes.
Les infections bactériennes secondaires sont connues non seulement pour la grippe mais aussi pour les rhinovirus, le virus respiratoire syncytial (VRS) ou le SRAS-CoV-2. "Lorsque les virus se multiplient dans les voies respiratoires, ils endommagent la surface de la couche cellulaire externe", explique Klausberger. "Cela permet aux bactéries d'adhérer plus facilement à la muqueuse et de s'y multiplier. Lors des pandémies de grippe mentionnées au début, ce sont surtout les agents pathogènes Staphylococcus aureus et Streptococcus pneumoniae qui ont profité de l'avantage viral. Ces deux bactéries colonisent fréquemment les voies respiratoires humaines dans des circonstances normales, sans provoquer de maladie. S. pneumoniae, par exemple, peut être détecté chez un enfant sur deux jusqu'à l'âge de deux ans. "Le fait de savoir que ces bactéries sont déjà présentes signifie qu'une infection grippale représente un risque potentiel encore plus grand", avertit Klausberger.
Quelle est l'efficacité de la protection vaccinale ?
L'idée qui sous-tend le projet de M. Klausberger est simple : "Nous savons qu'une infection grippale prépare le terrain pour des complications bactériennes. Il pourrait donc être bénéfique de prévenir l'infection virale par la vaccination". Afin d'explorer cette hypothèse, les chercheurs du BOKU ont coopéré avec l'Institut de recherche Mechnikov pour les vaccins et les sérums, basé à Moscou. Les chercheurs autrichiens ont produit un vaccin antigrippal basé sur des "particules semblables à des virus" (VLP). À l'institut russe, ces VLP ont été utilisées pour immuniser des souris dans le cadre de la série d'expériences prévue. "Les VLP sont un phénomène qui se produit naturellement dans de nombreux virus", explique Klausberger. "Il s'agit de particules défectueuses produites lors de la réplication du virus. Bien qu'elles ne se distinguent pas extérieurement de leurs homologues infectieux, elles ne peuvent pas se répliquer parce qu'elles ne possèdent pas le matériel génétique nécessaire. "Cela fait des VLP un format de vaccin relativement sûr et très efficace.
Les particules semblables à des virus (VLP) peuvent être rendues visibles au moyen de la microscopie électronique cryogénique. Sous-produits du cycle de réplication de nombreuses espèces de virus, ces enveloppes vides de virus présentent un grand potentiel pour le développement de vaccins. (Échelle : barre noire = 100 nm) Source : M. Klausberger
L'expérience a porté sur les animaux vaccinés et sur un groupe témoin de souris non vaccinées. Chez tous les animaux, la première étape a consisté en une infection primaire par un virus de la grippe. Cinq jours plus tard, les souris ont été infectées par S. aureus ou S. pneumoniae. Au cours de l'expérience, les chercheurs ont contrôlé le succès de la vaccination et l'évolution de la maladie en étudiant différents paramètres, tels que les titres d'anticorps détectables dans le sang, la propagation des virus et des bactéries dans le tissu pulmonaire et le nombre de décès.
Un taux de survie de 100
Après un total de 18 jours, seuls 10 % des animaux témoins non vaccinés avaient survécu à l'infection secondaire par S. aureus, alors que le taux de survie des animaux ayant reçu une vaccination adaptée à la souche grippale était de 100 %. Dans le cas de S. pneumoniae, aucun des animaux non vaccinés n'a survécu aux deux infections, alors que 60 à 70 % des animaux vaccinés ont survécu.
"Nos résultats confirment qu'une bonne immunité contre les virus de la grippe peut également réduire le risque de complications dues à des infections secondaires", conclut M. Klausberger. Les chercheurs ont également bénéficié d'une meilleure compréhension de la production et de la purification des vaccins à base de VLP. "Les VLP ont un grand potentiel pour le développement de vaccins car ils sont très efficaces même à de faibles doses. En collaboration avec d'autres groupes de BOKU, nous nous concentrons sur l'optimisation de la production de ces vaccins", a déclaré M. Klausberger. Il existe déjà des vaccins à base de VLP pour le papillomavirus humain (HPV) et le virus de l'hépatite B. Des préparations contre les virus de la grippe sont en cours d'élaboration. Des préparations contre les virus de la grippe font actuellement l'objet d'essais cliniques.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Klausberger M., Leneva I.A., Egorov A., Strobl F. et al.: "Off-target effects of an insect cell-expressed influenza HA-pseudotyped Gag-VLP preparation in limiting postinfluenza Staphylococcus aureus infections. "Vaccine 38(4), 2020.