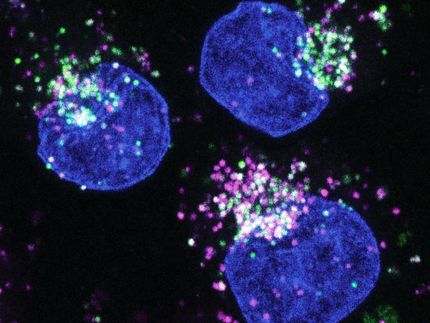
Fagocitos de la placa de cultivo para la terapia del cáncer
"Nuestros fagocitos inducidos tienen el potencial de destruir células cancerosas en aplicaciones terapéuticas devorándolas"
Hoy en día, las terapias celulares contra el cáncer suelen fracasar porque las células inmunitarias son incapaces de penetrar eficazmente en el tumor. El uso de determinados fagocitos se considera una alternativa prometedora, pero hasta ahora no era posible cultivarlos en cantidades suficientes en la placa de cultivo. Investigadores del Consorcio Alemán contra el Cáncer (DKTK) del Hospital LMU de Múnich han encontrado ahora una solución: Utilizar un factor de transcripción que puede activarse o desactivarse mediante un activador en el medio de cultivo de las células.
En el DKTK, el Centro Alemán de Investigación Oncológica (DKFZ) de Heidelberg, como centro central, une sus fuerzas a largo plazo con centros universitarios asociados con conocimientos oncológicos especiales.
Las terapias que utilizan las células inmunitarias del propio paciente, armadas contra el cáncer en la placa de cultivo, ya han demostrado ser muy eficaces en algunas leucemias y linfomas. Para ello, las células T del paciente se modifican genéticamente con moléculas receptoras que reconocen específicamente determinadas características de las células tumorales.
El problema, sin embargo, es que estas llamadas células T CAR son incapaces de penetrar eficazmente en los tumores sólidos, lo que significa que las terapias suelen ser ineficaces. La solución podría ser otro grupo de células inmunitarias: ciertos fagocitos, los llamados macrófagos, que forman parte del sistema inmunitario innato.
Los macrófagos tienen la capacidad intrínseca de penetrar en los tumores. Pueden eliminar patógenos o células enfermas engulléndolos, y también activan otras líneas de defensa del sistema inmunitario. También pueden estar dotados de proteínas receptoras dirigidas contra las características tumorales, pero: "Hasta ahora era imposible cultivar fagocitos en la cantidad necesaria en la placa de cultivo", explica Philipp Greif, jefe de un grupo de investigación del DKTK en el Hospital LMU de Múnich.
En cuanto las células madre sanguíneas, de las que finalmente surgen los fagocitos, se aíslan de su entorno natural en la médula ósea, comienzan a diferenciarse en células sanguíneas maduras. Sin embargo, el "rendimiento" de los fagocitos sigue siendo demasiado bajo para utilizarlos en aplicaciones médicas.
Un equipo dirigido por Philipp Greif y Christian Wichmann, del Hospital LMU, ha encontrado ahora una solución a este problema: los investigadores equiparon genéticamente células progenitoras de sangre humana con la proteína MLL-ENL. Esta abreviatura se refiere a la fusión de dos proteínas que juntas forman un factor de transcripción cancerígeno que promueve la división celular en muchas leucemias.
El truco de los investigadores del DKTK: dotaron a MLL-ENL de un dominio controlable mediante el cual puede activarse con una sustancia química. Los expertos lo denominan factor de transcripción "inducible". Si las células madre sanguíneas se propagaban en la placa de cultivo en presencia de la sustancia, era posible hacer crecer grandes cantidades de células progenitoras sanguíneas monocíticas tardías, etapas precursoras del macrófago. En cuanto se eliminó la sustancia del medio de cultivo, los científicos pudieron estimular a las células para que se diferenciaran definitivamente utilizando estímulos adecuados y mensajeros inmunitarios como el interferón-gamma, y resultaron ser macrófagos funcionales.
Los análisis de la expresión génica de las células así obtenidas demostraron que eran extremadamente similares a los monocitos naturales, los precursores de los macrófagos. Esto también se confirmó mediante pruebas funcionales: los fagocitos inducidos en laboratorio reaccionaron a las citocinas apropiadas y eliminaron bacterias y células apoptóticas.
Los macrófagos utilizan sus receptores Fc para reconocer células que el sistema inmunitario ha marcado como extrañas con anticuerpos. Los fagocitos inducidos en la placa de cultivo mostraban precisamente esta propiedad: eran capaces de captar y eliminar células extrañas marcadas con anticuerpos.
"Nuestros fagocitos inducidos tienen el potencial de destruir células cancerosas en aplicaciones terapéuticas devorándolas. Los macrófagos van a equiparse con una proteína receptora dirigida para dirigirlos específicamente contra las células tumorales. Ahora probaremos esta opción en otros estudios preclínicos con un modelo de ratón", explica Roland Windisch, primer autor del estudio actual.
"En este trabajo, hemos utilizado por primera vez factores de transcripción inducibles para producir específicamente grandes cantidades de un determinado tipo celular fuera del organismo. Mediante el uso de otros factores de transcripción, también puede ser posible utilizar este principio para generar diferentes tipos de células sanguíneas para aplicaciones terapéuticas en la placa de cultivo", dice Christian Wichmann, médico de transfusión en el Hospital LMU y jefe del estudio. De este modo, también podría ser posible producir a gran escala otras células sanguíneas humanas y ofrecer en el futuro una alternativa a la donación de sangre".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Roland Windisch, Sarah Soliman, Adrian Hoffmann, Linping Chen-Wichmann, Anna Danese, Sebastian Vosberg, Jimena Bravo, Sebastian Lutz,... Jürgen Bernhagen, Andreas Humpe, Hannes Klump, Christian Brendel, Daniela S. Krause, Philipp A. Greif, Christian Wichmann et al.; "Engineering an inducible leukemia-associated fusion protein enables large-scale ex vivo production of functional human phagocytes"; Proceedings of the National Academy of Sciences, Volume 121, 2024-6-10