Arrodillar a los patógenos multirresistentes
Los lipopéptidos fluorados actúan como antibióticos muy eficaces
Las infecciones bacterianas multirresistentes que no pueden tratarse con ningún antibiótico conocido suponen una grave amenaza mundial. Un equipo de investigadores chinos acaba de presentar en la revista Angewandte Chemie un método para desarrollar nuevos antibióticos contra los patógenos resistentes. Los fármacos se basan en bloques de proteínas con cadenas lipídicas fluoradas.
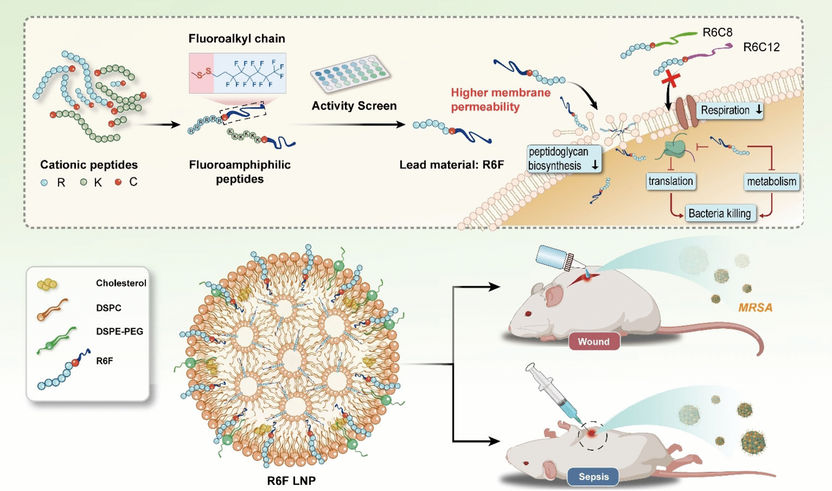
© Wiley-VCH
Los antibióticos suelen recetarse con demasiada facilidad. En muchos países se distribuyen sin receta y se administran en granjas industriales: profilácticamente para prevenir infecciones y mejorar el rendimiento. Como consecuencia, la resistencia va en aumento, cada vez más también contra los antibióticos de reserva. Es esencial desarrollar alternativas innovadoras.
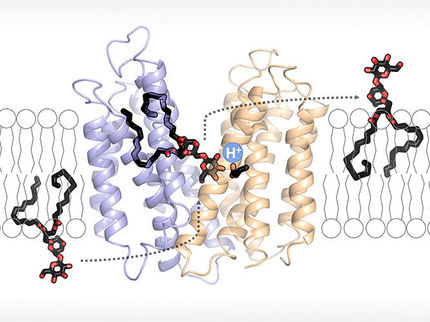
Es posible aprender algunas lecciones de los propios microbios. Las lipoproteínas, pequeñas moléculas proteicas con cadenas de ácidos grasos, son ampliamente utilizadas por las bacterias en sus batallas contra los competidores microbianos. Ya se ha aprobado el uso de varias lipoproteínas como fármacos. Los factores comunes entre las lipoproteínas activas incluyen una carga positiva y una estructura anfifílica, lo que significa que tienen segmentos que repelen la grasa y otros que repelen el agua. Esto les permite unirse a las membranas bacterianas y atravesarlas hasta su interior.
Un equipo dirigido por Yiyun Cheng, de la Universidad Normal de China Oriental, en Shanghai, pretende amplificar este efecto sustituyendo los átomos de hidrógeno de la cadena lipídica por átomos de flúor. De este modo, la cadena lipídica es al mismo tiempo repelente al agua (hidrófoba) y repelente a la grasa (lipofóbica). Su energía superficial especialmente baja refuerza su unión a las membranas celulares, mientras que su lipofobicidad altera la cohesión de la membrana.
El equipo sintetizó un espectro (biblioteca de sustancias) de lipopéptidos fluorados a partir de hidrocarburos fluorados y cadenas peptídicas. Para unirlos, utilizaron el aminoácido cisteína, que los une mediante un puente disulfuro. Los investigadores examinaron las moléculas probando su actividad contra el Staphylococcus aureus resistente a la meticilina (SARM), una cepa bacteriana muy extendida y peligrosa que es resistente a casi todos los antibióticos. El compuesto más eficaz que encontraron fue el "R6F", un lipopéptido fluorado formado por seis unidades de arginina y una cadena lipídica de ocho átomos de carbono y trece de flúor. Para aumentar la biocompatibilidad, el R6F se encerró en nanopartículas de fosfolípidos.
En modelos de ratón, las nanopartículas de R6F demostraron ser muy eficaces contra la sepsis y las infecciones crónicas de heridas por SARM. No se observaron efectos secundarios tóxicos. Las nanopartículas parecen atacar a las bacterias de varias maneras: inhiben la síntesis de importantes componentes de la pared celular, favoreciendo el colapso de las paredes; también perforan la membrana celular y la desestabilizan; alteran la cadena respiratoria y el metabolismo; y aumentan el estrés oxidativo al tiempo que alteran el sistema de defensa antioxidante de las bacterias. En combinación, estos efectos matan a las bacterias, tanto a otras como al SARM. No parece desarrollarse resistencia alguna.
Estos conocimientos proporcionan puntos de partida para el desarrollo de fármacos peptídicos fluorados altamente eficaces para tratar bacterias resistentes a múltiples fármacos.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.