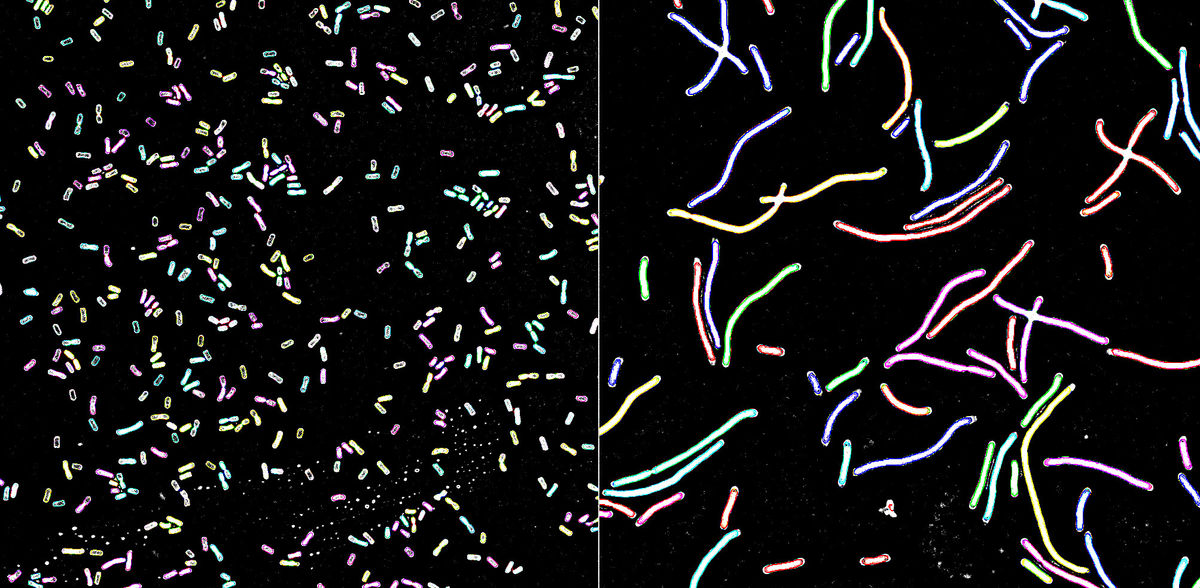Descubierto un nuevo mecanismo de regulación de la división celular en el patógeno bacteriano Klebsiella
Pequeño ácido ribonucleico de gran impacto
Klebsiella pneumoniae es uno de los patógenos bacterianos más comunes y peligrosos que afectan al ser humano, causante de infecciones del tracto gastrointestinal, neumonía, infecciones de heridas e incluso envenenamiento de la sangre. Con el objetivo de descubrir puntos débiles de Klebsiella que puedan aprovecharse terapéuticamente, un equipo de investigación del Grupo de Excelencia en Equilibrio MicroversoEnlace externo de la Universidad de Jena ha estudiado a fondo la biología molecular de la bacteria y ha descubierto la importancia de un pequeño ácido ribonucleico no codificante (ARNs) en la regulación génica de K. pneumoniae. Sus hallazgos se publican en la revista "Proceedings of the National Academy of Sciences".
"Klebsiella es una bacteria relevante para la investigación por varias razones. Por un lado, esta bacteria es problemática en la clínica porque Klebsiella es muy adaptable, capaz de multiplicarse rápidamente y adquirir continuamente nuevas resistencias además de las resistencias naturales existentes a diversos agentes antibióticos. Por otro lado, se sabe poco sobre la regulación génica en Klebsiella, especialmente en comparación con especies estrechamente relacionadas como E. coli o Salmonella", afirma la Dra. Kathrin Fröhlich, jefa del estudio y responsable del grupo de investigación junior de biología del ARN de bacterias de la Universidad de Jena. Junto con un equipo de científicos del Cluster of Excellence, analizó el transcriptoma de Klebsiella en busca de sRNA desconocidos hasta entonces y de pistas sobre sus funciones.
"Además de muchos ARNsr que ya se conocían de bacterias relacionadas, también encontramos más de 50 nuevos reguladores potenciales", afirma Eric Ruhland, primer autor del estudio y candidato a doctor en el Cluster de Excelencia "Equilibrio del Microverso" de Jena. Los investigadores determinaron los socios de interacción de todos estos ARNs mediante un método basado en la secuenciación de alto rendimiento.
Control autónomo de la división celular
Al analizar los emparejamientos de ARN identificados de este modo, el sARN DinR despertó el interés particular de los investigadores. "Finalmente pudimos averiguar que DinR es producido por la célula cuando se produce un daño en el ADN. En estas condiciones, DinR inhibe la formación de FtsZ, una proteína estructural importante para la división celular", explica Ruhland. DinR controla así otro mecanismo, hasta ahora desconocido, con el que la bacteria puede interrumpir la división celular si hay defectos en el material genético. Esto sirve para dar tiempo a la célula a reparar el genoma dañado antes de que se transmita a otra generación de la bacteria - desde una perspectiva evolutiva, un mecanismo que sirve para producir descendencia lo más sana posible.
"Sin embargo, la reparación del ADN es propensa a errores y esta situación de estrés conduce a una mayor tasa de mutación", afirma Fröhlich. Estos cambios en el material genético también pueden dar lugar a nuevas resistencias a los antibióticos o modificar la resistencia de las bacterias. "En el futuro, queremos entender cómo se enfrenta exactamente la Klebsiella a los daños en el ADN y qué papel desempeñan los ARNs en la comparativamente alta adaptabilidad de la especie bacteriana, que está haciendo que la Klebsiella sea cada vez más problemática en entornos clínicos", dice el jefe del grupo de investigación junior. "Con este estudio, estamos contribuyendo a una mejor comprensión de los procesos biológicos moleculares fundamentales en Klebsiella, lo que también puede abrir vías para tratar las infecciones de una manera más específica."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Eric Ruhland, Malte Siemers, Ruman Gerst, Felix Späth, Laura Nicole Vogt, Marc Thilo Figge, Kai Papenfort, Kathrin Sophie Fröhlich; "The global RNA–RNA interactome of Klebsiella pneumoniae unveils a small RNA regulator of cell division"; Proceedings of the National Academy of Sciences, Volume 121, 2024-2-20