Con ácido fórmico hacia la neutralidad del CO₂.
Investigadores desarrollan un nuevo método para el uso sostenible del CO₂
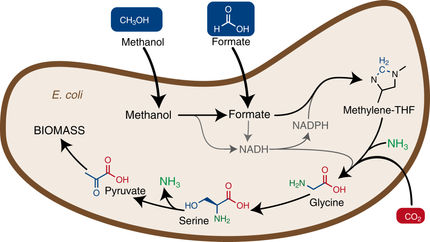
Las nuevas vías metabólicas sintéticas para la fijación delCO2 no sólo podrían contribuir a reducir el contenido deCO2 de la atmósfera, sino también a sustituir los procesos convencionales de fabricación química de productos farmacéuticos y principios activos por procesos biológicos neutros en carbono. Un nuevo estudio demuestra un proceso que puede convertir elCO2 en un material valioso para la industria (bio)química a través del ácido fórmico.

El formiato puede concebirse como el núcleo de una bioeconomía neutra en carbono, en la que se produzca a partir de CO2 por medios (electro)químicos y se convierta en productos de valor añadido mediante cascadas enzimáticas o microbios artificiales. Un paso clave en la expansión de la asimilación sintética del formiato es su reducción termodinámica a formaldehído, visible aquí como un cambio de color amarillo.
© Max Planck Institute for Terrestrial Microbiology/Geisel
Ante el aumento de las emisiones de gases de efecto invernadero, la captura de carbono, es decir, el secuestro delCO2 procedente de grandes fuentes de emisión, es una cuestión urgente. En la naturaleza, la asimilación deCO2 lleva millones de años produciéndose, pero su capacidad dista mucho de ser suficiente para compensar las emisiones de origen humano.
Los investigadores dirigidos por el Prof. Dr. Tobias Erb, del Instituto Max Planck de Microbiología Terrestre, están utilizando la caja de herramientas de la naturaleza para desarrollar nuevas formas de fijación delCO2. Ahora han conseguido desarrollar una vía metabólica artificial que produce el altamente reactivo formaldehído a partir del ácido fórmico, un posible producto intermedio de la fotosíntesis artificial. El formaldehído podría introducirse directamente en varias vías metabólicas para formar otras sustancias valiosas sin ningún efecto tóxico.
Como en el proceso natural, se necesitan dos componentes primarios: Energía y carbono. La primera puede obtenerse no sólo de la luz solar directa, sino también de la electricidad, por ejemplo, de módulos solares.
El ácido fórmico es un componente C1 con potencial
Dentro de la cadena de valor añadido, la fuente de carbono es variable. ElCO2 no es la única opción, todos los monocarbonos (componentes básicos C1) entran en juego: CO (monóxido de carbono), ácido fórmico, formaldehído, metanol y metano. Sin embargo, casi todas estas sustancias son muy tóxicas, ya sea para los organismos vivos (CO, formaldehído, metanol) o para el planeta (metano como gas de efecto invernadero). Sólo el ácido fórmico, cuando se neutraliza a su base formiato, es tolerado por muchos microorganismos en altas concentraciones.
"El ácido fórmico es una fuente de carbono muy prometedora", subraya la Dra. Maren Nattermann, primera autora del estudio, publicado recientemente en la revista Nature Communications. "Pero convertirlo en formaldehído en el tubo de ensayo consume bastante energía". Esto se debe a que la sal del ácido fórmico, el formiato, no puede convertirse fácilmente en formaldehído. "Hay una seria barrera química entre las dos moléculas que tenemos que salvar con energía bioquímica -ATP- antes de poder realizar la reacción real".
El objetivo del investigador era encontrar una forma más económica. Al fin y al cabo, cuanta menos energía se necesite para introducir carbono en el metabolismo, más energía quedará para impulsar el crecimiento o la producción. Pero ese camino no existe en la naturaleza.
"Hace falta cierta creatividad para descubrir las llamadas enzimas promiscuas con múltiples funciones", afirma Tobias Erb. "Sin embargo, el descubrimiento de enzimas candidatas es sólo el principio. Hablamos de reacciones que se pueden contar porque son muy lentas: en algunos casos, menos de una reacción por segundo por enzima. Las reacciones naturales pueden ocurrir mil veces más rápido".
Aquí es donde entra en juego la bioquímica sintética, dice Maren Nattermann: "Si conoces la estructura y el mecanismo de una enzima, sabes dónde intervenir. Aquí, nos beneficiamos significativamente del trabajo preliminar de nuestros colegas en investigación básica".
El uso de tecnología de alto rendimiento acelera la optimización de enzimas
La optimización de las enzimas constó de varios enfoques: se intercambiaron específicamente bloques de construcción (mutagénesis dirigida) y se generaron y seleccionaron mutaciones aleatorias por su capacidad (mutagénesis semirracional). "Tanto el formiato como el formaldehído son maravillosamente adecuados porque penetran en las paredes celulares. Podemos poner formiato en el medio de cultivo de las células que producen nuestras enzimas y, al cabo de unas horas, convertir el formaldehído producido en un tinte amarillo no tóxico", explica Maren Nattermann.
El resultado no habría sido posible en tan poco tiempo sin el uso de métodos de alto rendimiento. Para lograrlo, los investigadores colaboraron con su socio industrial Festo SE & Co. KG, con sede en Esslingen (Alemania). "Tras unas 4.000 variantes, conseguimos cuadruplicar la producción", afirma Maren Nattermann. "Hemos creado así la base para que el organismo modelo E.coli, el caballo de batalla microbiano de la biotecnología, crezca en ácido fórmico. Por ahora, sin embargo, nuestras células sólo pueden producir formaldehído, no convertirlo más."
Con su socio de colaboración, el Dr. Sebastian Wenk, del MPI de Fisiología Molecular de Plantas, los investigadores están desarrollando actualmente una cepa que pueda captar los productos intermedios e introducirlos en el metabolismo central. Paralelamente, el equipo está investigando con un grupo de trabajo del MPI de Conversión Química de la Energía dirigido por el Prof. Dr. Walter Leitner sobre la conversión electroquímica deCO2 en ácido fórmico. El objetivo a largo plazo es una "plataforma todo en uno", desde elCO2 mediante un proceso electrobioquímico hasta productos como la insulina o el biodiésel.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Nattermann, M.; Wenk, S.; Pfister, P.; He, h.; Lee, S.H.; Szymanski, W.; Guntermann, N.; Zhu, F.; Nickel, L.; Wallner, C.; Zarzycki, J.; Paczia, N.; Gaißert, N.; Franciò, G.; Leitner, N.; Gonzalez, R.; Erb, T. J.; Engineering a new-to-nature cascade for phosphate-dependent formate to formaldehyde conversion in vitro and in vivo; Nature Communications 14, 2682 (2023)