Ataque a través de carreteras
Nuevas perspectivas para el tratamiento de tumores, enfermedades autoinmunes o estados inflamatorios crónicos
El aumento de la Proliferación celular es una característica clave de enfermedades como el cáncer. Un equipo de investigación de la Universidad de Würzburg y dos Institutos Leibniz ha conseguido ahora influir indirectamente en este proceso.
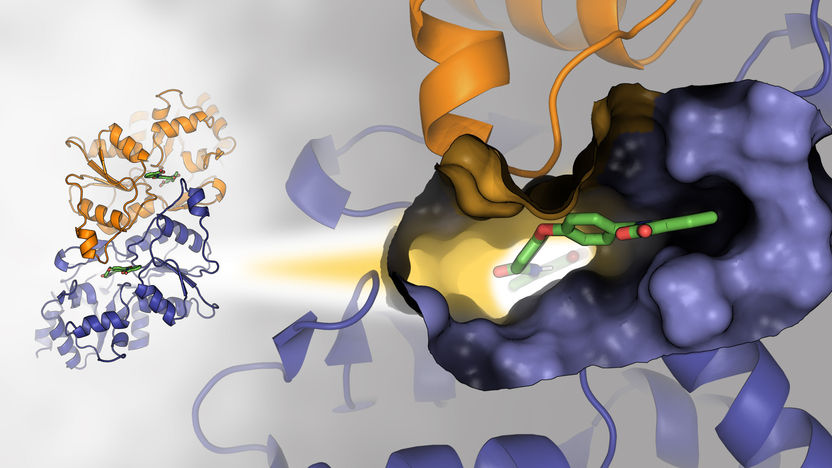
Estructura dimérica de la fosfoglicolato fosfatasa. La sección ampliada de la derecha muestra el bolsillo de unión al ligando en complejo con la pequeña molécula inhibidora CP1.
Natalia Yuan-Chen
Por muy diferentes que sean los cánceres o las enfermedades autoinmunes, como la esclerosis múltiple, la artritis reumatoide o la psoriasis, todas ellas tienen una característica en común: van acompañadas de un aumento de la proliferación celular. En consecuencia, las células enfermas deben aumentar enérgicamente su producción de bloques moleculares, lo que está inevitablemente ligado a un gran aumento de la demanda de energía.
Por lo tanto, el control de la producción celular de bloques de construcción para la síntesis de macromoléculas y la homeostasis energética es una estrategia importante en el desarrollo de nuevos fármacos contra dichas enfermedades. Un equipo de científicos de la Universidad Julius-Maximilians de Würzburg (JMU) ha logrado dar un paso importante en esta dirección. Utilizando una diana farmacológica hasta ahora inexplorada, lograron influir en estos procesos celulares.
Publicación en Nature Communications
La autora principal del estudio, que se ha publicado en la revista Nature Communications, es Antje Gohla, profesora de Farmacología Bioquímica del Departamento de Farmacología y Toxicología de la JMU. En este trabajo también han participado equipos del Centro Rudolf Virchow (RVZ) de Imagen Integrativa y Traslacional, el Biocentro y el Instituto de Farmacia de la JMU, así como el Instituto Leibniz de Farmacología Molecular-FMP de Berlín y el Instituto Leibniz de Ciencias Analíticas-ISAS de Dortmund.
"Un objetivo típico para el desarrollo de nuevos fármacos es la preferencia de muchas células por el azúcar en forma de glucosa como uno de los principales proveedores de energía y bloques de construcción, ya que la glucosa es una molécula versátil y casi polivalente en el metabolismo", explica Antje Gohla. Sin embargo, el éxito terapéutico de esta estrategia ha sido limitado hasta ahora.
Un aspecto importante del metabolismo humano ha sido ignorado por los investigadores durante mucho tiempo: "En paralelo a las conocidas vías de descomposición y conversión de la glucosa, funcionan en segundo plano numerosos "procesos de reparación", que son fundamentales para el buen funcionamiento del metabolismo", explica Gohla.
Inhibición de importantes procesos de reparación
El equipo de investigación se centró en estos procesos en su estudio. En concreto, los científicos investigaron la cuestión de si estos procesos de reparación podrían ser adecuados como objetivos farmacológicos. La respuesta es clara: "Por primera vez, pudimos identificar un compuesto que inhibe selectivamente la actividad de la llamada fosfoglicolato fosfatasa, una importante enzima de reparación en el metabolismo del azúcar", explica el farmacólogo. En el tubo de ensayo, el compuesto bloquea efectivamente la proliferación de las células tumorales.
Las fosfatasas suelen considerarse objetivos farmacológicos difíciles. Por ello, el equipo está especialmente satisfecho de haber logrado identificar y caracterizar un inhibidor de fosfatasas estructuralmente novedoso.
Importante apoyo de la biología estructural
En esta búsqueda, Gohla contó con el apoyo de expertos en cribado de alto rendimiento, metabolómica, biología estructural y química médica. Con su ayuda, dijo, fue posible dilucidar en detalle el mecanismo de acción molecular de un inhibidor de la fosfoglicolato fosfatasa.
El profesor Hermann Schindelin, del Centro Rudolf Virchow, realizó una importante contribución al dilucidar la estructura tridimensional de la fosfoglicolato fosfatasa en complejo con el inhibidor mediante el análisis de la estructura cristalina de rayos X. "La visualización del fármaco en proximidad espacial al sitio activo no sólo explica los datos cinéticos de la enzima, sino que, sobre todo, proporciona un punto de partida para el futuro desarrollo de una nueva generación de inhibidores con mejores propiedades de unión", explica el biólogo estructural.
Perspectivas de nuevas terapias
En general, los resultados demuestran que todavía hay objetivos farmacológicos sin explotar en el metabolismo celular del azúcar. Mientras que la investigación se ha centrado hasta ahora en las principales vías metabólicas de la glucosa, que también son vitales para muchas células sanas, este nuevo enfoque se dirige a la mayor necesidad de las células asociadas a la enfermedad de realizar procesos de reparación. "El concepto es dirigirse farmacológicamente a la mayor necesidad de las células tumorales o de las células inmunitarias equivocadas para los procesos de reparación metabólica, de manera que estas células se envenenan acumulando subproductos metabólicos tóxicos", explica Gohla.
Sin embargo, aún queda un largo camino por recorrer antes de que estos compuestos puedan utilizarse como fármacos. No obstante, los autores del estudio esperan que, a partir de sus hallazgos fundamentales, se abran en el futuro nuevas perspectivas para el tratamiento de tumores, enfermedades autoinmunes o afecciones inflamatorias crónicas.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Glycolytic flux control by drugging phosphoglycolate phosphatase. Elisabeth Jeanclos, Jan Schlötzer, Kerstin Hadamek, Natalia Yuan-Chen, Mohammad Alwahsh, Robert Hollmann, Stefanie Fratz, Dilan Yesilyurt-Gerhards, Tina Frankenbach, Daria Engelmann, Angelika Keller, Alexandra Kaestner, Werner Schmitz, Martin Neuenschwander, Roland Hergenröder, Christoph Sotriffer, Jens Peter von Kries, Hermann Schindelin, Antje Gohla. Nature Communications; 2022