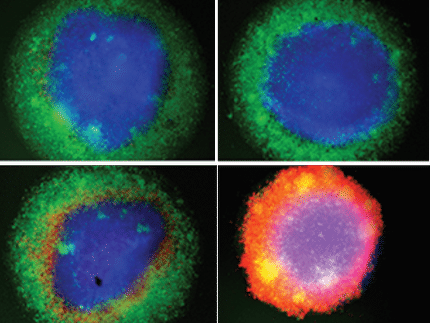
Una nueva y prometedora terapia contra los tumores sólidos positivos para MAGE-A1
T-knife Therapeutics anuncia la dosificación del primer paciente con TK-8001 en el ensayo clínico de fase 1/2 IMAG1NE
T-knife Therapeutics, Inc. una compañía biofarmacéutica en fase clínica dedicada al desarrollo de inmunoterapias basadas en receptores de células T que proporcionan beneficios transformadores a los pacientes con cáncer, anunció que ha dosificado al primer paciente en el ensayo clínico de fase 1/2 IMAG1NE. El ensayo IMAG1NE está diseñado para evaluar la seguridad y la eficacia preliminar de TK-8001, una terapia de células T (TCR-T) específica para el gen del antígeno asociado al melanoma (MAGE-A1), en pacientes con tumores sólidos.
Imagen simbólica
Computer generated picture
"Creemos que nuestra plataforma MyT se distingue por su capacidad de identificar TCRs que han sido optimizados de forma natural en cuanto a afinidad, especificidad y mantenimiento de la función de las células T a largo plazo, lo que convierte a TK-8001 en una nueva y prometedora terapia dirigida a los tumores sólidos positivos para MAGE-A1", declaró el doctor Eugen Leo, director médico de T-knife. "Nuestro ensayo IMAG1NE combina un TCR con el mejor potencial de su clase, una fabricación diseñada para seleccionar las células T más potentes y unos criterios de selección de pacientes guiados por biomarcadores que buscan inscribir a aquellos pacientes que creemos que tienen la mayor probabilidad de obtener respuestas seguras, profundas y duraderas a TK-8001."
"Estamos entusiasmados por llevar a la clínica nuestro primer candidato a producto derivado de la plataforma MyT", añadió Thomas M. Soloway, director general de T-knife. "Este es un hito significativo que representa el rápido progreso en T-knife, y estamos agradecidos por el apoyo y la confianza que hemos recibido de nuestros numerosos colaboradores, investigadores y la comunidad de pacientes mientras perseguimos nuestro objetivo de construir una compañía global centrada en llevar el poder de las terapias basadas en el TCR a los pacientes con cáncer."
En estudios preclínicos, el TCR dirigido a MAGE-A1 incorporado en TK-8001 mostró una alta afinidad y especificidad de unión a un epítopo de MAGE-A1 presentado en HLA-A*02:01. Es importante destacar que las células T que incorporan el TCR TK-8001 derivado de la Plataforma MyT demostraron una actividad de eliminación en serie in vitro y una mayor actividad antitumoral in vivo en comparación con las células T diseñadas con TCRs derivados de donantes humanos.
El ensayo de fase 1/2 IMAG1NE es un ensayo de fase 1/2 multicéntrico, abierto y de dosificación acelerada, diseñado para evaluar la seguridad y la eficacia preliminar de TK-8001 en pacientes con tumores sólidos MAGE-A1 positivos. La parte de fase 1 del estudio se centra en la selección de una dosis para pasar a la parte de fase 2 del estudio. La parte de escalada de dosis de la fase 1 está diseñada para inscribir aproximadamente de 6 a 18 pacientes a fin de evaluar la seguridad y la tolerabilidad de TK-8001 a varias dosis. Una vez que se haya identificado la dosis recomendada para la fase 2, el TK-8001 se evaluará en una parte de expansión del ensayo.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Más noticias del departamento investigación y desarrollo
Noticias más leídas
Más noticias de nuestros otros portales
Algo está pasando en la industria de las ciencias de la vida ...
Así es el verdadero espíritu pionero: Muchas start-ups innovadoras están aportando ideas frescas, savia nueva y espíritu emprendedor para cambiar el mundo del mañana a mejor. Sumérjase en el mundo de estas jóvenes empresas y aproveche la oportunidad de ponerse en contacto con los fundadores.