La inteligencia artificial pliega moléculas de ARN
Nuevas estructuras fiables y predecibles
La estructura espacial de las moléculas de ARN es crucial para su funcionamiento. Pero predecirla es un reto.
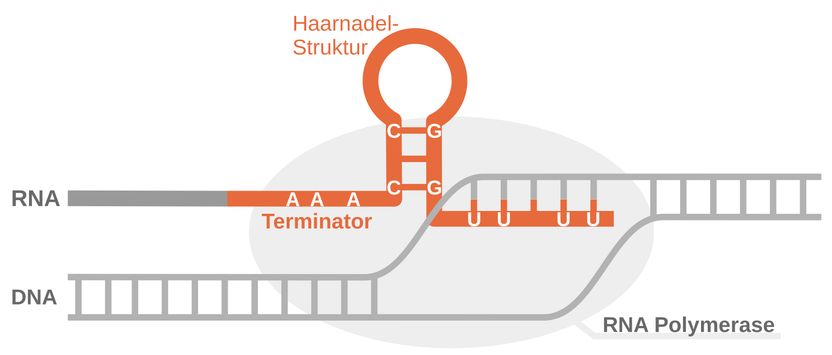
Algunos segmentos de una molécula de ARN (naranja) forman las llamadas estructuras de horquilla.
© Vivian Brandenburg
Para la función de muchas biomoléculas, su estructura tridimensional es crucial. Por ello, los investigadores no sólo se interesan por la secuencia de cada uno de los componentes de las biomoléculas, sino también por su estructura espacial. Con la ayuda de la inteligencia artificial (IA), los bioinformáticos ya pueden predecir con fiabilidad la estructura tridimensional de una proteína a partir de su secuencia de aminoácidos. Sin embargo, en el caso de las moléculas de ARN, esta tecnología aún está en pañales. Investigadores de la Ruhr-Universität Bochum (RUB) describen en la revista PLOS Computational Biology del 7 de julio de 2022 una forma de utilizar la IA para predecir con fiabilidad la estructura de ciertas moléculas de ARN a partir de su secuencia de nucleótidos.
Para el trabajo, los equipos dirigidos por Vivian Brandenburg y el profesor Franz Narberhaus de la Cátedra de Biología de Microorganismos de la RUB cooperaron con el profesor Axel Mosig del Área de Competencia de Bioinformática del Centro de Diagnóstico de Proteínas de Bochum.
Hay que tener en cuenta el entorno celular
"El ARN suele considerarse únicamente un mensajero entre el ADN genómico y las proteínas", afirma Axel Mosig. "Pero muchas moléculas de ARN asumen funciones celulares". Su estructura espacial es importante para ello. Regiones similares en una secuencia de nucleótidos pueden agruparse para formar arreglos tridimensionales.
"Identificar estas autosimilitudes en una secuencia de ARN es como un rompecabezas matemático", explica Vivian Brandenburg. Existe un modelo biofísico para este rompecabezas con sus correspondientes algoritmos de predicción. Sin embargo, el modelo no puede tener en cuenta el entorno celular del ARN, que también influye en el proceso de plegado. "Si el ARN estuviera aislado y flotando en una solución acuosa, el modelo podría predecir la estructura con mucha precisión", dice Brandenburg. Pero una célula viva contiene muchos otros componentes.
Aquí es donde entra en juego la inteligencia artificial. La IA puede aprender patrones sutiles del entorno celular basándose en estructuras conocidas. A continuación, podría incorporar estos hallazgos a sus predicciones estructurales. Sin embargo, para el proceso de aprendizaje, la IA necesita suficientes datos de entrenamiento, algo que no existe en la práctica.
Obtención de datos de entrenamiento con un truco
Para resolver el problema de la falta de datos de entrenamiento, el equipo de Bochum utilizó un truco: los investigadores trabajaron con motivos estructurales de ARN conocidos. Utilizando una especie de marcha atrás, pudieron generar casi cualquier número de secuencias de nucleótidos a partir de los modelos energéticos de estas estructuras que se plegarían en estas estructuras espaciales. Con la ayuda de este llamado plegado inverso, los investigadores generaron muchos pares de secuencias de nucleótidos y estructuras con los que pudieron entrenar a la IA.
Nuevas estructuras predecibles de forma fiable
A continuación, los investigadores enfrentaron a la IA a una nueva tarea: tenía que predecir la estructura de ciertas moléculas de ARN bacteriano. Estas moléculas, llamadas terminadores de transcripción, son importantes señales de parada en la traducción del ADN genómico en las bacterias. A menudo, como muchas otras moléculas de ARN con importantes funciones celulares, están ocultas en el genoma y son difíciles de distinguir de las zonas con otras funciones.
La inteligencia artificial fue capaz de reconocer y predecir de forma fiable la estructura típica de los terminadores de transcripción, que recuerda a una horquilla. El equipo de investigación pudo demostrarlo utilizando datos experimentales disponibles públicamente.
"Mientras que los enfoques de la IA son ya casi inevitables en la predicción de las estructuras de las proteínas, el desarrollo de las estructuras del ARN no ha hecho más que empezar", resume Axel Mosig.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.