¿Grasa saludable? El factor de transcripción C/EBPβ influye positivamente en el almacenamiento de grasa
¿Podremos pronto controlar el almacenamiento del exceso de grasa?
La enfermedad nutricional y metabólica crónica de la obesidad se caracteriza por un aumento excesivo de la grasa corporal y su acumulación en los tejidos. Quienes padecen obesidad también tienen un mayor riesgo de padecer enfermedades concomitantes o secundarias, como la diabetes de tipo 2, la enfermedad del hígado graso y la aterosclerosis. Investigadores del Instituto Europeo de Investigación sobre la Biología del Envejecimiento (ERIBA) de Groningen (Países Bajos) y del Instituto Leibniz sobre el Envejecimiento - Instituto Fritz Lipmann (FLI) de Jena (Alemania) han demostrado ahora por primera vez en un modelo de ratón cómo el factor de transcripción C/EBPβ puede influir positivamente en el almacenamiento de grasa y mantener la salud incluso bajo una dieta especialmente rica en grasas.
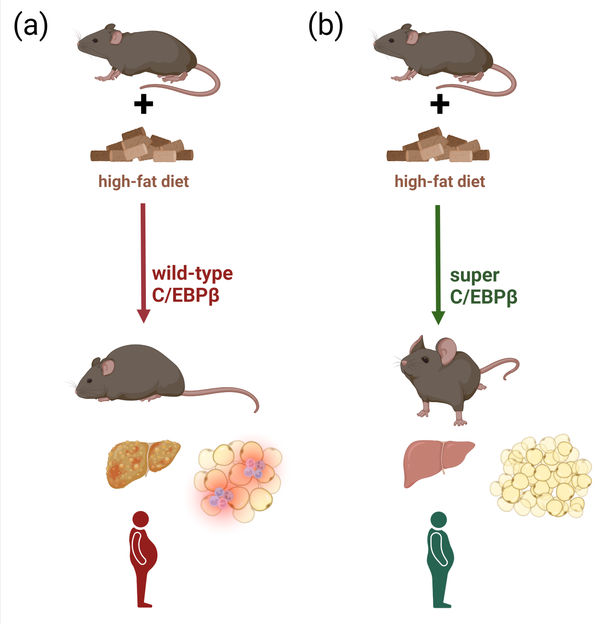
Los ratones modificados genéticamente con una mayor función del factor de transcripción C/EBPβ (b) almacenan el exceso de grasa en el tejido adiposo hiperplásico. Con una dieta alta en grasas, estos ratones muestran un tejido adiposo menos inflamado y son significativamente más sanos.
FLI / Kerstin Wagner; created with BioRender.com
En los últimos años, el número de personas con sobrepeso y obesidad en los países industrializados ha aumentado considerablemente. En Alemania, por ejemplo, una de cada dos personas tiene ahora sobrepeso, y cerca del 20% de la población es obesa. La obesidad se define como un peso corporal excesivo causado por una proporción extremadamente alta de grasa, generalmente debida a una acumulación de grasa en células grasas (adipocitos) muy agrandadas (hipertróficas) en el abdomen. Esta llamada grasa visceral conduce a la inflamación, que desempeña un papel fundamental en el desarrollo y la progresión de diversos trastornos metabólicos, como la diabetes de tipo 2, las enfermedades cardíacas, los accidentes cerebrovasculares y ciertos cánceres. Por este motivo, el aumento mundial de la prevalencia de la obesidad es una preocupación creciente para la salud pública, y se están investigando intensamente los vínculos entre la obesidad y los problemas de salud.
En un estudio reciente publicado en la revista eLife, investigadores del Instituto Europeo de Investigación para la Biología del Envejecimiento (ERIBA) de Groningen (Países Bajos) y del Instituto Leibniz sobre el Envejecimiento - Instituto Fritz Lipmann (FLI) de Jena (Alemania) han demostrado ahora que los ratones modificados genéticamente con una función aumentada del factor de transcripción C/EBPβ pueden almacenar el exceso de grasa de tal manera que se mantienen sanos incluso en condiciones de estrés, como una dieta marcadamente rica en grasas.
El lugar de almacenamiento de la grasa influye en la salud
El almacenamiento de grasa en el depósito de grasa visceral se produce principalmente a través del aumento de tamaño de las células grasas individuales (almacenamiento de grasa hipertrófica). Sin embargo, cuando estas células alcanzan su máxima capacidad de almacenamiento, la ingesta continuada de grasa comienza a acumularse de forma perjudicial en los tejidos fuera de los depósitos de grasa (esteatosis), especialmente en el hígado y los músculos, lo que provoca un deterioro de la función de estos tejidos. "Sin embargo, hay un subgrupo de personas que, a pesar de ser obesas durante un largo periodo de tiempo, no experimentan ningún problema de salud apreciable", informa el profesor Cornelis Calkhoven, antiguo jefe de grupo de investigación en el FLI que ahora trabaja en ERIBA.
Estudios anteriores han demostrado que dos cosas en particular contribuyen a este fenotipo de obesidad saludable: En primer lugar, la grasa que no se almacena en el abdomen, sino como grasa subcutánea bajo la piel de los brazos, los muslos y la espalda, es mejor para la salud. Además, la grasa que se almacena en el llamado tejido adiposo hiperplásico, que se forma por un aumento del número de células grasas (almacenamiento de grasa hiperplásica), también es mucho menos probable que cause daños. Al haber más células disponibles para el almacenamiento de grasa, éstas siguen siendo más pequeñas y, por tanto, son metabólicamente más sanas y se inflaman menos. "Sin embargo, nuestro conocimiento de los factores genéticos que regulan las mencionadas condiciones favorables de almacenamiento de grasa es todavía muy limitado y requiere estudios más detallados", añade el profesor Calkhoven.
El aumento de la función del factor de transcripción C/EBPβ controla el almacenamiento de grasa
Cuando se alimenta a los ratones con una dieta alta en grasas en el laboratorio, en poco tiempo ganan peso, se vuelven obesos y desarrollan problemas metabólicos similares a los de los humanos obesos, incluyendo la inflamación del tejido adiposo, la acumulación de grasa en tejidos normalmente libres de grasa como el hígado y los músculos, y la diabetes de tipo 2.
"En nuestro estudio actual, hemos podido demostrar, por un lado, que los ratones modificados genéticamente con una función aumentada del factor de transcripción C/EBPβ almacenan el exceso de grasa principalmente en el tejido adiposo hiperplásico, con más células grasas y más pequeñas", informa la Dra. Christine Müller, de ERIBA. Incluso con dietas extremadamente ricas en grasas, estos ratones con superfunción de C/EBPβ presentan menos inflamación del tejido adiposo, no acumulan grasa en el hígado o el corazón y mantienen un metabolismo de la glucosa saludable. Por otra parte, en los machos, la superfunción de C/EBPβ también estimula el almacenamiento favorable de grasa en depósitos bajo la piel. "Ambos son factores que contribuyen a un fenotipo obeso saludable en los seres humanos", afirmó el Dr. Müller.
En dos estudios publicados anteriormente, los investigadores de Jena y Groningen ya demostraron que los mismos ratones con superfunción del C/EBPβ, con una dieta normal, tienen un metabolismo generalmente mejorado, lo que también se asocia con menos cáncer y un pronunciado retraso en varias enfermedades relacionadas con el envejecimiento en comparación con sus compañeros de camada de tipo salvaje.
¿Podremos pronto controlar el almacenamiento del exceso de grasa?
"Nuestros estudios aportan pruebas impresionantes de que la superfunción de C/EBPβ adapta la fisiología de los ratones hacia un metabolismo más saludable, incluso en condiciones nutricionales poco saludables, como cuando se estresa con una dieta alta en grasas", explicó el profesor Calkhoven, resumiendo los hallazgos. "El estudio actual identifica el factor de transcripción C/EBPβ como un regulador clave del almacenamiento de grasa saludable, pero al mismo tiempo plantea la cuestión de si la inducción farmacológica de la superfunción de C/EBPβ puede utilizarse potencialmente para redirigir el almacenamiento del exceso de grasa del modo hipertrófico perjudicial al modo hiperplásico más beneficioso. Esto tendría inmensas implicaciones para la salud metabólica y el envejecimiento".
Los estudios iniciales ya han demostrado que una estrategia farmacológica de este tipo dirigida a C/EBPβ es, en principio, factible. El desarrollo de tales fármacos tendría, pues, enormes implicaciones para el tratamiento de la obesidad y las enfermedades metabólicas relacionadas.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Enhanced C/EBPβ function promotes hyperplastic versus hypertrophic fat tissue growth and prevents steatosis in response to high-fat diet feeding. Müller C, Zidek LM, Eichwald S, Kortman G, Koster MH, Calkhoven CF. eLife 2022, 11, e62625.
Reduced expression of C/EBPβ-LIP extends health- and lifespan in mice. Müller C, Zidek LM, Ackermann T, de Jong T, Liu P, Kliche V, Zaini MA, Kortman G, Harkema L, Verbeek DS, Tuckermann JP, von Maltzahn J, de Bruin A, Guryev V, Wang ZQ, Calkhoven CF. eLife 2018, 7, e34985.
A screening strategy for the discovery of drugs that reduce C/EBPβ-LIP translation with potential calorie restriction mimetic properties. Zaini MA, Müller C, Ackermann T, Reinshagen J, Kortman G, Pless O, Calkhoven CF. Scientific Rep. 2017, 7, 42603.