Infecciones fúngicas: La cooperación microbiana conduce a la tolerancia a los medicamentos
Las infecciones por hongos representan un problema de salud cada vez más importante y son más peligrosas de lo que se pensaba
El tratamiento de las infecciones fúngicas suele verse obstaculizado por hongos patógenos que no responden, o son tolerantes, a los fármacos antifúngicos. Un equipo de investigadores de la Charité - Universitätsmedizin Berlin y del Instituto Francis Crick ha identificado ahora la cooperación microbiana como una de las causas de esta tolerancia a los fármacos. La relación de colaboración y las interacciones a nivel metabólico benefician a toda la comunidad de células de levadura, tanto en su crecimiento como en su supervivencia. El mecanismo subyacente, que se ha descrito en Nature Microbiology, abre nuevas vías en el desarrollo de mejores terapias antimicrobianas.
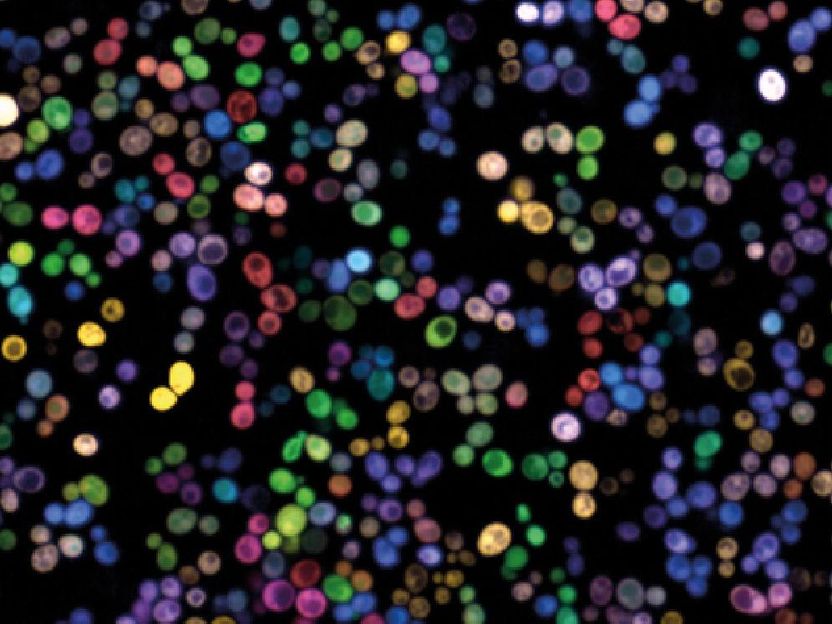
Células que interactúan metabólicamente tras el tratamiento con antifúngicos (los diferentes colores en el análisis de microscopía de fluorescencia SeMeCo ilustran la capacidad de las células para producir sus propios metabolitos).
© Francis Crick Institute | Mary Wu
Las infecciones fúngicas representan un problema sanitario cada vez más importante y son más peligrosas de lo que se pensaba. Cada año mueren en el mundo más personas por infecciones fúngicas invasivas que por la malaria y, sin embargo, sólo hay tres clases de fármacos antifúngicos que pueden tratar estas infecciones. Sin embargo, el uso clínico de estos fármacos se ve obstaculizado por el hecho de que los microorganismos que causan las infecciones suelen desarrollar tolerancia a estos "antimicóticos", lo que significa que el tratamiento suele fracasar.
¿Cómo se desarrolla esta tolerancia a los fármacos? ¿Qué papel desempeñan las interacciones microbianas y qué beneficios se asocian a ellas? Un equipo formado por investigadores de la Charité de Berlín y del Instituto Francis Crick de Londres ha descubierto un mecanismo que relaciona las interacciones metabólicas microbianas con la tolerancia a los fármacos. "Descubrimos que las células de levadura se relacionan frecuente y activamente entre sí, y que estas interacciones implican el intercambio de metabolitos. También pudimos demostrar cómo esto crea tanto ventajas de crecimiento como tolerancia a antimicóticos comunes", dice el último autor del estudio, el Prof. Dr. Markus Ralser, Director del Instituto de Bioquímica de Charité y Jefe de Grupo del Instituto Francis Crick. El artículo publicado marca el primer hito impresionante de un proyecto que se puso en marcha en 2020 y que se lleva a cabo en colaboración con la Universidad de Tel Aviv. Dedicado al estudio de la tolerancia a los fármacos en las infecciones fúngicas, el proyecto cuenta con el apoyo de una subvención de sinergia del Consejo Europeo de Investigación (ERC).
Las comunidades microbianas se componen tanto de células que funcionan normalmente como de células con el metabolismo alterado. Estas últimas (también conocidas como células auxotróficas) han perdido la capacidad de producir ciertos metabolitos esenciales y deben absorberlos de las células metabólicamente competentes (prototróficas) presentes en su entorno. La cuestión de si las células de esta comunidad se benefician de esta existencia comunitaria, y en qué medida, era hasta ahora uno de los principales problemas sin resolver en el campo de la microbiología. Ahora, los autores de este estudio han podido desvelar al menos parte del misterio.
Para estudiar la coexistencia de estos diferentes tipos de células, los investigadores utilizaron un enfoque metagenómico, es decir, analizaron la composición genética de todas las comunidades microbianas presentes en el entorno. Utilizando un conjunto de datos cotejados de numerosos laboratorios y que comprende datos de más de 12.000 comunidades de especies microbianas de todo el mundo, los investigadores descubrieron que las comunidades con células tanto auxotróficas como prototróficas son extremadamente comunes. "Estas células metabólicamente deficientes (auxotróficas) son particularmente comunes en las comunidades cooperativas vinculadas al huésped -especialmente en el microbioma intestinal-, donde parecen disfrutar de una ventaja", explica el profesor Ralser de Einstein. "Sospechamos que su ubicuidad puede explicarse por los cambios en su entorno metabólico compartido, en particular el entorno proporcionado por el huésped que presenta los metabolitos necesarios".
Para comprender los mecanismos bioquímicos subyacentes, los investigadores utilizaron un modelo de levadura de cooperación metabólica que les permitió observar poblaciones de células metabólicamente deficientes y metabólicamente competentes de forma aislada. A continuación, analizaron estas poblaciones celulares mediante tecnologías proteómicas y metabolómicas de alto rendimiento de última generación, además de la modelización metabólica y las pruebas de susceptibilidad a los fármacos. Al combinar estas tecnologías, los investigadores descubrieron que los microorganismos metabólicamente deficientes que viven en comunidades cooperativas junto a los metabólicamente competentes adaptan sus metabolismos para favorecer la exportación de metabolitos. En particular, esta estrategia también facilita que estos microorganismos expulsen una serie de sustancias antimicrobianas.
"Este mecanismo tiene beneficios para ambas poblaciones celulares", resume el profesor Ralser. Y continúa: "Al aumentar su actividad exportadora, los microorganismos metabólicamente interactivos ayudan a crear un entorno común rico en metabolitos, que las células de la comunidad necesitan para su crecimiento y supervivencia. Esto significa que incluso los microorganismos metabólicamente competentes se benefician de esta relación de cooperación. Además, se reducen los niveles de principios activos en el interior de las células, lo que las hace más tolerantes a cientos de sustancias antimicrobianas". Los resultados de este estudio abren nuevos horizontes que se extienden más allá de los límites de la ecología microbiana. Se espera que otros estudios, que explorarán hasta qué punto la tolerancia microbiana está determinada por el metabolismo y el entorno metabólico, ayuden a desarrollar nuevas generaciones de fármacos antifúngicos.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.




















































