Desmutar el genoma
Se descifran los mecanismos epigenéticos de la activación genética específica de los padres
Las enfermedades hereditarias, así como los cánceres y las enfermedades cardiovasculares, pueden estar asociadas a un fenómeno conocido como impronta genómica, en el que sólo está activo el gen heredado de forma materna o paterna. Un equipo internacional de investigación en el que participan científicos de la Universidad Técnica de Múnich (TUM), el Instituto Max Planck de Genética Molecular (MPIMG) de Berlín y la Universidad de Harvard en Cambridge (EE UU) ha investigado ahora los mecanismos responsables de la desactivación de los genes.
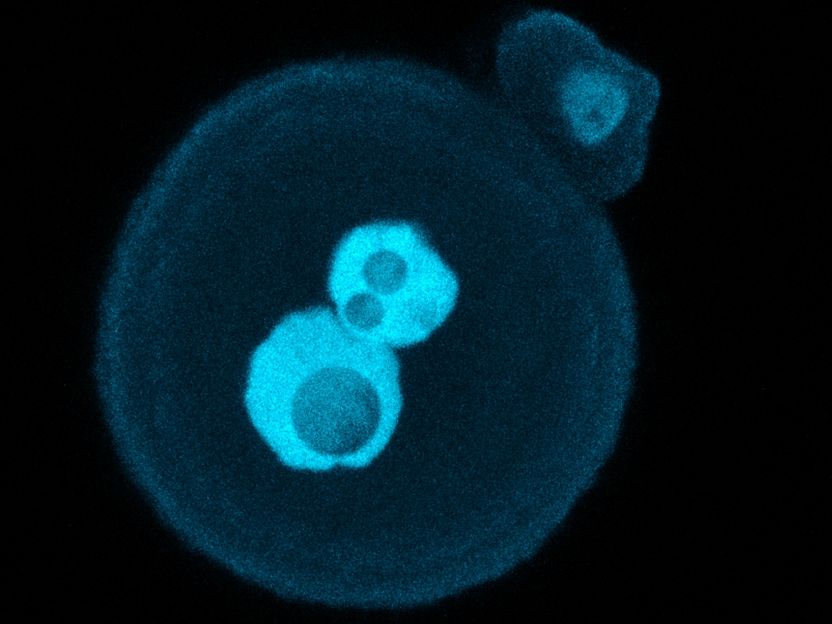
El cigoto de un ratón teñido con colorantes fluorescentes, con los núcleos de los espermatozoides y los óvulos aún visibles como manchas brillantes en el centro
A. S. Kumar MPI f. mol. Genet.
Nuestras células contienen toda la información genética de nuestra madre y nuestro padre. De cada uno de ellos heredamos 23 cromosomas que contienen nuestro ADN. Por tanto, en nuestro genoma hay dos copias de cada gen y, por regla general, ambas están activas. Esto tiene la ventaja de que las mutaciones defectuosas heredadas de la madre o el padre suelen ser anuladas por la otra copia del gen.
Sin embargo, para alrededor del uno por ciento de nuestros genes, sólo el gen heredado del padre o de la madre está activo, mientras que el otro está desactivado, un fenómeno conocido como impronta genómica.
Enfoque para el tratamiento de enfermedades
"Muchas enfermedades genéticas y epigenéticas están asociadas a la impronta genómica, como el síndrome de Beckwith-Wiedemann, el síndrome de Angelman y el síndrome de Prader-Willi", explica Daniel Andergassen, jefe del Grupo de Investigación Junior Independiente del Instituto de Farmacología y Toxicología de la TUM. "Si se pudiera reactivar el gen sano y desactivado, sería teóricamente posible compensar las complicaciones causadas por el gen activo y defectuoso".
"Pero antes de desarrollar futuros tratamientos, tenemos que entender los fundamentos", dice Alexander Meissner, director del MPIMG. "En los últimos años ha quedado claro que la impronta genómica está mediada por múltiples mecanismos moleculares".
Leer el bloqueo del gen
En la impronta genómica, se modifica químicamente el "embalaje" del material genético o el propio ADN. En lugar de cambiar la información genética, las modificaciones bloquean la lectura del gen.
"Son los llamados mecanismos epigenéticos", dice Andergassen. "El ADN puede verse como el hardware, y la epigenética como el software responsable de regular los genes". La regulación genética tiene lugar en todas las células del cuerpo. Todas las células contienen la misma información genética, pero según el órgano, se activan distintos genes.
Las tijeras genéticas eliminan el "interruptor de apagado"
Meissner y Andergassen, que al principio del estudio aún realizaban la investigación en la Universidad de Harvard (EE.UU.) junto con Zachary Smith, utilizaron ratones para investigar qué mecanismos epigenéticos estaban detrás de la impronta.
Utilizaron la técnica de biología molecular conocida como CRISPR-Cas9, que funciona como una "tijera genética", quitando e insertando segmentos de ADN. Los científicos eliminaron "interruptores de apagado" epigenéticos conocidos y observaron si el gen desactivado se reactivaba. Con este enfoque, pudieron vincular los "interruptores de desconexión" epigenéticos más importantes con los genes impresos.
Las moléculas de hidrocarburos desactivan los genes
Resulta que la mayoría de los genes se inactivan mediante la metilación del ADN, que une moléculas de hidrocarburos al material genético. Otro grupo de genes es silenciado por un conjunto de enzimas conocidas como policombas. En la placenta, entra en juego un mecanismo adicional: En este tejido, algunos genes se desactivan modificando químicamente las proteínas que sirven de andamiaje estructural al ADN.
La pequeña pero crucial diferencia
Además de la impronta genómica que desactiva genes individuales, los investigadores estudiaron otro fenómeno. En las células femeninas, que a diferencia de las masculinas tienen dos cromosomas X, un cromosoma se desactiva por completo muy pronto en el desarrollo embrionario. Esto ocurre en casi todos los mamíferos, incluidos los humanos.
"Descubrimos que la enzima PRC2 desempeña un papel importante en la inactivación del cromosoma X, al menos en la placenta", dice Andergassen. "Una vez que eliminamos esta enzima, el cromosoma X silencioso se reactiva". Los resultados podrían ser importantes para las enfermedades relacionadas con el cromosoma X, ya que la reactivación del gen silencioso podría compensar el mal funcionamiento del gen activo.
En un proyecto de seguimiento en la TUM, Andergassen estudiará si las enfermedades cardíacas también podrían estar relacionadas con la epigenética y, especialmente, con el cromosoma X inactivo en las mujeres. "Como nuestra epigenética cambia a medida que envejecemos, es concebible que el cromosoma X vuelva a activarse y que la actividad genética duplicada influya negativamente", dice el investigador.
Con su investigación, el equipo ha conseguido ofrecer una visión general de los mecanismos epigenéticos que mantienen la impronta genómica. "Podemos explicar prácticamente toda la expresión génica específica de los padres con los tres mecanismos epigenéticos conocidos", dice Andergassen. "Sin embargo, sabemos relativamente poco sobre la expresión en la placenta y si es similar en todos los mamíferos. Serán necesarios más estudios para investigar cómo influyen estos procesos en el desarrollo del feto."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.