El desarrollo embrionario en una placa de Petri
La técnica de cultivo de células en 3D podría reemplazar a los embriones de ratón
Al cultivar células madre de ratón en un gel especial, un equipo de investigación de Berlín logró hacer crecer estructuras similares a las partes de un embrión. Las estructuras similares al tronco desarrollan los precursores de los tejidos neurales, óseos, cartílagos y musculares de los grupos celulares en cinco días. Esto podría permitir la investigación de los efectos de los agentes farmacológicos de manera más eficaz en el futuro, y a una escala que no sería posible en los organismos vivos.
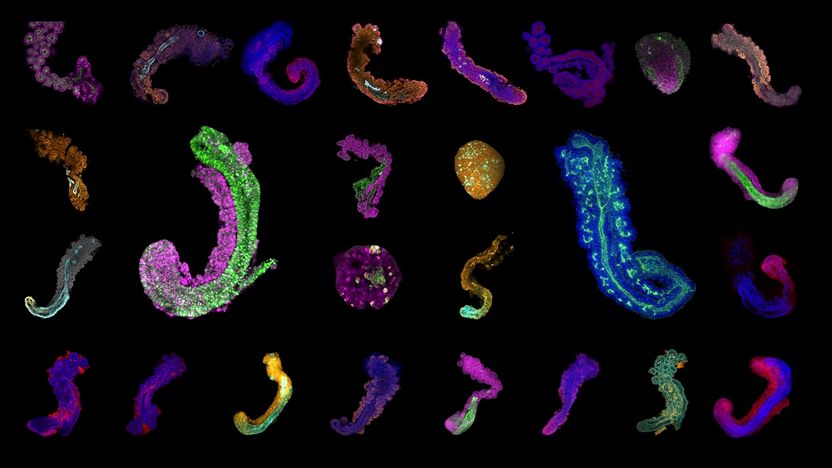
Collage de imágenes microscópicas fluorescentes de estructuras similares a un tronco generadas a partir de células madre en varias etapas de su desarrollo en un plato. Las estructuras parecidas a un tronco han sido teñidas para la expresión de diferentes genes clave del desarrollo (colores). Algunas han sido tratadas con fármacos que se dirigen a importantes vías de desarrollo, lo que conduce a defectos en el tubo neural y a la sobreproducción de somitas dispuestas como un racimo de uvas (por ejemplo, arriba a la izquierda).
© Dennis Schifferl, Adriano Bolondi, Polly Burton, Jesse Veenvliet - MPI f. Mol. Genet.
Ciertamente, evitaría a las madres las dificultades del embarazo, pero los mamíferos no crecen en los huevos. En cierto modo, esto también es poco práctico para la ciencia. Mientras que los embriones de peces, anfibios o aves pueden ser fácilmente observados en crecimiento, el desarrollo de los mamíferos evade la mirada del observador tan pronto como el embrión se implanta en el útero. Es precisamente el momento en que el embrión experimenta profundos cambios de forma y desarrolla precursores de varios órganos, un proceso muy complejo que deja muchas preguntas sin respuesta.
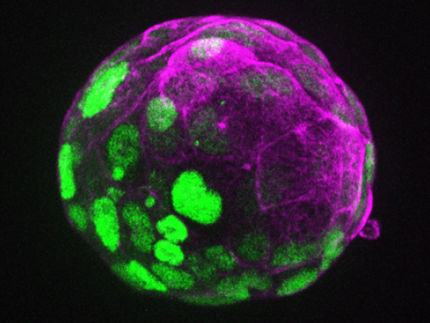
Pero ahora un equipo de investigación del Instituto Max Planck de Genética Molecular de Berlín logró replicar una fase central del desarrollo embrionario en un enfoque de cultivo celular, haciendo crecer por primera vez la porción central del tronco a partir de células madre embrionarias de ratones. El método recapitula los primeros procesos de generación de forma del desarrollo embrionario en la placa de Petri.
Las estructuras tienen un tamaño aproximado de un milímetro y poseen un tubo neural a partir del cual se desarrollaría la médula espinal. Además, tienen somitas, que son los precursores del esqueleto, el cartílago y el músculo. Algunas de las estructuras incluso desarrollan los precursores de órganos internos como el intestino. Después de unos cinco días, los paralelismos con el desarrollo normal terminan.
"Este modelo de desarrollo embrionario inicia una nueva era", dice Bernhard G. Herrmann, Director del Instituto Max Planck de Genética Molecular y Director del Instituto de Genética Médica de la Charité - Universitätsmedizin de Berlín. "Esto nos permite observar la embriogénesis del ratón directamente, de forma continua, y con un gran número de muestras paralelas - lo que no sería posible en el animal."
Se considera bastante fácil aislar los embriones tempranos del tubo o del útero y hacerlos crecer en la placa de Petri, siempre y cuando todavía estén libres para moverse. Pero una vez que el embrión se ha implantado en el endometrio, el aislamiento se hace extremadamente difícil. "Podemos obtener resultados más detallados más rápidamente, y sin necesidad de investigación con animales", dice Alexander Meissner, quien como Herrmann es Director del Instituto Max Planck de Genética Molecular y supervisó conjuntamente el estudio. "De los procesos más complejos como la morfogénesis, normalmente sólo obtenemos instantáneas - pero esto cambia con nuestro modelo."
Un gel proporciona apoyo y orientación espacial
Hasta ahora, sólo ha sido posible cultivar grupos de células a partir de células madre embrionarias, los llamados gastruloides. "Los ensamblajes celulares en los gastruloides se desarrollan en una medida similar a la de nuestras estructuras troncales, pero no asumen la apariencia típica de un embrión", dice Jesse Veenvliet, uno de los dos autores principales del estudio. "Los grupos de células carecen de las señales que desencadenan su organización en un arreglo significativo".
En el cultivo celular, la señal requerida es generada por un gel especial que imita las propiedades de la matriz extracelular. Esta sustancia gelatinosa consiste en una compleja mezcla de moléculas de proteína extendidas que es secretada por las células y se encuentra en todo el cuerpo como un material de relleno elástico, especialmente en los tejidos conectivos. La utilización de este gel es el "truco" crucial del nuevo método. "El gel proporciona apoyo a las células cultivadas y las orienta en el espacio; pueden distinguir el interior del exterior, por ejemplo", dice Veenvliet. También evita que las moléculas secretas como la proteína matriz fibronectina se filtren en el medio de cultivo celular. "Las células son capaces de establecer una mejor comunicación, lo que conduce a una mejor auto-organización".
Células con propiedades similares a las del embrión
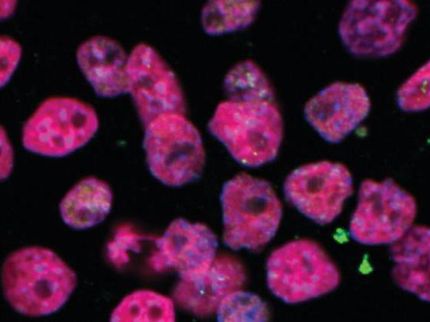
Después de cuatro o cinco días, el equipo disolvió las estructuras en células individuales y las analizó individualmente. "Aunque no todos los tipos de células están presentes en las estructuras del tronco, son sorprendentemente similares a un embrión de la misma edad", dice Adriano Bolondi, que también es el autor principal del trabajo. Junto con la bioinformática Helene Kretzmer, Bolondi y Veenvliet compararon la actividad genética de las estructuras con los embriones de ratón reales. "Encontramos que todos los genes marcadores esenciales se activaron en el momento adecuado en los lugares adecuados de los embriones, y que sólo un pequeño número de genes estaban fuera de línea", dice Bolondi.
Los investigadores introdujeron una mutación con efectos conocidos en el desarrollo en su modelo y pudieron recrear los resultados de embriones "reales", validando aún más su modelo. También proporcionan ejemplos de manipulación del proceso de desarrollo con agentes químicos.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.