Degradadores moleculares de pegamento - una nueva arma para apuntar a los conductores de cáncer "no drogables".
Una estrategia para luchar contra el cáncer es apuntar a su talón de Aquiles, la adicción a las proteínas promotoras del crecimiento. Sin embargo, como muchos de estos llamados impulsores del cáncer son notoriamente difíciles de bloquear con una droga, esto requiere enfoques novedosos y no convencionales. En cooperación con el Centro Alemán de Investigación del Cáncer (DKFZ) y el Centro Nacional de Enfermedades Tumorales (NCT) de Heidelberg, investigadores de Boston y Basilea han dilucidado el mecanismo de acción de una de estas drogas no convencionales. Este "degradador de pegamento molecular" se une a una cinasa dependiente de ciclinas e induce su interacción con el sistema de eliminación de desechos de la célula, lo que a su vez resulta en la degradación de un impulsor de cáncer y la subsiguiente inhibición del crecimiento. Los hallazgos de los científicos abren nuevos caminos en el desarrollo de drogas.
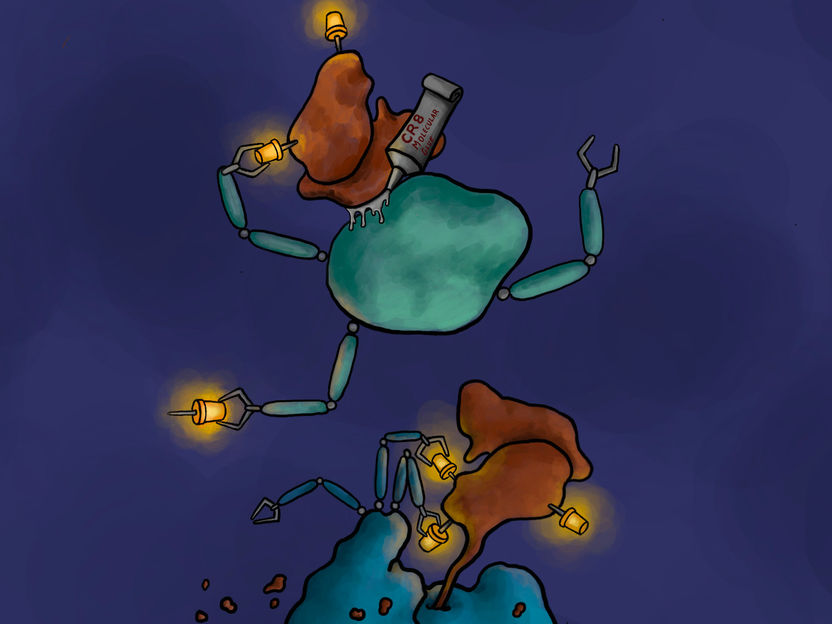
Cómo funciona un degradador de pegamento molecular. El inhibidor de cinasa CR8 une el complejo CDK12/ciclina K que produce cáncer (marrón) a una ligasa E3 (verde). Esta interacción hace que la ciclina K se una a las moléculas de ubiquitina (amarillo). Las moléculas de la ciclina K así etiquetadas pueden ser reconocidas y descompuestas por el sistema de eliminación de residuos de la célula (azul).
Copyright: Jonas Koeppel
La mayoría de los medicamentos contra el cáncer que se utilizan actualmente en la clínica son inhibidores, pequeñas moléculas que funcionan uniéndose y bloqueando la actividad de las enzimas. Sin embargo, sólo una fracción de las proteínas críticas para el crecimiento del cáncer tienen una bolsa adecuada para la inhibición. Un enfoque novedoso para atacar estos factores de cáncer "no farmacológicos" consiste en secuestrar la maquinaria molecular diseñada para eliminar las proteínas aberrantes de la célula mediante su degradación.
Un componente vital del sistema de eliminación de desechos de la célula son las ligasas E3, enzimas que regulan la abundancia y, por lo tanto, la actividad de muchas proteínas. En los últimos años se han descrito medicamentos que secuestran ligasas E3 para destruir y eliminar selectivamente las proteínas causantes de enfermedades. El ejemplo más conocido es la talidomida, que actúa como un "pegamento molecular" que induce la proximidad entre un factor de transcripción llamado Ikaros y un receptor de sustrato de ligasa E3. Al "pegar" estas dos proteínas entre sí, el Ikaros está etiquetado con ubiquitina y por lo tanto es objeto de degradación. Un análogo de la talidomida llamado lenalidomida ha sido aprobado en Alemania para el tratamiento de ciertos cánceres de la sangre, a saber, el mieloma múltiple y el síndrome mielodisplásico.
"Para identificar nuevos pegamentos moleculares, investigamos miles de fármacos por su capacidad de inhibir las células cancerosas en relación con los niveles de expresión de las ligasas E3", informa Mikołaj Słabicki, investigador postdoctoral del Instituto de Cáncer Dana-Farber (DFCI) de Boston y de la División de Oncología Médica Traslacional del DKFZ y el NCT de Heidelberg y primer coautor del estudio. "Descubrimos que el inhibidor de la cinasa CR8 inhibe el crecimiento de las células cancerosas al reclutar una ligasa E3 al complejo CDK12/ciclina K que promueve el crecimiento, lo que resulta en una rápida degradación de la ciclina K".
Tras una caracterización más detallada del CR8, los investigadores encontraron una similitud estructural con un conocido inhibidor de la cinasa llamado roscovitina o seliciclib. "Hemos demostrado que es posible tomar un inhibidor de cinasa convencional y, al unir un grupo químico en particular, transformarlo en un degradador molecular de pegamento", dijo el coautor principal Benjamin Ebert, Presidente del Departamento de Oncología Médica de la DFCI y ganador del Premio Meyenburg de Investigación sobre el Cáncer 2019. Los detalles moleculares del complejo de pegamento molecular inducido por el CR8 fueron revelados por investigadores del Instituto Friedrich Miescher de Investigación Biomédica (FMI) en Basilea, incluyendo al co-autor principal Nicolas Thomä y a los co-autores principales Zuzanna Kozicka y Georg Petzold. Los equipos de ambos lados del Atlántico llegaron a la conclusión de que se necesita una pequeña fracción química para que el CR8 actúe como degradador de pegamento molecular. "Esta podría ser una estrategia más generalizable para el diseño de drogas y dar lugar a nuevas opciones para el tratamiento del cáncer", dice Kozicka.
La búsqueda de nuevos degradadores de pegamento molecular fue un esfuerzo conjunto de científicos del DFCI, el Instituto Broad de Harvard y el Instituto Tecnológico de Massachusetts en Cambridge, y el FMI en colaboración con investigadores del DKFZ y el NCT de Heidelberg, incluidos dos importantes estudiantes de biología del cáncer, Manisha Manojkumar y Jonas Koeppel.
"Este estudio fue un verdadero trabajo detectivesco, con cada experimento descubriendo piezas adicionales del rompecabezas. Exigió un esfuerzo multidisciplinario por parte de los miembros del equipo de varios campos, entre ellos la biología del cáncer, la bioinformática, la genómica funcional, la biología estructural y la bioquímica, y fue una experiencia increíblemente emocionante y gratificante", dice Słabicki.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.





















































