Warum kann EHEC lebensbedrohlich sein?
Einzigartige Kombination molekularer Eigenschaften macht den Erreger so gefährlich
Bis heute ist noch immer ungeklärt, was den EHEC-Ausbruchstamm O104:H4, der im Jahr 2011 Deutschland in Angst und Schrecken versetzte, so gefährlich machte. Wissenschaftlerinnen um die Professorin Dr. Regine Hengge von der Humboldt-Universität zu Berlin (HU) berichten nun in der Fachzeitschrift "EMBO Molecular Medicine" von einer speziellen, bisher einzigartigen Kombination von molekularen Eigenschaften des EHEC-Ausbruchsstamms, die eine Erklärung bietet, weshalb dieser Erreger so häufig des lebensdrohliche hämolytisch-urämische Syndrom (HUS) auslösen kann.
Im Jahr 2011 erkrankten in Deutschland in kürzester Zeit fast 4000 Menschen an einer Infektion mit Bakterien vom Typ Escherichia coli EHEC O104:H4. 22 Prozent der Patienten entwickelten das wegen Nierenversagens lebensbedrohliche hämolytisch-urämische Syndrom (HUS) und 53 Patienten verstarben – ein umfangreicherer EHEC-Ausbruch mit höherer HUS-Rate als jemals zuvor beobachtet wurde. Es gelang damals Wissenschaftlern, innerhalb weniger Tage die Genomsequenz des Erregers zu entschlüsseln. Diese zeigte, dass dieser Ausbruchstamm kein klassischer EHEC (entero-hämorrhagischer E. coli), sondern genetisch ein entero-aggregativer E. coli (EAEC) war, der allerdings das für EHEC typische Shiga-Toxin produzierte. Derartige 'Kombi-Stämme' waren bereits früher vereinzelt isoliert und analysiert worden – keiner jedoch hatte diese verheerende Virulenz gezeigt, deren Ursache auch in einer Vielzahl von Folgestudien bis heute nicht überzeugend geklärt werden konnte.
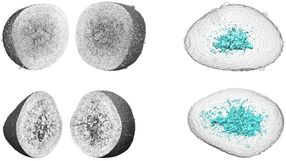
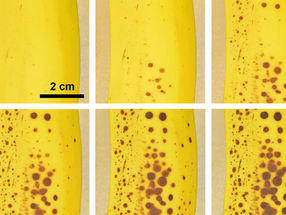
Wissenschaftlerinnen um die Professorin Dr. Regine Hengge von der Humboldt-Universität zu Berlin (HU) in Zusammenarbeit mit Professor Dr. Lothar Wieler von der Freien Universität Berlin (FU) haben nun in der Fachzeitschrift "EMBO Molecular Medicine" eine Arbeit publiziert, die eine Erklärung bietet, weshalb der Erreger so häufig des lebensbedrohliche hämolytisch-urämische Syndroms auslösen kann. Insgesamt zeigt der Ausbruchstamm eine bisher einzigartige Kombination von Eigenschaften, die zu einem fatalen Szenario führen können: Der Erreger bildet ein zusätzliches, nur in speziellen E. coli-Varianten vom Typ EAEC vorkommendes Enzym in extrem großen Mengen, welches das Signalmolekül cyclic-di-GMP produziert. Dieses Signalmolekül löst in E. coli-Bakterien die Produktion von sogenannten amyloiden Curli-Fasern aus, die sich in einer klebrigen Netzwerkstruktur um die Bakterien herum lagern. Strukturell ist dieses Netzwerk mit den Plaques verwandt, die bei der Alzheimer-Krankheit im menschlichen Hirn auftreten. In unserem Darm löst dieses bakterielle Curli-Fasergeflecht eine starke Entzündung aus. Diese Wirkung ist ausgerechnet beim Ausbruchstamm besonders ausgeprägt, da dieser aufgrund einer einzigartigen Mutation keine Zellulose produzieren kann, die bei anderen E. coli-Varianten die entzündliche Wirkung der Curli-Fasern abschwächt. Eine starke Entzündungsreaktion im Darm fördert nun aber den Übertritt des vom Ausbruchstamm gleichzeitig produzierten Shiga-Toxins in die Blutbahn, sodass dieses Toxin die Nieren erreichen und dort das hämolytisch-urämische Syndrom auslösen kann.
Da die Synthese des gefährlichen Shiga-Toxins durch bestimmte Antibiotika weiter verstärkt wird, ist eine Antibiotika-Behandlung von Infektionen mit dem Ausbruchstamm oder verwandten EHEC-Bakterien problematisch. Es bleibt Ärzten daher oft nichts anderes übrig, als in der Behandlung den Immunstatus des Patienten zu unterstützen. Die neue Studie weist auch darauf hin, dass möglicherweise eine gezielte Unterdrückung spezieller Eigenschaften des Erregers, wie z.B. die Bildung seiner amyloiden Curli-Fasern, in der Behandlung von zukünftigen Infektionen mit ähnlichen Keimen sinnvoll sein könnte.