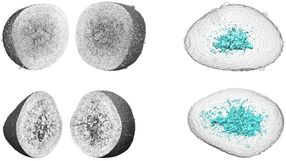
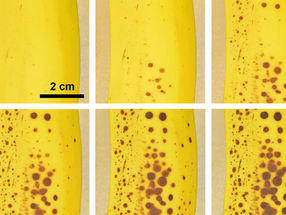
Immunzellen in der Leber verursachen Fettleber und Leberkrebs
Immunzellen, die in die Leber einwandern und dort mit Zellen des Lebergewebes interagieren, können Fettleber, nicht-alkoholische Steatohepatitis und Leberkrebs auslösen. Dies haben Wissenschaftler des Helmholtz Zentrums München herausgefunden und damit einen bislang unbekannten Entstehungsmechanismus dieser schweren und weit verbreiteten Erkrankungen identifiziert. Die Ergebnisse sind im Fachjournal ‚Cancer Cell‘ als Cover-Story publiziert.
Eine Verfettung der Leber entsteht – neben der durch massiven Alkoholkonsum verursachten Fettleber - vor allem durch übermäßigen Konsum von Fett und Zucker in Kombination mit geringer Bewegung. Man spricht dann von der nicht-alkoholischen Fettleber (NAFLD). Kommt eine chronische entzündliche Gewebsreaktion hinzu, kann eine nicht-alkoholische Steatohepatitis (NASH) entstehen. Diese Lebererkrankungen sind neben chronischen Virusinfektionen die häufigste Ursache von Leberkrebs (Hepatozelluläres Carcinom, HCC). In den USA leiden etwa 90 Millionen Menschen an einer Fettleber, in Europa sind es mehr als 40 Millionen und auch in Schwellenländern (z.B. Indien und China) steigt die Zahl der Betroffenen aufgrund eines zunehmend ungesunden Lebensstils. Auch das aus NASH und NAFLD resultierende HCC nimmt weltweit zu – in den USA ist das HCC die am schnellsten wachsende Krebserkrankung. Eine effiziente kausale Therapie für diese Patienten existiert nicht.
T-Zellen an der Entstehung von Fettleber, NASH und HCC beteiligt
Die Mechanismen, wie Fettleber, Steatohepatitis und HCC entstehen, sind weitgehend noch unverstanden. Immunzellen, insbesondere CD8+ T-Zellen und NK T-Zellen, scheinen dabei aber eine wichtige Rolle zu spielen. Dies hat das Wissenschaftlerteam um Prof. Dr. Mathias Heikenwälder, Prof. Dr. Matthias Tschöp, Dr. Kerstin Stemmer, Dr. Kristian Unger und Prof. Dr. Ulrike Protzer vom Helmholtz Zentrum München gemeinsam mit einem Team um Prof. Dr. Percy Knolle an der Technischen Universität München und Prof. Dr. Achim Weber vom Universitätsspital Zürich und Dr. Monika Wolf , Klinische Pathologie Universitätsspital Zürich herausgefunden. Im Tiermodell, mit dem die langfristigen Auswirkungen des metabolischen Sydroms untersucht werden, konnten die Wissenschaftler neuartige Mechanismen aufklären, die zu Fettleber und NASH führen und auch zeigen, wie daraus Leberkrebs entsteht.
Entzündungsgeschehen bietet Ansatzpunkte für Prävention und Therapie
Die Wissenschaftler gehen davon aus, dass das vorliegende metabolische Ungleichgewicht dazu führt, dass Immunzellen aktiviert werden und in die Leber einwandern. Dort interagieren die Immunzellen mit den Leberzellen und lösen einen gewebeschädlichen Entzündungsprozess sowie eine Destabilisierung der metabolischen Aktivität der Leberzellen aus. „Zunächst kommt es zu einer Verfettung der Leber. Die Entzündung fördert mit spezifischen Immunzellen das Voranschreiten der Fettleber und führt zur Entstehung von NASH. Diese Prozesse sind die Grundlage für eine Entartung von Leberzellen, die zum HCC führen kann“, erklärt Studienleiter Heikenwälder. „Unsere Ergebnisse liefern einen völlig neuen Einblick in die Entstehung dieser schweren Lebererkrankungen. Darauf aufbauend wollen wir nun neue präventive bzw. therapeutische Strategien gegen die Krankheiten entwickeln.“ Erste Studien im präklinischen Modell laufen bereits.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Ab sofort nichts mehr verpassen: Unser Newsletter für Biotechnologie, Pharma und Life Sciences bringt Sie jeden Dienstag und Donnerstag auf den neuesten Stand. Aktuelle Branchen-News, Produkt-Highlights und Innovationen - kompakt und verständlich in Ihrem Posteingang. Von uns recherchiert, damit Sie es nicht tun müssen.