Spinnenbiss führt zu neuen Wirkstoffen
Internationales Forscherteam geht Infektionsursache auf den Grund
Der Biss einer Spinne verursachte eine schwere Entzündung und kostete einer Australierin den Unterarm. Doch diese tragisch verlaufende Infektion führte ein internationales Forscherteam zu neuen Wirkstoffen, den sogenannten Necroximen. Die Substanzen werden von Bakterien gebildet, die im Inneren von Pilzen leben. Wissenschaftler isolierten sie aus dem infizierten Unterarmgewebe der Patientin. Die hochwirksamen Zellgifte können Anhaltspunkte für die Entwicklung neuer Krebsmedikamente liefern.
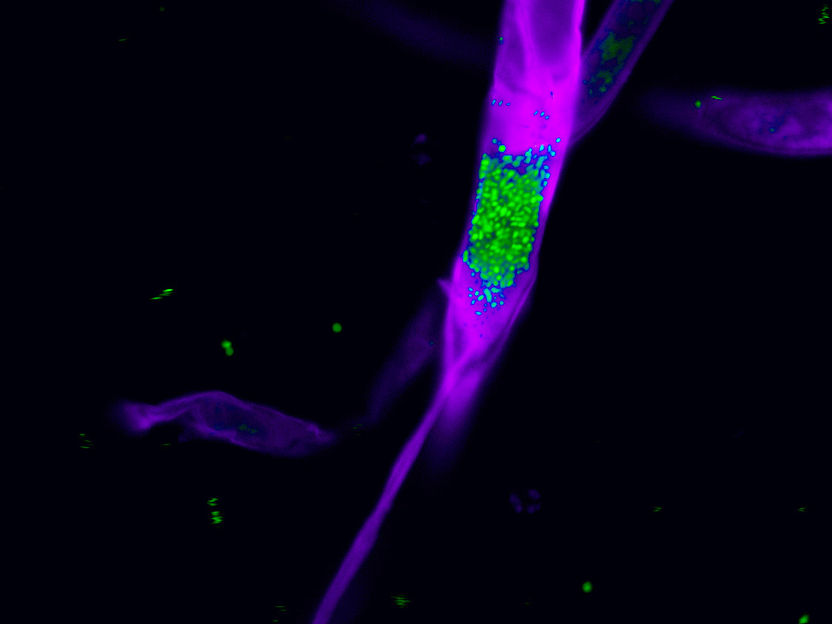
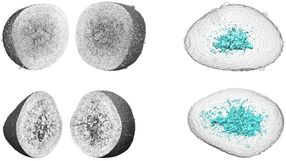
Mikroskopische Visualisierung der Bakterien im Pilz
Leibniz-HKI
Zahlreiche Wildtiere Australiens sind besonders giftig, darunter auch viele Spinnen. Ein Team um Christian Hertweck vom Leibniz-Institut für Naturstoff-Forschung und Infektionsbiologie – Hans-Knöll-Institut – (Leibniz-HKI) in Jena ist gemeinsam mit australischen Kollegen einem ungewöhnlichen Fall auf den Grund gegangen: In den 1980er Jahren biss eine Spinne einer Australierin in den Finger. Es entwickelte sich eine Mischinfektion im Unterarm, die Mediziner nur durch eine Amputation stoppen konnten. Aus dem abgestorbenen – nekrotischen – Gewebe isolierten Forscherkollegen damals den Pilz Rhizopus microsporus. Hertweck und seine Mitarbeiter entdeckten, dass im Zellinneren dieses Pilzes wiederum Bakterien leben. Sie sind es, die nach den Analysen der Jenaer Forscher einen ganzen Giftcocktail produzieren. Ein Teil dieses Gemischs, die sogenannten Rhizoxine, wurde bereits vor einigen Jahren am Leibniz-HKI entdeckt. Nun sind neue Moleküle mit völlig anderer Struktur hinzugekommen, die als Necroxime bezeichnet werden. Sie gehören zur Substanzklasse der Benzolacton-Enamide. Schon geringste Mengen dieser Necroxime bringen menschliche Zellen zum Absterben.
Das Team untersuchte auch, wie die Bakterien diese ungewöhnlichen Verbindungen herstellen. Dazu analysierten die Forscher das Genom der Bakterien. Durch bioinformatische Analysen entschlüsselten sie eine Vielzahl von Biosynthese-Genen. Sie codieren eine Art molekulares Fließband, an dem die Necroxime gebildet werden. Kleine Molekülbausteine werden über ein biochemisches Programm zusammengesetzt und modifiziert. Jede einzelne Domäne des enzymatischen Fließbands ist für einen speziellen Reaktionsschritt zuständig, bis schließlich das fertige Molekül freigesetzt wird. Da Necroxime und verwandte Stoffe toxisch auf menschliche Zellen wirken, kommen sie als Medikamente gegen Krebserkrankungen in Betracht. Chemiker müssen jedoch häufig die Molekülstruktur noch anpassen, um die pharmakologischen Eigenschaften zu verbessern und unerwünschte Wirkungen zu minimieren. Die Enzyme der Biosynthese sind für die Wissenschaftler ein geeignetes, von der Natur bereitgestelltes Werkzeug. Durch die Decodierung der zuständigen Gene ist es den Naturstoff-Forschern nun möglich, die Biosynthese von Wirkstoffen gezielt umzuprogrammieren. Zudem fanden sie ähnliche genetische Codes in den Genomen zahlreicher anderer Bakterien, die sie auf diese Weise als Wirkstoffproduzenten identifizierten.
Für Christian Hertweck, der auch einen Lehrstuhl an der Friedrich-Schiller-Universität Jena innehat, sind natürliche Lebenspartnerschaften eine Quelle der wissenschaftlichen Inspiration: „Das komplexe Zusammenleben unterschiedlicher Organismen – hier Bakterium, Pilz und Spinne – wird größtenteils von chemischen Substanzen gesteuert. Mit den Necroximen haben wir neue toxische Naturstoffe entdeckt, die möglicherweise auch nutzbringend für den Menschen zum Einsatz kommen könnten.“ Die Jenaer Forscher verfolgen diesen Ansatz in einem eigenen Forschungsschwerpunkt. So widmen sich Hertweck und viele Kollegen im Sonderforschungsbereich ChemBioSys der chemischen Sprache in Organismengemeinschaften. Auch im Exzellenzcluster Balance of the Microverse gehen die Wissenschaftler dem molekularen Zusammenspiel von Mikroorganismen mit anderen Lebewesen und der Umwelt nach. Solche Erkenntnisse sind von medizinischem Interesse, können aber auch beitragen, Umweltprozesse zu verstehen und zu beeinflussen.