Les nanoparticules d'intérêt médical se déplacent plus rapidement que prévu dans les cellules
Cette découverte a des implications importantes pour les applications en nanomédecine, telles que l'administration ciblée de médicaments et les études intracellulaires
Annonces
Une expérience menée par une équipe de scientifiques de DESY et de l'Universität Hamburg a permis de découvrir que les nanoparticules d'or peuvent se déplacer dans la matière biologique liquide plus rapidement que prévu lorsqu'elles sont recouvertes du polymère polyéthylène glycol (PEG). Les données de l'équipe, qui ont été acquises par spectroscopie de corrélation de photons X, révèlent à la fois la structure et la dynamique des nanoparticules dans divers fluides biologiques avec une haute résolution temporelle. La recherche a été publiée dans la revue Aggregate.
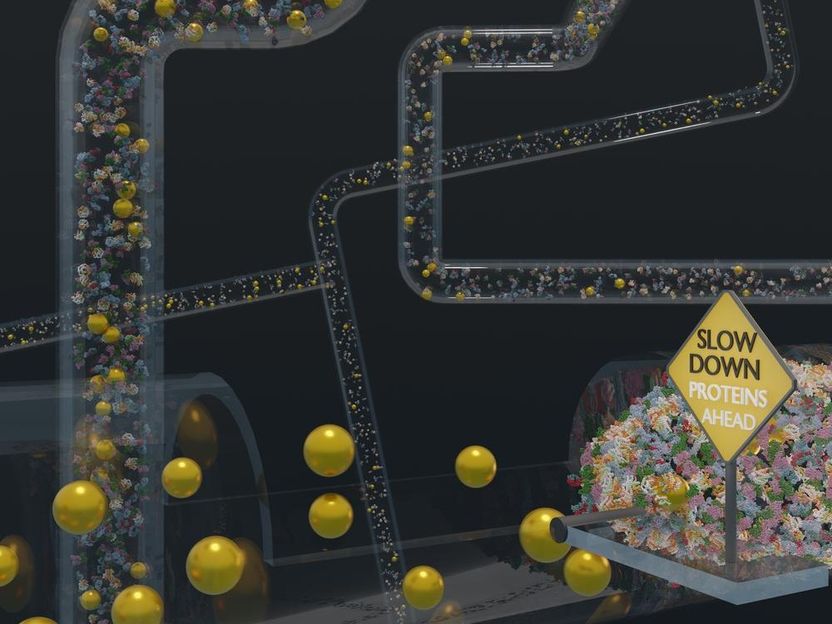
Pour illustrer le type d'environnement dans lequel les nanoparticules d'or peuvent être utilisées, les nanoparticules s'approchent des régions densément peuplées de protéines. Les chercheurs à l'origine de cette étude ont constaté que les nanoparticules, lorsqu'elles sont recouvertes du polymère PEG, se déplacent rapidement dans ces environnements denses.
Ferdinand Otto, UHH
Dans le domaine en pleine expansion de la nanomédecine, les nanoparticules d'or sont devenues un outil prometteur. Les nanoparticules sont de minuscules cristaux d'or entourés de molécules organiques, appelées ligands. Le revêtement des nanoparticules d'or par ces ligands peut être contrôlé avec précision. En outre, l'or n'est pas toxique et les nanoparticules d'or possèdent des propriétés physiques utiles telles qu'une forte absorption et diffusion de la lumière visible et des rayons X. Cela rend les nanoparticules d'or très intéressantes pour les chercheurs. Les nanoparticules d'or sont donc très utiles pour les applications médicales. Elles ont été largement utilisées lors de la pandémie de COVID-19 en tant qu'ingrédient clé des cartouches d'autotest utilisées dans le monde entier. Elles présentent également un fort potentiel pour l'administration ciblée de médicaments, comme agents de contraste pour la tomographie assistée par ordinateur et pour les approches thérapeutiques hyperthermiques, entre autres. Par exemple, pour le traitement du cancer, elles peuvent être injectées dans le site d'une tumeur, puis surchauffées par un laser afin de tuer les cellules cancéreuses de l'intérieur.
De nombreuses nanoparticules approuvées pour des applications médicales, y compris les nanoparticules lipidiques utilisées pour la plupart des vaccins COVID, sont recouvertes de PEG afin d'améliorer leur stabilité, leur solubilité et leur distribution dans le corps. Il est donc extrêmement important de comprendre comment la dynamique des particules dans les fluides biologiques est affectée par ce polymère. En raison de leur taille minuscule, les nanoparticules peuvent même pénétrer dans les cellules cibles, généralement une fois qu'elles sont entourées d'un amas de protéines, qui sont présentes en fortes concentrations dans le sang et à des densités encore plus élevées à l'intérieur des cellules. L'amas de protéines ne modifie pas seulement les propriétés des nanoparticules de sorte qu'elles risquent de ne plus atteindre leur cible, mais il peut également déclencher une réponse immunitaire indésirable. Les revêtements en PEG peuvent fortement réduire cette adsorption indésirable de protéines, et les scientifiques parlent souvent d'un effet "furtif" fourni par le revêtement en PEG.
Dans son étude, l'équipe a utilisé des nanoparticules d'or avec des revêtements PEG sur mesure et a étudié leur dynamique en présence de concentrations variables de protéines. Ils ont ainsi pu imiter les différents environnements que les nanoparticules rencontrent dans l'organisme : de la circulation sanguine à l'intérieur des cellules avec des concentrations de protéines extrêmement élevées.
"Plus vous mettez de molécules dans le fluide, plus il est dense sur le plan moléculaire, plus vous vous rapprochez de ce que l'on appelle l'encombrement des protéines, qui est ce qui se passe dans le corps", explique Felix Lehmkühler, un scientifique de DESY qui a codirigé les travaux de recherche. Lehmkühler compare l'encombrement des protéines à une grande fête dans une petite pièce : les participants à la fête se tiennent tous les uns près des autres, et quelqu'un - dans ce cas, la nanoparticule d'or - qui essaie de passer doit continuellement changer de direction ou est arrêté par certains des fêtards sur le chemin.
"Des expériences antérieures ont montré que ce processus d'adsorption des protéines était un effet courant. Nous voulions pousser notre expérience à l'extrême, à une concentration élevée de protéines similaire à la réalité, et tester les effets d'une enveloppe de PEG", explique Florian Schulz, post-doctorant à l'université de Hambourg, qui a codirigé l'expérience avec M. Lehmkühler. "Nous nous attendions à ce que les nanoparticules ralentissent lorsqu'elles pénètrent dans des environnements riches en protéines.
Cependant, l'équipe a trouvé quelque chose de bien différent dans ses résultats. "Lorsque nous entrons dans cette situation d'encombrement des protéines, nous constatons que la particule se déplace plus rapidement que prévu", explique M. Lehmkühler. C'est comme si la nanoparticule avait rapidement traversé la fête dans l'analogie précédente. L'équipe a utilisé la spectroscopie de corrélation des photons de rayons X pour surveiller la diffusion des nanoparticules. Ils n'ont observé aucun signe d'adsorption des protéines sur les nanoparticules lorsqu'elles se déplacent, ce qui confirme l'effet "furtif" bénéfique des enrobages PEG.
Dans les environnements protéiques très encombrés, semblables à la situation dans les cellules, les nanoparticules se diffusent beaucoup plus rapidement que ne le permet la viscosité prévue par la théorie. Plus fascinant encore, l'équipe a constaté que les viscosités des solutions biologiques riches en protéines sont exactement celles attendues lorsqu'elles sont mesurées à l'aide de méthodes classiques. Par conséquent, la viscosité locale de la nanoparticule diffère fortement de la viscosité de la matière biologique dans son ensemble, ce qui signifie que la nanoparticule a un effet important sur son environnement qui permet ce mouvement rapide. Cette découverte est extrêmement importante pour la compréhension de la dynamique des nanoparticules dans les systèmes biologiques, ce qui est essentiel pour une application sûre et réussie.
"Les changements de viscosité à l'échelle nanométrique ont été une surprise", déclare Schulz. "C'est la première fois que ce phénomène est observé. Nous avons dû vérifier, vérifier et revérifier pour nous assurer que cet effet était réel. Il s'agit d'une découverte très importante, car elle nous indique que si ces nanoparticules se diffusent si rapidement, c'est parce qu'elles affectent fortement leur environnement local."
"Cette étude souligne l'importance de ces mesures approfondies de la structure et de la dynamique pour notre compréhension des systèmes complexes", déclare Ferdinand Otto, premier auteur de la publication, "et la spectroscopie de corrélation des photons X est une excellente méthode qui commence à peine à être explorée dans ce contexte."
L'expérience a été réalisée à l'Installation européenne de rayonnement synchrotron (ESRF) de Grenoble, en France. Toutefois, ce type de recherche bénéficiera grandement de la source de lumière PETRA IV prévue à DESY. La technique utilisée dans cette recherche, la spectroscopie de corrélation de photons X, sera celle qui bénéficiera le plus de la modernisation de l'installation, car l'éclat de PETRA IV permettra d'étendre l'échelle de temps accessible à la nanoseconde, ou au milliardième de seconde.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.