Modèle neuromusculaire 2D pour la recherche de substances actives
Annonces
Dans les maladies neuromusculaires, l'interaction entre les neurones et les cellules musculaires est perturbée. Les chercheurs de l'équipe de Mina Gouti peuvent désormais la reproduire en 2D dans une boîte de culture. Cette approche est bien adaptée au criblage à haut débit dans la recherche de substances actives, écrivent-ils dans Nature Communications.
On connaît aujourd'hui environ 800 maladies neuromusculaires différentes. Ces maladies résultent d'une interaction perturbée entre les cellules musculaires, les cellules nerveuses motrices et les nerfs périphériques. Ces troubles entraînent une faiblesse musculaire, une paralysie et, dans certains cas, la mort, comme dans le cas de la sclérose latérale amyotrophique ou de l'amyotrophie spinale.
"Ces maladies sont très complexes et la cause du trouble peut se situer à des endroits très différents", explique le Dr Mina Gouti, responsable du groupe de travail Modélisation du développement et de la maladie par les cellules souches au Max Delbrück Center. Ainsi, les cellules nerveuses ou musculaires, mais aussi les connexions entre les deux types de cellules peuvent être affectées. "Pour mieux comprendre les causes et trouver des thérapies efficaces, nous avons donc besoin de systèmes de culture cellulaire humaine dans lesquels nous pouvons étudier l'interaction entre les motoneurones de la moelle épinière et les cellules musculaires".
Les organoïdes sont trop grands pour les dépistages à haut débit
Auparavant, les chercheurs autour de Gouti avaient déjà développé un système organoïde neuromusculaire tridimensionnel, les NMO. "L'un de nos objectifs est de tester des substances actives à grande échelle avec nos cultures", explique Gouti. "Les organoïdes tridimensionnels sont assez grands et ne peuvent pas être cultivés sur une longue période dans une plaque de culture à 96 trous, dans laquelle nous pouvons effectuer des criblages à haut débit avec des substances actives".
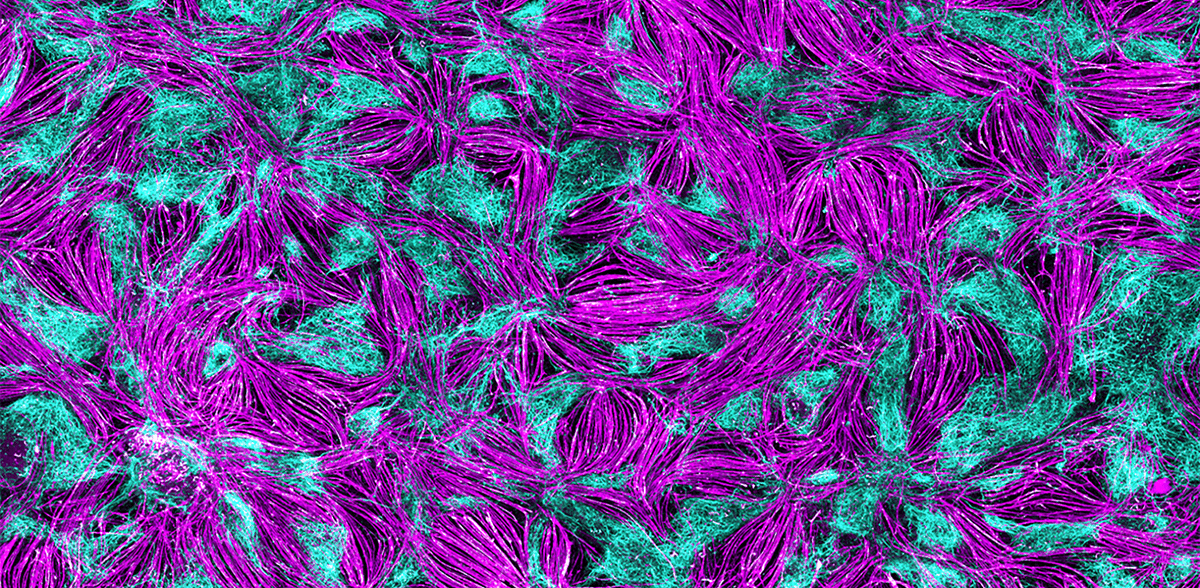
Pour ce type de criblage, une équipe internationale dirigée par Gouti a développé avec succès un système de culture cellulaire 2D auto-organisé à partir de cellules souches pluripotentes, qui contient des cellules nerveuses et des cellules musculaires, ainsi que les synapses chimiques, c'est-à-dire la connexion neuromusculaire qui permet l'interaction entre les deux types de cellules. "Grâce à ces cultures bidimensionnelles, nous pouvons dans un premier temps tester des substances actives potentielles à haut débit, puis examiner plus précisément les candidats prometteurs dans des organoïdes spécifiques aux patients", explique Gouti.
Pour établir le modèle 2D auto-organisé pour les connexions neuromusculaires, il fallait d'abord comprendre comment les motoneurones et les cellules musculaires se développent dans l'embryon. L'équipe de Mina ne fait pas elle-même de recherche sur l'embryon, mais utilise différentes lignées de cellules souches humaines qui peuvent être utilisées à des fins de recherche dans le respect de directives strictes, ainsi qu'une lignée de cellules souches plutiopotentes induites (iPSC). "Nous avons examiné différentes hypothèses. Nous avons ainsi réalisé que les types de cellules dont nous avons besoin pour les connexions neuromusculaires fonctionnelles sont issus de cellules progénitrices neuromésodermiques", explique la doctorante Alessia Urzi, première auteure de la publication. Urzi a trouvé la bonne composition de molécules de signalisation qui permettent aux cellules souches humaines de se développer en motoneurones fonctionnels et en cellules musculaires, et de tisser des liens entre les deux. "C'était très excitant d'observer pour la première fois au microscope comment les cellules musculaires se contractent", rapporte la chercheuse. "Une indication claire que nous sommes sur la bonne voie". Autre observation : les cellules différenciées s'organisent elles-mêmes en zones contenant des cellules musculaires et nerveuses, un peu comme une mosaïque.
Un interrupteur optogénétique pour les motoneurones
Les cellules musculaires développées dans la boîte de culture se contractent spontanément grâce à leur connexion avec les cellules nerveuses, mais sans rythme significatif. Cela ne suffisait pas à Urzi et Gouti. En collaboration avec des chercheurs de la Charité - médecine universitaire de Berlin, ils ont utilisé l'optogénétique pour activer les motoneurones. Stimulées par un flash lumineux, les cellules nerveuses s'enflamment, de sorte que les cellules musculaires se contractent de manière synchrone. Ils se rapprochent ainsi encore plus d'une situation physiologique dans l'organisme.
Un modèle d'atrophie musculaire spinale
Pour vérifier son modèle, Ursi a utilisé des iPSC humaines provenant de personnes atteintes d'atrophie musculaire spinale, une maladie neuromusculaire grave qui se manifeste chez les enfants au cours de leur première année de vie. Les cultures neuromusculaires obtenues à partir de ces cellules souches pluripotentes spécifiques au patient* ont révélé de graves problèmes de contraction des cellules musculaires, comme c'est le cas dans la musculature des malades.
Pour Gouti, ses cultures 2D et 3D sont des outils importants pour étudier les maladies neuromusculaires de manière plus détaillée et pour tester des concepts de traitement plus efficaces et individualisés. Dans la prochaine étape, Gouti et son équipe veulent effectuer des dépistages à haut débit afin de trouver de nouvelles possibilités de traitement pour les personnes atteintes d'amyotrophie spinale et de sclérose latérale amyotrophique. "Nous voulons d'abord vérifier, pour les substances actives déjà autorisées, si nous pouvons obtenir de meilleurs résultats thérapeutiques pour les personnes atteintes de maladies neuromusculaires complexes avec de nouvelles combinaisons de substances actives", explique Gouti.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Allemand peut être trouvé ici.
Publication originale
Alessia Urzi, Ines Lahmann, Lan Vi N. Nguyen, Benjamin R. Rost, Angélica García-Pérez, Noemie Lelievre, Megan E. Merritt-Garza, Han C. Phan, Gary J. Bassell, Wilfried Rossoll, Sebastian Diecke, Severine Kunz, Dietmar Schmitz, Mina Gouti; "Efficient generation of a self-organizing neuromuscular junction model from human pluripotent stem cells"; Nature Communications, Volume 14, 2023-12-19