Modèle d'infection issu de l'imprimante 3D
Des chercheurs impriment des biofilms bactériens sur des cellules pulmonaires humaines pour étudier les infections pulmonaires chroniques
Annonces
Certains agents pathogènes bactériens forment des biofilms au cours des processus d'infection pour se protéger des médicaments ou des cellules du système immunitaire humain. Chaque année, plus de 500 000 personnes meurent d'infections associées à des biofilms. Des chercheurs de l'Institut Helmholtz de recherche pharmaceutique de la Sarre (HIPS) ont mis au point une nouvelle méthode pour placer ces biofilms sur des cellules pulmonaires en laboratoire. Le système modèle produit par "bioprinting" devrait aider à mieux comprendre les processus d'infection et contribuer au développement de nouvelles substances actives. Les chercheurs ont publié leurs résultats dans la revue Biofabrication.
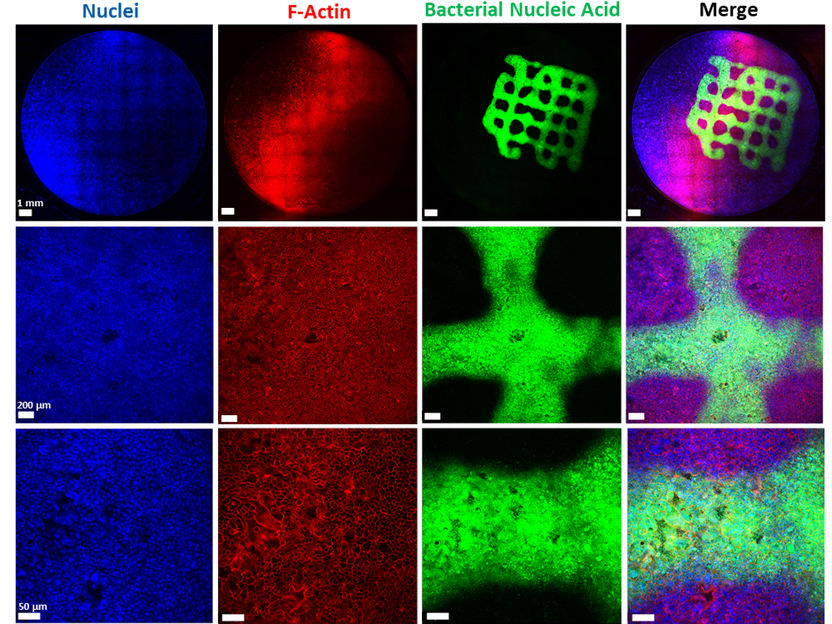
Image au microscope à fluorescence de biofilms imprimés sur des cellules épithéliales pulmonaires.
Licensed under CC BY 4.0, Aliyazdi et al. 2023, Biofabrication. DOI: 10.1088/1758-5090/acd95e
Pour développer de nouvelles thérapies contre les infections, les chercheurs dépendent de modèles de laboratoire qui leur permettent de simuler et d'étudier le processus d'infection. Ces modèles sont essentiels, en particulier lors des premiers essais et du développement de substances actives, afin de réduire au maximum le nombre d'expériences nécessaires sur les animaux. Dans le cas des infections associées à un biofilm, ces modèles sont très complexes, car avec le biofilm, en plus des cellules humaines et des agents pathogènes, un autre composant entre en jeu et doit être reproduit de la manière la plus réaliste possible. Une équipe dirigée par Claus-Michael Lehr, chef du département "Drug Delivery across Biological Barriers" à l'HIPS et professeur de biopharmacie et de technologie pharmaceutique à l'université de la Sarre, est parvenue à mettre au point et à caractériser un tel système modèle. Le HIPS est un site du Centre Helmholtz de recherche sur les infections (HZI) en coopération avec l'université de la Sarre.
Dans l'étude publiée, les cellules bactériennes, y compris le biofilm, sont placées sur une couche de cellules épithéliales pulmonaires à l'aide d'une imprimante 3D spéciale. Cette "bio-impression" est un processus complexe qui nécessite une encre aux propriétés particulières. "Le développement d'un modèle d'infection par biofilm n'est pas anodin, car la croissance rapide des bactéries et la libération de toxines peuvent facilement entraîner la mort prématurée des cellules pulmonaires. Par conséquent, la préservation du biofilm dans un tel système nécessite un environnement très contrôlé", explique Claus-Michael Lehr. "Nous avons optimisé nos biofilms imprimés en 3D pour qu'ils soient très proches d'un biofilm natif. L'un des principaux défis consistait à faire en sorte que les biofilms artificiels conservent leur forme après l'élimination de l'excès de bioink et n'aient pas d'effet toxique sur les cellules pulmonaires sous-jacentes. Ces deux défis ont permis d'obtenir des résultats encourageants avec le modèle développé". Pour tester la biocompatibilité avec les cellules humaines, les biofilms ont été imprimés sur des cellules épithéliales bronchiques humaines. Les constructions produites ont été évaluées à l'aide de la microscopie à fluorescence et de la microscopie électronique, entre autres méthodes, et ont été progressivement optimisées. La sensibilité des bactéries du biofilm aux antibiotiques utilisés en clinique a également été étudiée. Les biofilms imprimés ont conduit à une protection des bactéries contre les traitements antibiotiques similaire à celle des biofilms natifs et conviennent donc parfaitement pour simuler un traitement.
"Notre méthode peut désormais être utilisée pour analyser simultanément plusieurs aspects d'une infection associée à un biofilm, notamment la morphologie, la sensibilité aux antibiotiques ou les changements dans le métabolisme", explique Samy Aliyazdi, doctorant dans le département de Claus-Michael Lehr et premier auteur de l'étude. "Grâce à la bio-impression 3D, nous avons pu générer un modèle in vitro robuste basé sur l'homme que nous prévoyons maintenant d'utiliser pour le développement de nouveaux anti-infectieux."
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Annonces