Des larmes au lieu du sang
Capteur avec capacité de séparation : diagnostic de la jaunisse à partir des fluides lacrymaux
Les fluides lacrymaux humains contiennent de nombreuses protéines, métabolites et autres molécules dont les concentrations changent de manière significative avec certaines maladies. Une équipe de recherche vient de mettre au point un kit de test pratique pour les larmes, capable d'identifier les patients atteints de jaunisse. Leur succès repose sur un capteur hybride qui élimine simultanément les impuretés de l'échantillon. Cette approche pourrait fournir de nouvelles méthodes de détection et de diagnostic précoces basées sur des fluides corporels complexes, comme le rapporte l'équipe dans la revue Angewandte Chemie.
© Wiley-VCH
Un avantage particulier du diagnostic des fluides lacrymaux est que les échantillons peuvent être collectés de manière confortable et non invasive. Une méthode appelée spectroscopie Raman améliorée par la surface (SERS) est un candidat idéal pour l'analyse des biomolécules obtenues. L'effet Raman est un phénomène dans lequel la lumière frappant les matériaux provoque des vibrations et des rotations caractéristiques des fragments moléculaires. Le décalage de la fréquence de la lumière diffusée qui en résulte donne une "empreinte digitale" moléculaire. Si les molécules d'analyte sont en contact avec une surface métallique (points chauds), les signaux Raman sont suffisamment amplifiés pour atteindre l'ultra-sensibilité requise pour le diagnostic des larmes. Le marquage des analytes est inutile. Des dispositifs manuels Raman compacts seraient disponibles pour un diagnostic direct sur le terrain. Le problème consiste à trouver des capteurs SERS appropriés. Les capteurs actuels sont rapidement désactivés par le dépôt des composants des larmes. Existe-t-il un moyen de faire fonctionner ce système sans préparation complexe des échantillons ?
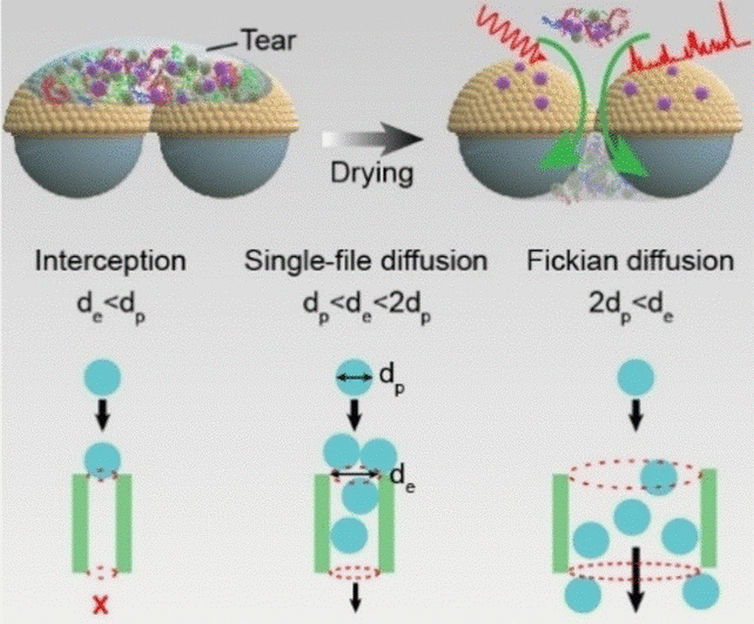
En fait, il y en a un. Une équipe dirigée par Yun Feng (troisième hôpital de l'université de Pékin), Zhou Yang (université des sciences et des technologies de Pékin) et Tie Wang (université des technologies de Tianjin et Académie chinoise des sciences de Pékin) en a fait la démonstration avec son nouveau kit de test de diagnostic de la taille d'une boîte d'allumettes. Son cœur est un film hybride. Une couche de nanosphères de dioxyde de silicium disposées symétriquement est recouverte d'une couche d'or très fine, sur laquelle est déposée une couche de nanoparticules d'or qui agissent comme des points chauds SERS. Les molécules cibles se lient à l'or et sont retenues à la surface, tandis que les composants lacrymaux plus petits glissent par les interstices entre les nanoparticules de dioxyde de silicium sur une couche absorbante située en dessous. Le diamètre des pores peut être ajusté en modifiant la taille des nanosphères pour séparer sélectivement les composants primaires perturbateurs des larmes (albumine, lysozyme, IgG et peroxydase). Le film, appelé SiO2@Au@AuNPs, est pris en sandwich entre deux supports en verre et enfermé dans un boîtier. Une pointe dépasse du dispositif pour recueillir le liquide lacrymal au coin de l'œil. L'analyse SERS s'effectue à travers une fenêtre située sur le dessus du dispositif.
L'équipe a réussi à identifier les patients atteints de jaunisse, un trouble métabolique associé à des maladies du foie et de la vésicule biliaire. La bilirubine, un pigment biliaire, n'est pas correctement excrétée par l'organisme, se concentre et peut se retrouver dans le liquide lacrymal. La bilirubine se lie fortement à l'or du capteur et peut être détectée avec une grande sensibilité par son signal SERS.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.























































