Une graisse saine ? Le facteur de transcription C/EBPβ influence positivement le stockage des graisses
Pourrons-nous bientôt contrôler le stockage de l'excès de graisse ?
Annonces
La maladie nutritionnelle et métabolique chronique qu'est l'obésité se caractérise par une augmentation excessive de la graisse corporelle et son accumulation dans les tissus. Les personnes souffrant d'obésité présentent également un risque accru de maladies concomitantes ou secondaires telles que le diabète de type 2, la stéatose hépatique et l'athérosclérose. Des chercheurs de l'Institut européen de recherche sur la biologie du vieillissement (ERIBA) de Groningue, aux Pays-Bas, et de l'Institut Leibniz sur le vieillissement - Institut Fritz Lipmann (FLI) d'Iéna, en Allemagne, viennent de démontrer pour la première fois dans un modèle de souris comment le facteur de transcription C/EBPβ peut influencer positivement le stockage des graisses et maintenir la santé, même dans le cadre d'un régime particulièrement riche en graisses.
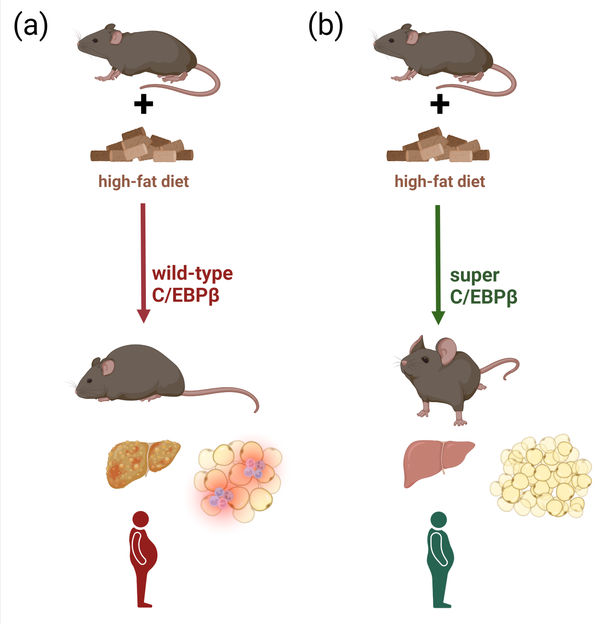
Des souris génétiquement modifiées avec une fonction accrue du facteur de transcription C/EBPβ (b) stockent l'excès de graisse dans un tissu adipeux hyperplasique. Lors d'un régime riche en graisses, ces souris présentent un tissu adipeux moins enflammé et sont en bien meilleure santé.
FLI / Kerstin Wagner; created with BioRender.com
Ces dernières années, le nombre de personnes en surpoids et obèses dans les pays industrialisés a fortement augmenté. En Allemagne, par exemple, une personne sur deux est aujourd'hui en surpoids, et environ 20 % de la population est obèse. L'obésité est définie comme un poids corporel excessif causé par une proportion extrêmement élevée de graisse, généralement due à une accumulation de graisse dans des cellules adipeuses (adipocytes) fortement hypertrophiées (hypertrophiques) dans l'abdomen. Cette graisse dite viscérale entraîne une inflammation, qui joue un rôle essentiel dans le développement et la progression de divers troubles métaboliques, notamment le diabète de type 2, les maladies cardiaques, les accidents vasculaires cérébraux et certains cancers. C'est pourquoi l'augmentation mondiale de la prévalence de l'obésité est une préoccupation croissante en matière de santé publique, et les liens entre l'obésité et les problèmes de santé font l'objet d'une étude intensive.
Dans une étude récente publiée dans la revue eLife, des chercheurs de l'Institut européen de recherche sur la biologie du vieillissement (ERIBA) à Groningue, aux Pays-Bas, et de l'Institut Leibniz sur le vieillissement - Institut Fritz Lipmann (FLI) à Iéna, en Allemagne, ont démontré que des souris génétiquement modifiées avec une fonction accrue du facteur de transcription C/EBPβ peuvent stocker l'excès de graisse de telle sorte qu'elles restent en bonne santé même dans des conditions stressantes, comme un régime alimentaire très riche en graisses.
Le site de stockage des graisses influence la santé
Le stockage des graisses dans le dépôt de graisse viscérale se fait principalement par l'augmentation de la taille des cellules graisseuses individuelles (stockage hypertrophique des graisses). Toutefois, lorsque ces cellules atteignent leur capacité de stockage maximale, la consommation continue de graisses commence à s'accumuler de manière préjudiciable dans les tissus situés en dehors des dépôts de graisses (stéatose), en particulier dans le foie et les muscles, ce qui entraîne une altération de la fonction de ces tissus. "Il existe toutefois un sous-groupe de personnes qui, bien qu'obèses pendant une longue période, ne connaissent pas de problèmes de santé notables", rapporte le professeur Cornelis Calkhoven, ancien chef de groupe de recherche au FLI, qui travaille désormais à l'ERIBA.
Des études antérieures ont démontré que deux éléments en particulier contribuent à ce phénotype d'obésité saine : Tout d'abord, la graisse stockée non pas dans l'abdomen mais sous forme de graisse sous-cutanée sous la peau des bras, des cuisses et du dos est meilleure pour la santé. En outre, la graisse stockée dans le tissu adipeux dit hyperplasique, qui est formé par une augmentation du nombre de cellules graisseuses (stockage hyperplasique de la graisse), est également beaucoup moins susceptible de causer des dommages. Étant donné que davantage de cellules sont disponibles pour le stockage des graisses, elles restent plus petites et sont donc métaboliquement plus saines et moins enflammées. "Toutefois, notre connaissance des facteurs génétiques qui régulent les conditions favorables susmentionnées du stockage des graisses est encore très limitée et nécessite des études plus détaillées", ajoute le professeur Calkhoven.
Une fonction accrue du facteur de transcription C/EBPβ contrôle le stockage des graisses
Lorsque des souris sont nourries en laboratoire avec un régime riche en graisses, en peu de temps elles prennent du poids, deviennent obèses et développent des problèmes métaboliques similaires à ceux des humains obèses, notamment une inflammation du tissu adipeux, une accumulation de graisses dans des tissus normalement dépourvus de graisses tels que le foie et les muscles, et un diabète de type 2.
"Dans notre étude actuelle, nous avons pu montrer d'une part que les souris génétiquement modifiées avec une fonction accrue du facteur de transcription C/EBPβ stockent l'excès de graisse principalement dans le tissu adipeux hyperplasique avec des cellules graisseuses plus nombreuses et plus petites", rapporte le Dr Christine Müller de l'ERIBA. Même avec des régimes extrêmement riches en graisses, ces souris à superfonction C/EBPβ présentent moins d'inflammation du tissu adipeux, n'accumulent pas de graisses dans le foie ou le cœur et conservent un métabolisme du glucose sain. En revanche, chez les mâles, la superfonction C/EBPβ stimule également un stockage favorable des graisses dans des dépôts sous la peau. "Ces deux facteurs contribuent à un phénotype obèse sain chez l'homme", a déclaré le Dr Müller.
Dans deux études publiées précédemment, les chercheurs d'Iéna et de Groningue ont déjà démontré que les mêmes souris à superfonction C/EBPβ, soumises à un régime alimentaire normal, ont un métabolisme généralement amélioré, qui est également associé à moins de cancer et à un retard prononcé de plusieurs maladies liées au vieillissement par rapport à leurs congénères de type sauvage.
Serons-nous bientôt en mesure de contrôler le stockage des graisses excédentaires ?
"Nos études fournissent des preuves impressionnantes que la superfonction C/EBPβ adapte la physiologie des souris vers un métabolisme plus sain, même dans des conditions nutritionnelles malsaines, comme lorsqu'elles sont stressées par un régime riche en graisses", a expliqué le Pr Calkhoven, résumant les résultats. "L'étude actuelle identifie le facteur de transcription C/EBPβ comme un régulateur clé du stockage sain des graisses, mais soulève en même temps la question de savoir si l'induction pharmacologique de la superfonction de C/EBPβ peut potentiellement être utilisée pour réorienter le stockage de l'excès de graisse du mode hypertrophique nocif au mode hyperplastique plus bénéfique. Cela aurait d'immenses implications pour la santé métabolique et le vieillissement."
Les premières études ont déjà montré qu'une telle stratégie pharmacologique de ciblage de C/EBPβ est en principe réalisable. Le développement de tels médicaments aurait donc d'énormes implications pour le traitement de l'obésité et des maladies métaboliques associées.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.
Publication originale
Enhanced C/EBPβ function promotes hyperplastic versus hypertrophic fat tissue growth and prevents steatosis in response to high-fat diet feeding. Müller C, Zidek LM, Eichwald S, Kortman G, Koster MH, Calkhoven CF. eLife 2022, 11, e62625.
Reduced expression of C/EBPβ-LIP extends health- and lifespan in mice. Müller C, Zidek LM, Ackermann T, de Jong T, Liu P, Kliche V, Zaini MA, Kortman G, Harkema L, Verbeek DS, Tuckermann JP, von Maltzahn J, de Bruin A, Guryev V, Wang ZQ, Calkhoven CF. eLife 2018, 7, e34985.
A screening strategy for the discovery of drugs that reduce C/EBPβ-LIP translation with potential calorie restriction mimetic properties. Zaini MA, Müller C, Ackermann T, Reinshagen J, Kortman G, Pless O, Calkhoven CF. Scientific Rep. 2017, 7, 42603.