Las enzimas abren una nueva vía hacia la sangre de donante universal
Los investigadores han descubierto enzimas que eliminan los obstáculos que se interponían en el desarrollo de la sangre de donante universal
La búsqueda de sangre de donante universal ha dado un paso decisivo. Investigadores de la Universidad Técnica de Dinamarca (DTU) y la Universidad de Lund han descubierto enzimas que, mezcladas con glóbulos rojos, son capaces de eliminar azúcares específicos que constituyen los antígenos A y B de los grupos sanguíneos ABO humanos. Los resultados se han publicado en la revista científica Nature Microbiology.
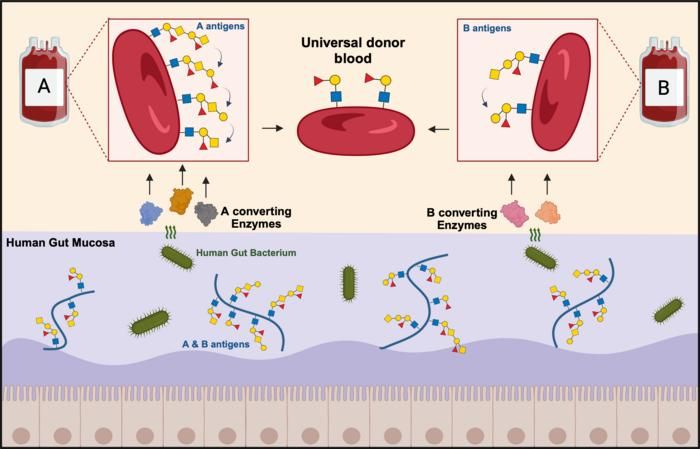
Los antígenos del grupo sanguíneo ABO que se encuentran en la superficie de los glóbulos rojos también se encuentran en la capa mucosa que recubre la superficie del intestino. Los investigadores han aprovechado una bacteria intestinal humana especializada y su capacidad para utilizar estos antígenos como nutrientes para descubrir y desarrollar dos mezclas enzimáticas que convierten los glóbulos rojos de los grupos A y B en sangre de donante universal.
Graphic: Mathias Jensen, postdoc at DTU.
"Por primera vez, los nuevos cócteles enzimáticos no sólo eliminan los antígenos A y B bien descritos, sino también variantes ampliadas que antes no se reconocían como problemáticas para la seguridad de las transfusiones. Estamos cerca de poder producir sangre universal a partir de donantes del grupo B, mientras que aún queda trabajo por hacer para convertir la sangre del grupo A, más compleja. Nuestro objetivo ahora es investigar en detalle si existen obstáculos adicionales y cómo podemos mejorar nuestras enzimas para alcanzar el objetivo final de la producción de sangre universal", afirma el profesor Maher Abou Hachem, director del estudio en la DTU y uno de los científicos principales del descubrimiento.
Afirma que el descubrimiento es el resultado de combinar la experiencia de investigadores de la DTU en enzimas de la microbiota intestinal humana y de investigadores de la Universidad de Lund en grupos sanguíneos basados en carbohidratos y medicina transfusional.
Gran demanda de sangre de donantes
Los glóbulos rojos humanos son portadores de estructuras complejas específicas de azúcares (antígenos) que definen los cuatro grupos sanguíneos ABO A, B, AB y O. Estos antígenos controlan la compatibilidad entre donantes y receptores para que las transfusiones de sangre y los trasplantes de órganos sean seguros. La sangre de los donantes se analiza para detectar marcadores de enfermedad y los principales grupos sanguíneos. Después puede almacenarse refrigerada hasta 42 días.
La necesidad de sangre de donante es alta debido a que las personas mayores constituyen una proporción mayor de la población y a que hay más pacientes sometidos a procedimientos médicos que requieren una gran cantidad de sangre. Convertir con éxito los tipos de sangre A o B en sangre ABO de donante universal puede reducir notablemente la logística y los costes asociados actualmente al almacenamiento de cuatro tipos de sangre diferentes. Además, el desarrollo de la sangre de donante universal permitirá aumentar el suministro de sangre de donante al reducir el desperdicio de sangre que se acerca a su fecha de caducidad.
La razón por la que es necesario eliminar los antígenos A y B para crear sangre de donante universal es que pueden desencadenar reacciones inmunitarias potencialmente mortales cuando se transfunden a receptores no compatibles.
El concepto de utilizar enzimas para generar sangre de donante universal se introdujo hace más de 40 años. Desde entonces, se han descubierto enzimas de mayor eficacia para eliminar los antígenos A y B, pero los investigadores aún no son capaces de explicar o abolir todas las reacciones inmunitarias relacionadas con la sangre, por lo que estas enzimas todavía no se utilizan en la práctica clínica.
Enzimas del intestino
Los grupos de investigación de la DTU y la Universidad de Lund han buscado nuevas formas de encontrar enzimas capaces de eliminar tanto los antígenos sanguíneos A y B como los azúcares que los bloquean. Los equipos de investigación descubrieron nuevas mezclas de enzimas procedentes de la bacteria intestinal humana Akkermansia muciniphila, que se alimenta descomponiendo la mucosidad que recubre la superficie del intestino. Resulta que estas enzimas son excepcionalmente eficaces, ya que los azúcares complejos de la superficie de la mucosa intestinal comparten parecido químico con los que se encuentran en la superficie de las células sanguíneas.
"Lo especial de la mucosa es que las bacterias, que pueden vivir en este material, suelen tener enzimas hechas a medida para descomponer las estructuras de azúcar de la mucosa, entre las que se encuentran los antígenos ABO del grupo sanguíneo". Esta hipótesis resultó ser correcta", afirma Maher Abou Hachem.
Los investigadores de este estudio probaron 24 enzimas, que utilizaron para procesar cientos de muestras de sangre.
"La sangre universal creará una utilización más eficiente de la sangre de los donantes, y también evitará dar transfusiones ABO-no coincidentes por error, lo que de otro modo puede llevar a consecuencias potencialmente fatales en el receptor. Cuando podamos crear sangre de donante ABO-universal, simplificaremos la logística de transporte y administración de productos sanguíneos seguros, al tiempo que minimizaremos el desperdicio de sangre", afirma el profesor Martin L. Olsson, responsable del estudio en la Universidad de Lund.
Los investigadores de la DTU y la Universidad de Lund han solicitado una patente sobre las nuevas enzimas y el método de tratamiento enzimático, y esperan seguir avanzando en este sentido en su nuevo proyecto conjunto durante los próximos tres años y medio. Si tiene éxito, el concepto deberá probarse en ensayos controlados con pacientes antes de que pueda considerarse su producción comercial y uso clínico.
El proyecto de investigación inicial está financiado por el Fondo de Investigación Independiente de Dinamarca (Tecnología y Ciencias de la Producción, FTP), el Consejo Sueco de Investigación, subvenciones ALF del gobierno sueco y consejos comarcales, así como la Fundación Knut y Alice Wallenberg y el Fondo de Investigación de Dinamarca, Ciencias Naturales, FNU), mientras que el nuevo proyecto continuado está financiado por la Fundación Novo Nordisk, Programa de Sinergias Interdisciplinarias.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Mathias Jensen, Linn Stenfelt, Jennifer Ricci Hagman, Michael Jakob Pichler, Julia Weikum, Tine Sofie Nielsen, Annika Hult, Jens Preben Morth, Martin L. Olsson, Maher Abou Hachem; "Akkermansia muciniphila exoglycosidases target extended blood group antigens to generate ABO-universal blood"; Nature Microbiology, 2024-4-29