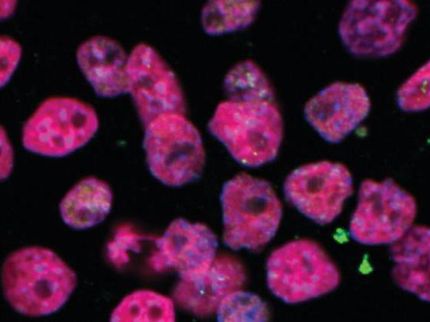
Un hito: Los investigadores han generado células germinales primordiales a partir de células madre, una primicia mundial.
Un gran paso hacia la producción de gametos de rinoceronte
Para salvar de la extinción al rinoceronte blanco del norte, el equipo de BioRescue se apresura a crear en laboratorio óvulos y espermatozoides de esta subespecie en peligro crítico. El equipo acaba de publicar un hito en Science Advances: han generado células germinales primordiales a partir de células madre, una primicia mundial.

Las dos últimas hembras viven en la reserva natural keniana "Ol Pejeta".
Jan Stejkal, Safari Park Dvůr Králové
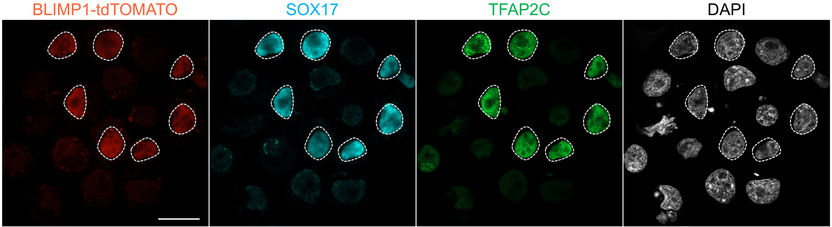
El gen SOX17 desempeñó un papel clave en la inducción de células germinales primordiales a partir de células madre pluripotentes del rinoceronte blanco.
Masafumi Hayashi, Universität Osaka

Najin, de 33 años, y su hija Fatu son los últimos rinocerontes blancos del norte que sobreviven en el planeta. Viven juntas en una reserva natural de Kenia. Con sólo dos hembras, esta subespecie de rinoceronte blanco ya no es capaz de reproducirse, al menos por sí sola. Pero no se han perdido todas las esperanzas: según un artículo publicado en la revista "Science Advances", un equipo internacional de investigadores ha logrado cultivar células germinales primordiales (PGC) -las precursoras de los óvulos y espermatozoides de rinoceronte- a partir de células madre embrionarias (ESC) y células madre pluripotentes inducidas (iPSC).
Esto representa un hito importante en un ambicioso plan. El proyecto BioRescue, coordinado por el Instituto Leibniz para la Investigación de Zoológicos y Vida Silvestre (Leibniz-IZW) y financiado por el Ministerio Federal de Educación e Investigación de Alemania (BMBF) desde 2019, quiere salvar al rinoceronte blanco del norte de la extinción. Para ello, los científicos siguen dos estrategias: una de ellas trata de generar espermatozoides y óvulos viables a partir de células de la piel de rinocerontes fallecidos. La idea es implantar los embriones resultantes en hembras de rinoceronte blanco del sur estrechamente emparentadas, que luego llevarán a término la descendencia subrogada. De este modo, la subespecie de rinoceronte blanco del norte, que los humanos ya han exterminado mediante la caza furtiva, podría salvarse gracias a las tecnologías reproductivas y de células madre más avanzadas.
Primer éxito con una especie amenazada
Pasar de un trozo de piel a un rinoceronte vivo puede ser una auténtica proeza de ingeniería celular, pero el proceso en sí no es inédito: el profesor Katsuhiko Hayashi, coautor del estudio, dirige laboratorios de investigación en las universidades japonesas de Osaka y Kyushu, en Fukuoka, donde sus equipos ya han logrado esta hazaña utilizando ratones. Pero para cada nueva especie, los pasos individuales son territorio inexplorado. En el caso del rinoceronte blanco del norte, Hayashi trabaja en estrecha colaboración con la Plataforma Tecnológica de Células Madre Pluripotentes del Dr. Sebastian Diecke, del Centro Max Delbrück, y con el profesor Thomas Hildebrandt, experto en reproducción del Leibniz-IZW. Los dos científicos berlineses son también coautores del presente estudio.
"Es la primera vez que se han generado con éxito células germinales primordiales de una especie de mamífero grande y en peligro de extinción a partir de células madre", explica el primer autor del estudio, Masafumi Hayashi, de la Universidad de Osaka. Anteriormente, sólo se había logrado en roedores y primates. A diferencia de los roedores, los investigadores han identificado el gen SOX17 como un actor clave en la inducción de PGC de rinoceronte. SOX17 también desempeña un papel esencial en el desarrollo de las células germinales humanas y, por tanto, posiblemente en las de muchas especies de mamíferos.
Las células madre embrionarias de rinoceronte blanco del sur utilizadas en Japón proceden del laboratorio Avantea de Cremona (Italia), donde fueron cultivadas por el equipo del profesor Cesare Galli. Las células madre embrionarias de rinoceronte blanco del norte, por su parte, proceden de las células de la piel de la tía de Fatu, Nabire, que murió en 2015 en el Safari Park Dvůr Králové de la República Checa. El equipo de Diecke en el Centro Max Delbrück se encargó de convertirlas en células madre pluripotentes inducidas.
Siguiente paso: maduración celular
Masafumi Hayashi afirma que esperan utilizar la tecnología punta de células madre del laboratorio de Katsuhiko Hayashi para salvar otras especies de rinocerontes en peligro: "Hay cinco especies de rinoceronte, y casi todas están clasificadas como amenazadas en la Lista Roja de la UICN". El equipo internacional también utilizó células madre para cultivar PGC del rinoceronte blanco del sur, cuya población mundial ronda los 20.000 ejemplares. Además, los investigadores pudieron identificar dos marcadores específicos, CD9 e ITGA6, que se expresaban en la superficie de las células progenitoras de ambas subespecies de rinoceronte blanco. "De cara al futuro, estos marcadores nos ayudarán a detectar y aislar las PGC que ya han surgido en un grupo de células madre pluripotentes", explica Hayashi.
Los científicos de BioRescue deben pasar ahora a la siguiente tarea difícil: madurar las PGC en el laboratorio para convertirlas en óvulos y espermatozoides funcionales. "Las células primordiales son relativamente pequeñas en comparación con las células germinales maduras y, lo que es más importante, todavía tienen un doble juego de cromosomas", explica la Dra. Vera Zywitza, del grupo de investigación de Diecke, que también participó en el estudio. "Por tanto, tenemos que encontrar las condiciones adecuadas para que las células crezcan y dividan su juego cromosómico por la mitad".
La variación genética es clave para la conservación
Hildebrandt, investigador del Leibniz-IZW, también persigue una estrategia complementaria. Quiere obtener óvulos de Fatu, de 22 años, y fecundarlos en el laboratorio de Galli, en Italia, con esperma congelado recogido de cuatro toros de rinoceronte blanco del norte ya fallecidos. Este esperma se descongela y se inyecta en el óvulo en un proceso conocido como inyección intracitoplasmática de espermatozoides(ICSI). Sin embargo, Hildebrandt explica que Fatu no puede tener descendencia, ya que tiene problemas en los tendones de Aquiles y no puede soportar más peso. Su madre, Najin, ya ha superado la edad fértil y también padece tumores ováricos. "Y en cualquier caso, como sólo nos queda una donante de óvulos naturales, la variación genética de cualquier descendencia resultante sería demasiado pequeña para crear una población viable", añade.
La principal prioridad del equipo, por tanto, es convertir las PGC que ahora tienen a su disposición en óvulos. "En ratones, descubrimos que la presencia de tejido ovárico era importante en este paso crucial", explica Zywitza. "Como no podemos simplemente extraer este tejido de las dos hembras de rinoceronte, probablemente tendremos que cultivarlo también a partir de células madre". Sin embargo, el científico tiene esperanzas de que el tejido ovárico de los caballos pueda ser útil, ya que los caballos se encuentran entre los parientes vivos más cercanos de los rinocerontes desde el punto de vista evolutivo. Si el ser humano hubiera cuidado al rinoceronte salvaje con el mismo esmero que al caballo domesticado, el inmenso reto al que se enfrentan ahora los científicos de BioRescue podría haberse evitado por completo.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.