Cuando la digestión de los macrófagos va mal
Si la secreción de los alvéolos pulmonares no se elimina con regularidad, pueden aparecer dificultades respiratorias.
En un estudio publicado en Science Immunology, un equipo dirigido por Alexander Mildner y Achim Leutz ha explicado el papel fundamental del factor de transcripción C/EBPb en este proceso.
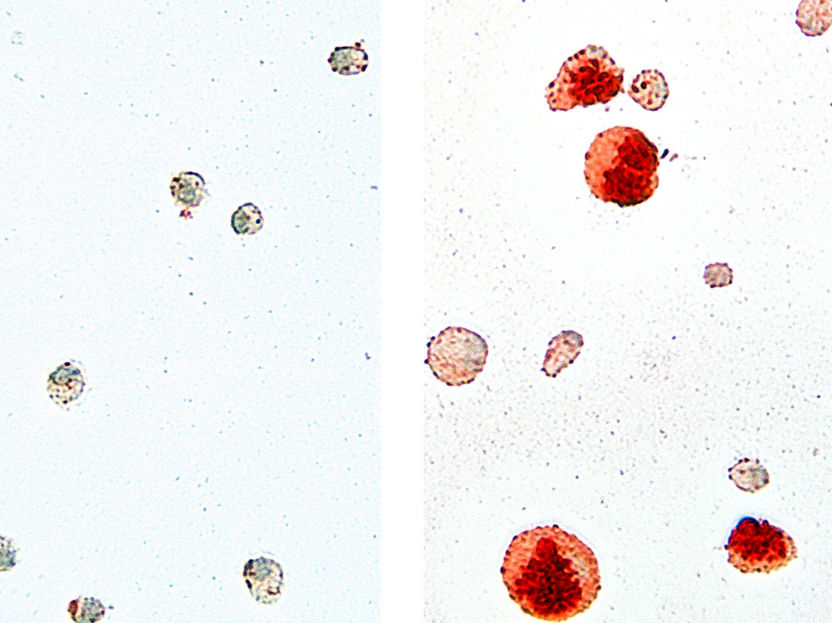
Macrófagos alveolares aislados de los pulmones de ratones de tipo salvaje (izquierda) y de animales deficientes en Cebpb (derecha). Las células se tiñeron con la tinción OilRed O para visualizar los lípidos intracelulares (rojo). Las células que carecen de Cebpb muestran un fenotipo grande y distendido con una alta deposición de lípidos.
AG Leutz, MDC
El intercambio de gases entre el aire que respiramos y nuestra sangre tiene lugar a través de los alvéolos, pequeños sacos de aire en nuestros pulmones. Para que este proceso funcione sin problemas, las células epiteliales de los alvéolos producen una sustancia llamada "surfactante" que cubre los alvéolos como una película. Este complejo está formado principalmente por fosfolípidos y proteínas y sirve para reducir la tensión superficial de los alvéolos. También actúa como un filtro, atrapando de forma fiable las bacterias y los virus que entran en los pulmones cuando inhalamos.
El tensioactivo se segrega continuamente, ya que los macrófagos alveolares (AM) -células carroñeras de los alvéolos- descomponen y eliminan constantemente la sustancia utilizada. Este proceso mantiene el equilibrio adecuado entre la síntesis y la eliminación del tensioactivo, un estado conocido como homeostasis. "Pero si se estropea, se acumula cada vez más secreción en los pulmones, lo que dificulta la respiración y aumenta el riesgo de infecciones pulmonares", explica el profesor Alexander Mildner, antiguo becario Heisenberg en el Centro Max Delbrück y actual jefe de grupo en la Universidad de Turku. Mildner es el último autor del estudio y lleva 20 años investigando los macrófagos. "Queríamos saber qué es lo que impide que estos fagocitos pulmonares funcionen correctamente", dice. Una acumulación excesiva de surfactante puede dar lugar a la proteinosis alveolar pulmonar (PAP), una enfermedad hasta ahora incurable que, en los casos más graves, obliga a lavar regularmente los pulmones de los pacientes.
El papel crucial de C/EBPb
El estudio fue impulsado por el descubrimiento de que los macrófagos alveolares no pueden desarrollarse adecuadamente si carecen de C/EBPb. El profesor Achim Leutz lleva muchos años investigando la función de este factor de transcripción. Es jefe del Laboratorio de Diferenciación Celular y Tumorigénesis del MDC, que acogió al grupo de investigación independiente de Mildner. Otros investigadores del MDC que participaron en el estudio fueron la Dra. Uta Höpken y el Dr. Darío Jesús Lupiáñez García. Mediante estudios de biología molecular y experimentos con animales, el equipo pudo explicar el papel de C/EBPb. Sus resultados se han publicado ahora en la revista Science Immunology.
"Aislamos macrófagos alveolares de ratones sanos y de aquellos que carecían del gen de C/EBPb y realizamos pruebas in vitro con estas células inmunitarias", explica la autora principal del estudio, la Dra. Dorothea Dörr. "También realizamos varios análisis del genoma y del transcriptoma de las células recién aisladas". En concreto, la investigadora estudió las propiedades biológicas y moleculares de los AM, es decir, su capacidad para absorber y metabolizar lípidos. Mientras que los macrófagos de los ratones sanos realizaban sus tareas correctamente, los extraídos de los ratones modificados genéticamente captaban y almacenaban una gran cantidad de lípidos, pero eran incapaces de digerirlos. En su lugar, se hincharon en las llamadas "células de espuma" y pronto perecieron, volviendo a depositar los lípidos ingeridos. Este mismo fenómeno ha sido observado por los médicos que tratan la enfermedad pulmonar PAP. Además, los macrófagos defectuosos apenas pudieron proliferar.
Una pieza importante del rompecabezas
Los análisis moleculares demostraron además que otro gen importante -también un factor de transcripción- está regulado a la baja en los ratones que carecen del gen C/EBPb: PPARg. Cuando se activa, estimula, entre otras cosas, la captación de ácidos grasos y la diferenciación de las células grasas y los macrófagos del organismo.
La enfermedad pulmonar PAP suele ser el resultado de problemas en la vía de señalización de la citocina GM-CSF, que significa factor estimulante de colonias de granulocitos y macrófagos. "Ya sabíamos que ciertas funciones esenciales de los macrófagos alveolares se controlan a través de la vía de señalización del GM-CSF", dice Mildner. "Ahora hemos descubierto que los macrófagos deficientes en C/EBPb muestran graves disfunciones en la proliferación de estas células y en la degradación del surfactante, provocando una patología similar a la de la PAP en los ratones". Parece, por tanto, que C/EBPb es el eslabón regulador que falta entre las vías de señalización de GM-CSF y PPARg. "Es como un rompecabezas", explica Leutz. "Si se coloca una pieza determinada, de repente es mucho más fácil encontrar otras piezas que faltan".
¿Una clave para entender otras enfermedades?
Los macrófagos pueden ser las células carroñeras del sistema inmunitario, pero hacen mucho más que eliminar bacterias y virus de nuestro sistema. Cada órgano tiene sus propios macrófagos especializados. En la remodelación del cerebro, por ejemplo, tienen la tarea de descomponer las neuronas y las sinapsis que ya no son necesarias. Si no realizan esta tarea correctamente, pueden desarrollarse enfermedades del sistema nervioso central.
Un metabolismo lipídico defectuoso no sólo es la causa de la PAP, sino que también es responsable de la aterosclerosis, una grave enfermedad vascular. Durante esta enfermedad, se acumulan cada vez más depósitos de grasa en las paredes de las arterias, donde son atrapados por glóbulos blancos como los macrófagos. Estos macrófagos ingieren los lípidos pero no pueden descomponerlos adecuadamente, por lo que se hinchan y forman placas. Si las placas se rompen, la grasa que contienen se escapa y puede formar coágulos que bloqueen las arterias, lo que puede provocar un derrame cerebral o un infarto.
"Creemos que la vía de señalización que hemos esclarecido podría ser importante en muchas enfermedades relacionadas con los lípidos", dice Mildner. "Así que la pregunta ahora es si lo que hemos aprendido de los macrófagos alveolares también podría ayudarnos a entender mejor la aterosclerosis y la obesidad mórbida (adiposidad)".
En cuanto a la PAP, es posible que ahora se vislumbre un nuevo tratamiento. Ya se conocen agentes terapéuticos que pueden modular la PPARg. Si se utilizan en combinación con un fármaco activador de C/EBPb, podría ser posible poner en marcha el metabolismo lipídico de los macrófagos alveolares desregulados.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.