Innovative Methode macht neu hergestellte Proteine in lebenden Fliegen sichtbar
Details zu einer neuen Forschungsmethode haben Wissenschaftler um Prof. Dr. Daniela Dieterich vom Institut für Pharmakologie und Toxikologie der Otto-von-Guericke-Universität Magdeburg (OVGU) und Dr. Ulrich Thomas vom Leibniz-Institut für Neurobiologie (LIN) kürzlich im Fachmagazin Nature Communications veröffentlicht.

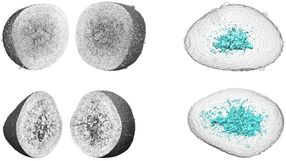
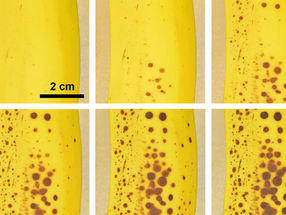
Neuhergestellte Proteine können in den Muskelzellen von Fliegenlarven mit Hilfe des mutierten Enzyms LtoG-MetRS nach einer biochemischer Reaktion visualisiert werden.
Damit Gewebe und Organe funktionieren und vielzellige Organismen lebensfähig sind, ist das Zusammenspiel verschiedener Zelltypen entscheidend: Nervenzellen, Nierenzellen oder Muskelzellen unterscheiden sich enorm in ihrer Form und Funktion. Proteine (Eiweiße) bilden das individuelle Mobiliar der Zellen, aber auch ihre Werkzeugkiste und Infrastruktur – sie sorgen für die Vielfalt der Zellen. Bisher war es jedoch nicht möglich, die Bildung individueller Eiweiße in ganz bestimmten Zellen zu beobachten und so die Dynamik im Proteinhaushalt zu verstehen.
Den Magdeburger Forschern ist es gelungen, Proteine zellspezifisch im lebenden Organismus – der Fruchtfliege Drosophila melanogaster – zu markieren und damit jüngst hergestellte Eiweiße direkt sichtbar zu machen. Prof. Dieterich erklärt: „Das Spezialistentum einzelner Zelltypen ist engstens an deren Ausstattung mit Eiweißen unterschiedlichster Art und Menge gekoppelt. Hinzu kommt, dass Zellen ihren Proteingehalt an sich ändernde, innere oder äußere Bedingungen und Stimuli anpassen.“
Solche Anpassungsprozesse können beispielsweise den Stoffwechsel, die Immunabwehr oder Gehirnaktivitäten bei Lernprozessen betreffen. In vielen Fällen gehen sie dabei einher mit der Herstellung von Proteinen. So ist insbesondere die Bildung von Langzeitgedächtnis im Gehirn abhängig von der Eiweißsynthese. Dr. Thomas fügt hinzu: „Problematisch ist, dass man die neugebildeten Proteine nur schwer von den bereits existierenden Eiweißen unterscheiden kann, und dass in komplexen Organen wie dem Gehirn verschiedene Zelltypen dicht gepackt nebeneinander vorkommen.“
Um die neusynthetisierten Proteine zellspezifisch zu markieren, veränderten die Magdeburger Wissenschaftler ein Enzym, welches im Normalfall die Aminosäure Methionin für den Einbau in entstehende Proteine vorbereitet. Es ist dadurch in der Lage, eine künstliche Aminosäure anstelle des Methionins einzubauen. Über eine spezielle genetische Methode in der Fruchtfliege kann das mutierte Enzym in ausgewählten Zellpopulationen der Fruchtfliege hergestellt werden und so nach Fütterung der künstlichen Aminosäure den Einbau dieser in die Proteine der betreffenden Zellen bewirken.
Die Besonderheit der künstlichen Aminosäure ist eine chemische Modifikation, die durch eine biochemische Reaktion – die sogenannte „Klick-Chemie“ – gekoppelt werden kann. Das neu gebildete Protein ist dadurch markiert und kann unter dem Mikroskop oder durch biochemische Aufreinigungsverfahren sichtbar gemacht werden kann. Dies ermöglicht nun die Untersuchung kompletter Eiweißmuster oder auch einzelner Proteine in Zelltyp-spezifischer Weise im lebenden Organismus.
In einer in derselben Online-Ausgabe erschienenen zweiten Publikation bringt das Team um Prof. Dieterich und Dr. Thomas diese Technik in Kooperation mit dem Münsteraner Max Planck-Forscher Dr. Erik Storkebaum zur Anwendung. In einem Fliegenmodell für die menschliche Muskelerkrankung vom Typ des Morbus Charcot-Marie-Tooth (eine schwerwiegende neurale Muskelatrophie) konnte das Forscherteam zeigen, dass Motoneuronen der Fliegen, welche die phänotypischen Auswirkungen der Krankheit aufweisen, eine verringerte Protein-Syntheserate haben. Mit der innovativen Methode der Magdeburger Wissenschaftler ist es also nicht nur möglich, Proteinsynthese-abhängige Prozesse in gesunden Organismen zu untersuchen, sondern auch in Krankheitsmodellen nach Störungen im Proteinstoffwechsel zu suchen. Damit kann das Verfahren von großem Nutzen bei der Aufdeckung von Krankheitsursachen als Voraussetzung für die Entwicklung zellspezifischer Medikamente und erweiterter Therapiemöglichkeiten sein.
Originalveröffentlichung
Cell-selective labelling of proteomes in Drosophila melanogaster; Ines Erdmann et al.; Nature Communications 6, Article number: 7521
Impaired protein translation in Drosophila models for Charcot–Marie–Tooth neuropathy caused by mutant tRNA synthetases; Sven Niehues et al.; Nature Communications 6, Article number: 7520