Drei Eltern und ein Baby
Forschende raten zur Vorsicht bei künstlicher Befruchtungsmethode
Die Zulassung einer Behandlungsmethode, bei der drei Eltern künstlich ein Kind zeugen, wird seit einigen Jahren in Großbritannien diskutiert und ist möglicherweise in zwei Jahren Realität. Die Methode soll helfen, genetische Defekte der Mutter bereits im Reagenzglas zu eliminieren. Der Defekt liegt in den Mitochondrien, den „Kraftwerken“ der Zellen. Um defekte Mitochondrien loszuwerden, muss der Zellkern einer Eizelle in eine andere Eizelle, die intakte Mitochondrien trägt, transferiert werden. Forschende der Vetmeduni Vienna zeigen erstmals, dass bereits wenige defekte Mitochondrien, die bei einem Transfer mitgeschleppt werden, später Krankheiten verursachen könnten. Die Ergebnisse wurden im Journal Cell Reports veröffentlicht.

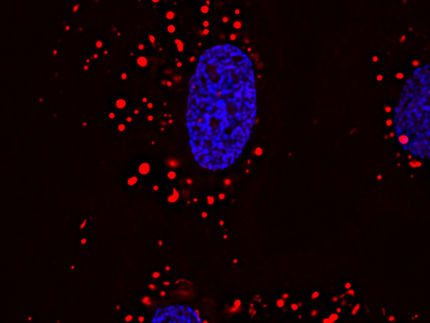
Schon wenige defekte Mitochondrien (hier in gelb oben im Bild), könnten schneller wachsen als gesunde (in blau) und so später eine Erkrankung verursachen.
Iain Johnston
Mitochondrien sind Zellorganellen, die sich im Inneren tierischer und menschlicher Zellen befinden. Sie produzieren Energie für den Organismus, besitzen ihr eigenes Erbmaterial, die mitochondriale DNA (mtDNA), und werden ausschließlich über die Mutter vererbt. Je nach Aktivität und Aufgabe besitzen Körperzellen unterschiedlich viele Mitochondrien. Meist sind es einige hundert bis tausend pro Zelle.
Mitochondriale Erbkrankheiten, sogenannte Mitochondropathien, treten weltweit bei etwa einer von 10.000 Personen auf. Beispielsweise können Diabetes, Schlaganfälle, Herzfehler, Epilepsie oder Muskelschwäche ihren Ursprung in einem mitochondrialen Defekt haben. Mitochondriale Erbkrankheiten sind bis dato unheilbar. Deshalb liegt nun der Fokus darauf, den betroffenen Frauen mittels Kerntransfer gesunden Nachwuchs zu ermöglichen.
Mitochondrien vermehren sich unterschiedlich schnell
Jörg Burgstaller, Wissenschafter in der Forschungsgruppe von Gottfried Brem an der Vetmeduni Vienna, beschäftigt sich seit Jahren mit der Genetik von Mitochondrien. Es war bekannt, dass sich unterschiedliche Mitochondrientypen innerhalb einer Zelle unterschiedlich schnell vermehren können. Allerdings wusste man bisher nicht, ob dieses Phänomen nur in Einzelfällen vorkommt oder häufiger auftritt. Genau das untersuchte Burgstaller in Mäusen. Dazu züchtete er vier Mausmodelle, in deren Zellen sich ein Gemisch aus genetisch unterschiedlich eng verwandten mtDNAs befanden. Für die Mäuse ist dies gesundheitlich kein Problem, da alle mtDNAs voll funktionsfähig waren.
Das Ergebnis: Je entfernter verwandt zwei Mitochondrientypen innerhalb einer Eizelle waren, desto häufiger kam es zu einem Wachstumsvorteil für einen der beiden Typen. Befanden sich also zum Zeitpunkt der Geburt zwei sehr unterschiedliche mtDNAs in den Zellen einzelner Organe, war nach einiger Zeit fast nur noch einer der beiden Typen nachweisbar. Eine Mitochondrien-Variante verdrängte also die andere. Bei eng verwandten Mitochondrientypen innerhalb der Zellen gab es diesen Effekt kaum; das Verhältnis der beiden Mitochondrientypen änderte sich nicht.
Effekt hat Auswirkungen auf die Fortpflanzungsmedizin
Burgstallers Ergebnisse haben möglicherweise Auswirkungen auf die in Großbritannien geplante Einführung des sogenannten „Three-parent baby“, zu Deutsch „Drei-Eltern Baby“. Dabei entnehmen Fachleute den Zellkern einer menschlichen Eizelle, deren Mitochondrien einen Defekt haben und setzen ihn in eine Eizelle mit „gesunden“ Mitochondrien. Das daraus entstehende Kind hat drei Eltern, nämlich jene Mutter, deren Zellkern verwendet wird, die Mutter, deren Mitochondrien ins Spiel kommen und einen Vater, dessen Spermium die modifizierte Eizelle befruchtet.
Diese Methode birgt nun aber folgendes Problem: Bei jedem Zellkerntransfer wird eine kleine Menge defekter Mitochondrien in die gesunde Eizelle übertragen. „Bisher dachte man, dass diese minimale „Verunreinigung“ keine Folgen für das entstehende Kind hat. Unsere Erkenntnisse zeigen jedoch, dass der Effekt dramatische Auswirkungen auf die Gesundheit der Nachkommen haben kann. Sind nämlich die Mitochondrien der beiden Mütter zufällig genetisch sehr unterschiedlich, könnte es zu denselben Effekten wie im Mausmodell kommen“, so Burgstaller, der diese Theorie gemeinsam mit Co-Autorin Joanna Poulton, Professorin für Mitochondriale Genetik und Spezialistin für Mitochondriale Erkrankungen am John Radcliffe Hospital in Oxford, entwickelt hat. „Eine mtDNA könnte sich gegen die andere durchsetzen. Handelt es sich dabei um die defekte mtDNA, wäre der Nuzen der Therapie gefährdet.“
Die Lösung des „Drei-Eltern Baby“-Problems
Burgstaller und seine KollegInnen schlagen folgende Lösung für das Problem vor: Die mtDNA der beiden Mütter, also der Kern- und der Mitochondrienspenderin, sollte vorab analysiert und aufeinander abgestimmt werden. Die Forschenden sprechen von einem sogenannten „matching“ der Mitochondrientypen der beteiligten Mütter. Damit kann der Effekt der Verdrängung verhindert werden. In Zukunft könnte der beobachtete Effekt eventuell auch gezielt zur Verdrängung defekter mtDNA genutzt werden.