Comment l'ADN s'auto-organise dans l'embryon précoce
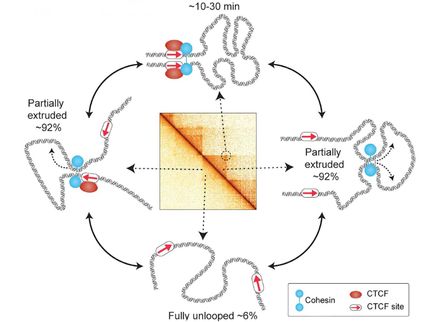
Une équipe de recherche internationale dirigée par Helmholtz Munich a, pour la première fois, donné un aperçu détaillé de la manière dont l'organisation spatiale du matériel génétique est établie dans le noyau cellulaire des embryons précoces au cours des premières heures suivant la fécondation. De manière surprenante, les embryons font preuve d'une grande souplesse pour répondre aux perturbations de ce processus. L'étude, qui vient d'être publiée dans Cell, révèle qu'aucun régulateur principal ne contrôle cette organisation nucléaire. Au contraire, de multiples mécanismes redondants assurent une architecture nucléaire robuste et adaptable, permettant aux embryons de corriger les erreurs dans l'organisation initiale de leur noyau.

Image symbolique
Computer-generated image
L'organisation précoce de l'ADN est robuste et flexible
Lorsque l'ovule et le spermatozoïde fusionnent, une réorganisation complète de l'ADN commence dans le noyau. L'épigénétique joue un rôle crucial dans ce processus, en régulant l'activité des gènes par des modifications chimiques de l'ADN et des protéines qui lui sont associées. "Nous voulions comprendre comment ces programmes épigénétiques influencent l'activité des gènes et garantissent que la cellule exécute correctement ses tâches de développement", explique la directrice de l'étude, le professeur Maria-Elena Torres-Padilla, directrice de l'Institut de l'épigénétique et des cellules souches à Helmholtz Munich et professeur à la faculté de biologie de l'université Ludwig-Maximilians (LMU). "Auparavant, on ne savait pas si un mécanisme central unique contrôlait l'organisation nucléaire après la fécondation. Nos résultats montrent qu'après la fécondation, de multiples voies de régulation parallèles contrôlent l'organisation nucléaire, en se renforçant mutuellement".
Remise en question du modèle classique d'organisation nucléaire
Pour décrypter les mécanismes de cette réorganisation, les chercheurs ont effectué un criblage de perturbations à moyenne échelle dans des embryons de souris. Pour cartographier les changements épigénétiques dans les embryons précoces, ils ont utilisé des techniques de biologie moléculaire de pointe (voir l'encadré ci-dessous). Les analyses ont mis en évidence de multiples mécanismes de régulation redondants impliqués dans l'organisation nucléaire.
En outre, les expériences ont révélé que, contrairement aux hypothèses antérieures, l'activité des gènes n'est pas strictement déterminée par le positionnement nucléaire. "La position des gènes dans le noyau n'est pas toujours en corrélation avec leur activité", explique Mrinmoy Pal, premier auteur de la publication et chercheur doctorant à l'Institut d'épigénétique et des cellules souches. Certains gènes sont restés actifs malgré leur déplacement vers une région nucléaire traditionnellement considérée comme inactive, tandis que des déplacements similaires dans d'autres cas ont conduit à une réduction drastique de l'expression des gènes. "Cela remet en question le modèle classique de l'organisation nucléaire et de la fonction du génome", conclut M. Pal.
Les embryons peuvent auto-corriger les erreurs précoces d'organisation nucléaire
Il est encore plus surprenant de constater que les embryons peuvent corriger eux-mêmes les perturbations de l'organisation nucléaire, même après la première division de l'œuf fécondé. Si l'organisation nucléaire a été perturbée avant la première division cellulaire, elle peut être rétablie au cours du deuxième cycle cellulaire. Cela suggère que les embryons précoces ne sont pas seulement résistants, mais qu'ils possèdent également des mécanismes pour compenser les erreurs dans leur organisation nucléaire initiale. Les chercheurs ont découvert que ce processus est régulé par des marques épigénétiques héritées de l'ovule maternel. Si ces signaux maternels sont perturbés, l'embryon peut activer d'autres programmes épigénétiques pour rétablir une organisation nucléaire correcte qui pourrait ne pas provenir de la mère. Cela indique que les embryons peuvent utiliser différents points de départ pour leur développement afin de prévenir les défauts de développement.
Pertinence pour le vieillissement et les maladies
Les résultats de l'étude pourraient avoir de vastes implications : dans des maladies telles que la progéria, une maladie génétique entraînant un vieillissement prématuré, des perturbations importantes se produisent dans l'ADN associé à la lamelle nucléaire. En outre, plusieurs cancers sont liés à des modifications de l'organisation du génome nucléaire. "Nos résultats pourraient aider à mieux comprendre ces mécanismes et, à long terme, à développer de nouvelles approches pour influencer spécifiquement les programmes épigénétiques afin d'améliorer les résultats des maladies", déclare Torres-Padilla.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.