Des capteurs pour les super-germes
Résistance aux antibiotiques
Les bactéries résistantes aux antibiotiques provoquent des infections parfois mortelles qui ne peuvent pratiquement plus être traitées avec les médicaments existants. Des maladies courantes comme les infections urinaires ou les plaies cutanées deviennent ainsi un risque médical. Les chercheurs de l'Empa travaillent donc sur des capteurs qui identifient rapidement les germes résistants et recommandent un traitement efficace.
La propagation de super-germes résistants aux antibiotiques plonge le domaine des soins dans une crise mondiale. On estime qu'en 2028, le nombre de victimes de bactéries multirésistantes sera aussi élevé qu'avant la découverte de la pénicilline 100 ans plus tôt, avec des coûts se chiffrant en milliards. L'Organisation mondiale de la santé (OMS) considère la « pandémie silencieuse » comme l'une des plus grandes menaces pour la santé mondiale.
L'apparition de résistances est favorisée par l'utilisation précipitée d'antibiotiques sans que l'agent pathogène sous-jacent n'ait été identifié au préalable. Ce n'est pas tout à fait incompréhensible, car : Le diagnostic à l'aide de méthodes longues et fastidieuses fait perdre un temps précieux, si bien que dans les situations d'urgence, on renonce souvent à attendre les résultats de laboratoire correspondants. Conséquence possible : un traitement reste inefficace et le risque de développement de résistances augmente. C'est pourquoi les chercheurs de l'Empa travaillent en collaboration avec des partenaires cliniques sur des outils de diagnostic innovants tels que des capteurs qui détectent plus rapidement les agents pathogènes résistants et permettent un traitement sur mesure en temps utile.
Un capteur s'allume en cas de pneumonie
Les bactéries multirésistantes sont particulièrement fréquentes dans les infections contractées à l'hôpital, comme la pneumonie. L'un des agents pathogènes pouvant déclencher une telle pneumonie est Klebsiella pneumoniae. Pour ce super-germe, la chercheuse de l'Empa Giorgia Giovannini du laboratoire « Biomimetic Membranes and Textiles » développe actuellement, en collaboration avec l'hôpital cantonal de Saint-Gall, un capteur qui émet une lumière fluorescente lorsqu'une infection à la Klebsiella est présente.
Le capteur réagit à l'uréase, une enzyme produite par les bactéries. Dans le projet « Doorstep », les chercheurs travaillent sur des particules de polymère qui entourent un colorant fluorescent. Si l'uréase bactérienne décompose le polymère, le colorant peut déployer sa luminosité. La méthode de diagnostic devrait fonctionner avec un frottis de gorge ou un échantillon de crachat. Cela permettrait de déterminer les agents pathogènes d'une pneumonie en quelques heures au lieu de plusieurs jours.
Un pansement avertit des germes de la plaie
Les plaies infectées constituent en outre un domaine d'application important pour un diagnostic rapide et précis des agents pathogènes résistants. Elles ne provoquent pas seulement des douleurs et des lésions tissulaires – elles sont aussi un foyer pour les super-germes résistants aux antibiotiques. Une équipe dirigée par les chercheurs de l'Empa Luciano Boesel et Giorgia Giovannini lance maintenant un projet en collaboration avec l'hôpital cantonal de Saint-Gall, dans lequel ils souhaitent développer un pansement multisensoriel pour les plaies. Ce pansement est basé sur des nanoparticules de silice intégrées dans un hydrogel résistant composé de polymères biocompatibles. La technologie des capteurs doit être intégrée directement dans le matériau du pansement. Les nanoparticules sont fonctionnalisées avec des substances qui peuvent indiquer spécifiquement les excrétions de certaines bactéries.
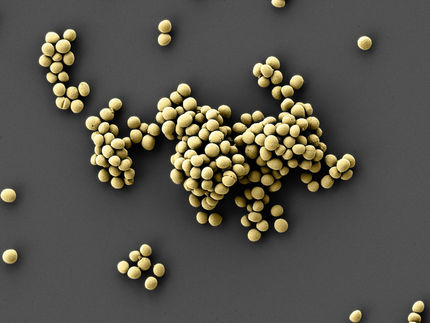
Ainsi, les capteurs doivent réagir aux germes particulièrement redoutables des plaies, comme le staphylocoque doré, et indiquer une modification de l'équilibre acido-basique dans la plaie. En outre, le risque de résistance aux antibiotiques doit être rapidement visible. Comme les germes hautement pathogènes des plaies disposent de l'enzyme bêta-lactamase, avec laquelle ils inactivent certains antibiotiques, le capteur contient des colorants qui sont décomposés par cette enzyme. Si des bactéries résistantes produisent l'enzyme dans la plaie, le capteur avertit en émettant une lueur claire sous la lumière UV. Dans le quotidien de la clinique, le capteur de plaie permet ainsi un diagnostic rapide et peu coûteux ainsi qu'un traitement personnalisé de la plaie. Le projet a été rendu possible grâce aux généreuses contributions de la Fondation Philipp et Henny Bender, de la Fondation Blumenau-Léonie Hartmann, de la Fondation Hans Groeber et de la Fondation Räschle.
Repêché dans l'urine
Pseudomonas aeruginosa est un autre représentant désagréable du règne bactérien. Cette bactérie en bâtonnet peut provoquer diverses maladies, dont des infections de l'appareil urinaire, par exemple via des sondes urinaires lors d'un séjour à l'hôpital. Et ces agents pathogènes sont également souvent résistants à divers antibiotiques. Une équipe de chercheurs de l'Empa et de l'ETH Zurich a donc mis au point un procédé utilisant des nanoparticules magnétiques pour détecter les bactéries de manière rapide et précise. Comme les particules magnétiques sont couplées à des composants protéiques qui réagissent exclusivement avec la pseudomonas aeruginosa, les cellules bactériennes peuvent finalement être « pêchées » spécifiquement dans l'urine via un champ magnétique.
L'étape suivante consiste à analyser la sensibilité des agents pathogènes à différents antibiotiques à l'aide d'un procédé de chimioluminescence. Si des bactéries résistantes sont présentes dans l'éprouvette, l'échantillon émet de la lumière. En revanche, si les germes peuvent être tués par des antibiotiques, il reste dans l'obscurité. « En tout et pour tout, le test de résistance dure environ 30 minutes – contre plusieurs jours pour une culture classique de bactéries », explique Qun Ren, chef de groupe au laboratoire « Biointerfaces » de l'Empa à Saint-Gall. Il est ainsi possible de déterminer en peu de temps l'antibiothérapie appropriée – et d'empêcher ainsi l'apparition de nouvelles résistances.
Publication originale
Fei Pan, Stefanie Altenried, Subas Scheibler, Alexandre H.C. Anthis, Qun Ren; "Specific capture of Pseudomonas aeruginosa for rapid detection of antimicrobial resistance in urinary tract infections"; Biosensors and Bioelectronics, Volume 222
Werner C. Albrich, Christian R. Kahlert, Susanne Nigg, Luciano F. Boesel, Giorgia Giovannini; "Fluorescent Probe for the pH-Independent Rapid and Sensitive Direct Detection of Urease-Producing Bacteria"; Analytical Chemistry, Volume 96, 2024-12-16