L'usine d'acides gras filmée au travail
Les images à haute résolution permettent de mieux comprendre la production cellulaire d'acides gras : un potentiel pour la médecine et la biotechnologie
Les acides gras sont essentiels à tous les organismes vivants : pour stocker l'énergie, former les membranes et se multiplier. Ils sont produits par une machinerie cellulaire complexe, la synthase des acides gras (FAS). Une équipe de l'Institut Max Planck (MPI) pour les sciences multidisciplinaires, dirigée par Ashwin Chari et Holger Stark, vient de visualiser la structure de la FAS avec un niveau de détail sans précédent. Cela permet d'observer directement les réactions enzymatiques et de reconstruire les transitions structurelles au sein d'un cycle de synthèse des acides gras. Ces découvertes ouvrent de nouvelles voies pour lutter contre les agents infectieux et promettent des avancées dans le domaine de la biotechnologie.
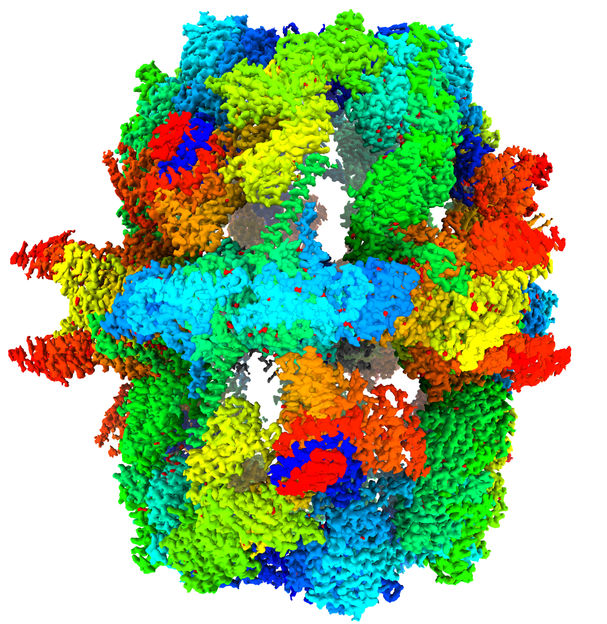
L'image montre la structure de l'acide gras synthase de la levure à une résolution de 1,9 angström. La carte de cryo-microscopie électronique est représentée en surface.
© Ashwin Chari / Max Planck Institute for Multidisciplinary Sciences

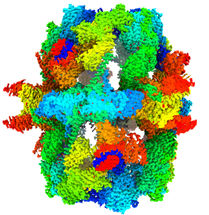
La carte de cryo-microscopie électronique à une résolution de 1,9 angström permet de visualiser de nombreux détails moléculaires au sein de l'acide gras synthase. L'usine moléculaire d'acides gras est représentée en gris-bleu transparent, les points rouges à l'intérieur de la synthase d'acides gras représentent des molécules d'eau modélisées et structurées.
© Ashwin Chari / Max Planck Institute for Multidisciplinary Sciences

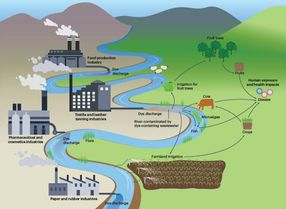
L'homme ingère généralement la plupart des acides gras dont il a besoin par le biais de son alimentation. Néanmoins, la biosynthèse des acides gras est une voie métabolique vitale. Pour les levures et les bactéries, elle est même indispensable. Chez les levures et les organismes supérieurs, la biosynthèse des acides gras est catalysée par de grands complexes multimériques de différentes enzymes, alors que les homologues bactériens sont représentés par des protéines individuelles. Bien que l'architecture de la machinerie de biosynthèse des acides gras varie considérablement d'un organisme à l'autre, les réactions catalysées et les modules enzymatiques individuels se ressemblent.
Un aperçu détaillé de la structure et de la chimie de la fabrique d'acides gras
Les équipes Max Planck dirigées par Holger Stark, chef du département de dynamique structurelle, et Ashwin Chari, chef du groupe de recherche sur la biochimie structurelle et les mécanismes, ont maintenant résolu la structure tridimensionnelle du FAS de la levure, pour la première fois, à une résolution sans précédent : 1,9 angström, soit 19 millions de fois plus petit qu'un millimètre. "En biologie structurale, il est essentiel de dépasser la barrière des deux angströms pour comprendre la chimie cellulaire", explique le directeur de Max Planck. "Nous révélons les parties les plus intimes du SAF et pouvons observer à la fois les réactions enzymatiques et les détails chimiques de l'interaction entre les protéines et les petites molécules.
La combinaison de la biochimie et de la cryo-microscopie électronique à haute résolution a été déterminante pour le succès des scientifiques de Göttingen. Pour leurs expériences, ils ont utilisé le microscope électronique à la plus haute résolution du monde, capable de résoudre les atomes individuels d'une protéine.
Visualiser le SAF avec une grande précision n'est cependant pas suffisant pour comprendre sa fonction. À l'instar de son homologue humain, le FAS fongique synthétise des acides gras en sept étapes réactionnelles individuelles en utilisant des précurseurs chimiques définis de manière cyclique et répétitive. Chaque étape chimique est réalisée par un module enzymatique distinct au sein du FAS. La chaîne d'acides gras en croissance doit donc être transportée d'un module enzymatique à l'autre dans une séquence efficace et ordonnée. Une navette moléculaire - la protéine porteuse d'acyle (ACP) - s'acquitte de cette tâche importante et orchestre la chorégraphie des réactions chimiques nécessaires à la biosynthèse des acides gras.
Observer la navette moléculaire en action
Les équipes de Stark et Chari ont également pu filmer la FAS en action et reconstituer un cycle complet de biosynthèse des acides gras. Pour ce faire, les chercheurs ont utilisé une combinaison de méthodes pour suivre l'ACP dans le labyrinthe du FAS. Dans un premier temps, ils ont lancé la biosynthèse des acides gras dans une éprouvette et arrêté son activité en congelant rapidement les molécules de FAS après différentes périodes de temps. Cela a permis d'arrêter le FAS dans des états distincts de la biosynthèse des acides gras. Le cryo-microscope électronique a ensuite permis d'obtenir des images instantanées du cycle du FAS. "Trouver la combinaison et les quantités précises de substrats pour arrêter le FAS à des points critiques du cycle de production a constitué un défi technique majeur", explique le chef du groupe de recherche, M. Chari. "Nous ne pouvons reconstruire l'ensemble du cycle de biosynthèse des acides gras que si toutes les transitions pertinentes sont visualisées et décrites avec précision par des modèles."
L'étape suivante a été l'élucidation assistée par ordinateur des structures tridimensionnelles des SAF. Kashish Singh, premier auteur de l'article publié dans la revue Cell, explique cette procédure complexe : "Nous avons développé des procédures de traitement d'images qui décomposent le FAS en compartiments fonctionnels individuels. Nous avons ensuite trié les structures de manière à ce que la séquence d'images représente un cycle de biosynthèse des acides gras. Grâce à ces instantanés, nous avons finalement pu suivre la manière dont la petite molécule ACP interagit avec certains sites du FAS et d'autres molécules au cours de la production d'acides gras."
Potentiel pour la médecine et la biotechnologie
Meina Neumann-Schaal, chef de département à l'Institut Leibniz German Collection of Microorganisms and Cell Cultures GmbH, rapporte que cette molécule présente également un intérêt médical : "L'ACP du FAS de la levure contient une région structurelle qui fait défaut à son homologue humain. Cette molécule constitue donc un point de départ prometteur pour l'inhibition des organismes pathogènes qui utilisent également le FAS de la levure. Il s'agit notamment de levures pathogènes telles que Candida albicans, qui infecte les muqueuses, ainsi que de mycobactéries, l'agent infectieux à l'origine de la tuberculose. Comme la tuberculose multirésistante constitue toujours un défi pour un traitement efficace, il y a un besoin urgent de nouveaux inhibiteurs.
Un autre résultat de la recherche pourrait être utilisé pour des avancées biotechnologiques. Les équipes de Chari et Stark ont apporté la preuve de concept que des modules enzymatiques supplémentaires peuvent être incorporés dans le FAS pour modifier son activité. "Dans le cadre d'une activité normale, le SAF produit un mélange d'acides gras à chaîne courte et longue. À l'avenir, un FAS personnalisé pourrait être utilisé pour produire des acides gras avec les longueurs de chaîne souhaitées", explique M. Chari. L'industrie chimique a besoin de ces acides gras pour produire, entre autres, des cosmétiques, des savons et des arômes. Ce sont également des éléments constitutifs des produits pharmaceutiques et des biocarburants. Les équipes de recherche de Göttingen voient également la possibilité de produire des acides gras de manière durable en utilisant des usines de biosynthèse de SAF spécifiquement modifiées, au lieu de les extraire du pétrole brut ou de l'huile de palme comme c'est le cas actuellement.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.