Comment lutter plus efficacement contre le cancer du sang ?
Plusieurs centaines de combinaisons de traitement différentes à tester simultanément à l'extérieur du corps
Malgré l'existence de traitements approuvés, le myélome multiple reste incurable. Des chercheurs de l'ETH Zurich et de l'hôpital universitaire de Zurich ont entrepris d'améliorer les résultats des traitements en testant des centaines de produits thérapeutiques existants à l'extérieur du corps afin de prédire leur efficacité.
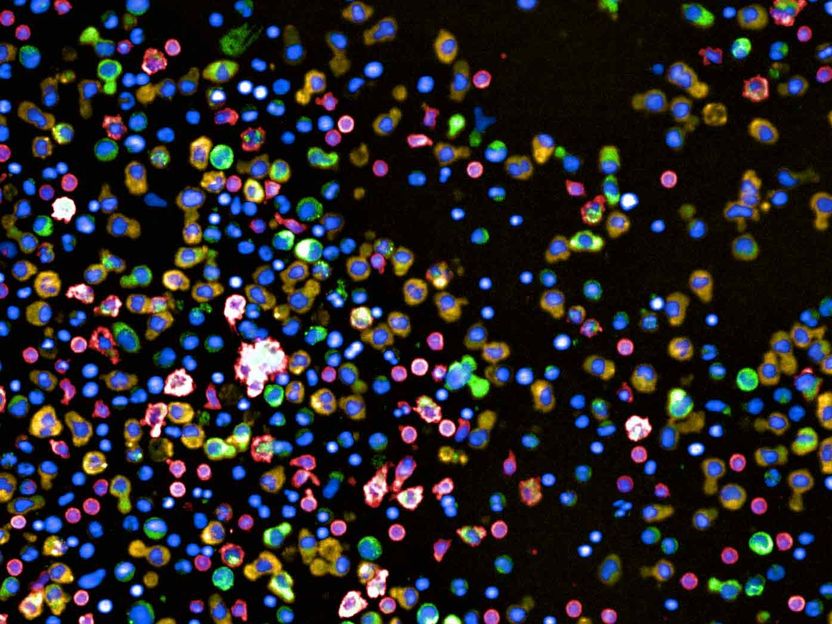
Cellules de moelle osseuse d'un patient atteint de myélome multiple. Les cellules rouges sont des monocytes sains, les cellules vertes et jaunes sont des cellules plasmatiques.
Berend Snijder Lab / ETH Zürich
Le myélome multiple est un cancer du sang rare causé par la multiplication incontrôlée de plasmocytes anormaux. Ces plasmocytes sont un type particulier de globules blancs qui jouent un rôle important dans le système immunitaire en produisant des anticorps essentiels dans la moelle osseuse et les ganglions lymphatiques.
Malgré un nombre croissant de médicaments approuvés et d'approches thérapeutiques telles que l'immunothérapie, la maladie n'est toujours pas guérissable. L'espérance de vie moyenne des patients après le diagnostic n'est que de cinq ans.
L'un des principaux défis à relever est la tendance du cancer à réapparaître même après un traitement. En effet, le traitement rend les cellules cancéreuses plus résistantes aux médicaments utilisés, jusqu'à ce que, après plusieurs séries de traitements, il n'y ait plus d'options efficaces.
Pour résoudre ce problème, les chercheurs de l'ETH ont adapté leur plateforme de dépistage afin de trouver des moyens de résoudre ce problème et d'offrir ainsi un nouvel espoir de traitement plus efficace.
Biopsies au microscope
Les chercheurs utilisent une méthode de dépistage à haut débit appelée pharmacoscopie, développée par le professeur Berend Snijder, pour tester l'efficacité de différents traitements sur les cellules cancéreuses du patient.
Cette méthode de pointe permet de tester simultanément plusieurs centaines de combinaisons de traitements différents à l'extérieur du corps. En analysant les réactions des cellules à chaque traitement, ils peuvent déterminer la méthode la plus prometteuse pour chaque patient.
Pour ce faire, les cellules des biopsies sont placées dans des plaques spéciales comportant 384 petits puits, chacun contenant une combinaison différente de substances thérapeutiques potentielles. Après 24 heures, les cellules sont colorées à l'aide de différents anticorps et leurs réactions sont évaluées à l'aide d'images générées par microscopie automatisée. Un algorithme d'apprentissage profond est ensuite utilisé pour identifier et classer les types de cellules. Le processus est largement automatisé, ce qui permet une analyse efficace et précise des résultats.
138 biopsies testées individuellement
Les chercheurs ont utilisé la pharmacoscopie pour examiner de près 138 biopsies de moelle osseuse provenant de 89 patients atteints de myélome multiple à différents stades, y compris des patients nouvellement diagnostiqués et non traités, ainsi que des patients ayant subi plusieurs cycles de traitement.
L'objectif était d'observer le comportement des cellules cancéreuses en réponse à divers médicaments et combinaisons de médicaments approuvés dans chaque biopsie. Sur la base de l'apparence des cellules, les chercheurs ont pu déterminer la meilleure option de traitement pour chaque patient.
Bien que le laboratoire de Snijder ait déjà utilisé la pharmacoscopie dans des études similaires sur d'autres types de cancer du sang, tels que les lymphomes et les leucémies, la plate-forme a dû être adaptée à cette étude sur le myélome.
L'espoir de traitements plus efficaces
Les travaux novateurs réalisés par les chercheurs de l'ETH et de l'hôpital universitaire de Zurich permettent d'espérer des traitements plus efficaces pour le myélome multiple. En utilisant la pharmacoscopie pour tester des centaines de traitements, les chercheurs ont pu identifier de nouvelles options thérapeutiques plus efficaces pour chaque patient.
Cette nouvelle approche de médecine personnalisée est transférable à la clinique et peut donc aider les médecins à trouver la meilleure option pour leurs patients à un stade précoce. "Toutefois, nous devrons d'abord valider la méthode dans le cadre d'essais cliniques", précise M. Snijder.
Le laboratoire Snijder souhaite à présent développer la plate-forme afin d'étendre son utilisation aux tumeurs solides. Contrairement aux cancers du sang, les tumeurs solides doivent d'abord être dissociées jusqu'à un certain point avant de pouvoir être testées dans le format de la plaque à 384 puits. Le laboratoire est en train d'adapter la plate-forme de dépistage aux tumeurs cérébrales, entre autres.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.