Microscaffolds - une nouvelle stratégie pour l'ingénierie tissulaire
Des cellules vivantes rencontrent un procédé d'impression 3D à haute résolution
Annonces
Jusqu'à présent, il existait deux approches complètement différentes pour produire des tissus artificiels. À la TU Wien, une troisième approche a été mise au point, qui combine les avantages des deux.
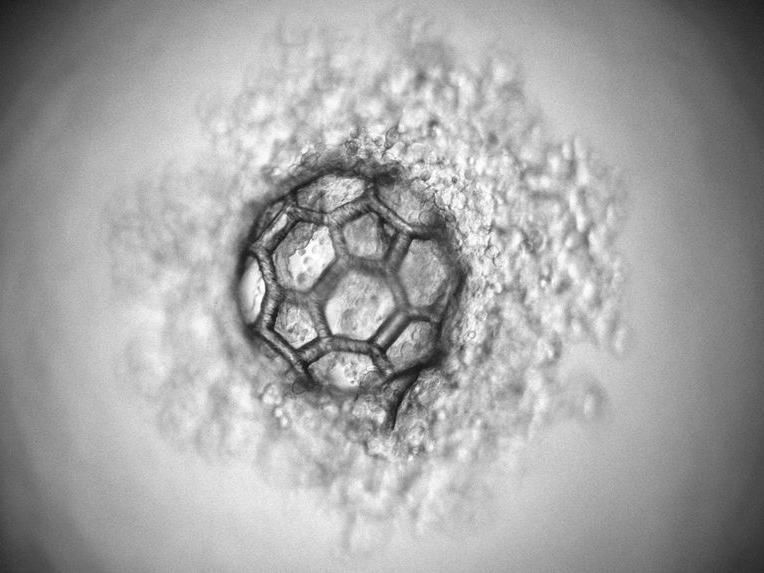
Le micro-échafaudage sous le microscope
Technische Universität Wien
C'est un vieux rêve de la médecine : s'il était possible de produire artificiellement des tissus de n'importe quel type à partir de cellules souches, les blessures pourraient être soignées avec les propres cellules du corps, et un jour il serait même possible de produire des organes artificiels. Cependant, il est difficile de donner aux cellules la forme souhaitée. Les méthodes qui ont existé jusqu'à présent peuvent être divisées en deux catégories fondamentalement différentes : Soit on crée d'abord de petits blocs de construction tissulaire, comme des agglomérats de cellules rondes ou des feuilles de cellules plates, puis on les assemble, soit on crée d'abord un échafaudage fin et poreux que l'on cultive ensuite avec des cellules. Les deux approches présentent des avantages et des inconvénients.
À la TU Wien (Vienne), une troisième approche a maintenant été développée : Une technique spéciale d'impression 3D au laser permet de produire des micro-échafaudages d'un diamètre inférieur à un tiers de millimètre, qui peuvent accueillir des milliers de cellules. De cette façon, une densité cellulaire élevée est présente dès le départ, mais on a toujours la possibilité d'adapter la forme et les propriétés mécaniques de la structure.
Avec ou sans échafaudage ?
"Les approches basées sur les échafaudages qui ont été développées jusqu'à présent présentent de grands avantages : Si vous fabriquez d'abord un échafaudage poreux, vous pouvez définir précisément ses propriétés mécaniques", explique le Dr Olivier Guillaume, auteur principal de l'étude actuelle, qui effectue des recherches à la TU Wien dans l'équipe du professeur Aleksandr Ovsianikov à l'Institut de science et de technologie des matériaux. "L'échafaudage peut être mou ou dur selon les besoins, il est constitué de matériaux biocompatibles qui se dégradent dans l'organisme. Ils peuvent même être équipés de biomolécules spéciales qui favorisent la formation de tissus."
L'inconvénient, cependant, est qu'il est difficile de peupler rapidement et complètement un tel échafaudage avec des cellules. Un travail manuel important est encore nécessaire aujourd'hui, même si des recherches sont déjà menées sur des processus automatisés. En particulier avec les grands échafaudages, il faut beaucoup de temps pour que les cellules migrent à l'intérieur de la structure ; souvent, la densité cellulaire reste très faible et inhomogène.
La situation est complètement différente si aucun échafaudage de ce type n'est utilisé. Il est également possible de cultiver simplement de petits agglomérats de cellules, qui sont ensuite assemblés selon la forme souhaitée, de sorte qu'ils finissent par fusionner. Avec cette technique, le nombre de cellules est important dès le départ, mais il n'y a pratiquement aucune possibilité d'intervenir dans le processus. Par exemple, il peut arriver que les sphères cellulaires changent de taille ou de forme et que le tissu se retrouve avec des propriétés différentes de celles souhaitées.
Des cellules vivantes et un procédé d'impression 3D à haute résolution
"Nous avons réussi à combiner les avantages des deux approches en utilisant une méthode d'impression 3D à très haute résolution sur laquelle nous menons des recherches depuis des années à la TU Wien", explique le professeur Aleksandr Ovsianikov.
Cette technique, la polymérisation à deux photons, utilise un matériau sensible à la lumière qui est durci par un faisceau laser exactement aux endroits souhaités. De cette façon, les structures peuvent être produites avec une précision de l'ordre de moins d'un micromètre.
Cette méthode laser est maintenant utilisée pour créer des échafaudages filigranes et très poreux d'un diamètre d'un peu moins d'un tiers de millimètre. La conception de ces micro-échafaudages permet de générer rapidement des agglomérats de cellules à l'intérieur. Dans le même temps, les cellules sont protégées des dommages mécaniques externes, de la même manière qu'un pilote de rallye est protégé par un arceau de sécurité pour voiture de course.
"Ces échafaudages remplis de cellules sont relativement faciles à manipuler et peuvent se coaliser", explique Aleksandr Ovsianikov. "Lorsque plusieurs d'entre eux sont mis en contact direct, il est possible de créer en peu de temps de grandes constructions tissulaires avec une densité cellulaire initiale élevée. Malgré tout, nous pouvons bien contrôler les propriétés mécaniques de la structure."
Le cartilage et l'os comme premiers tissus cibles
Le concept sous-jacent de cette nouvelle stratégie d'ingénierie tissulaire a déjà été présenté en détail par le groupe de recherche en 2018. Maintenant, pour la première fois, il a été possible de montrer que cette méthode fonctionne réellement : "Nous avons pu montrer que la méthode apporte réellement les avantages que nous espérions", explique Aleksandr Ovsianikov. "Nous avons utilisé des cellules souches pour nos expériences, qui peuvent être induites à produire du cartilage ou du tissu osseux. Nous avons pu montrer que les cellules des unités d'échafaudage voisines fusionnent effectivement et forment un seul tissu. Ce faisant, la structure conserve sa forme. À l'avenir, ces unités d'échafaudage pourraient même être rendues injectables pour être utilisées en chirurgie mini-invasive."
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.











































