Cómo reaccionan las biomoléculas a la luz ultravioleta
Un experimento innovador revela la dinámica ultrarrápida de las proteínas en su entorno
Anuncios
Un sofisticado experimento aporta nuevos conocimientos sobre la reacción ultrarrápida de las biomoléculas cuando reciben el impacto de la luz ultravioleta energética en su entorno natural. El equipo del científico del DESY Jochen Küpper registró los procesos inducidos por la luz que tienen lugar en un pequeño complejo de dos moléculas que sirvió como sistema modelo para las interacciones entre las proteínas y las moléculas de disolvente que las rodean, normalmente agua. El experimento es un paso importante en el camino hacia la grabación de una "película molecular" de este tipo de reacciones químicas, según informa el equipo en la revista Nature Communications. Küpper es el científico principal del DESY para la obtención de imágenes de moléculas controladas.
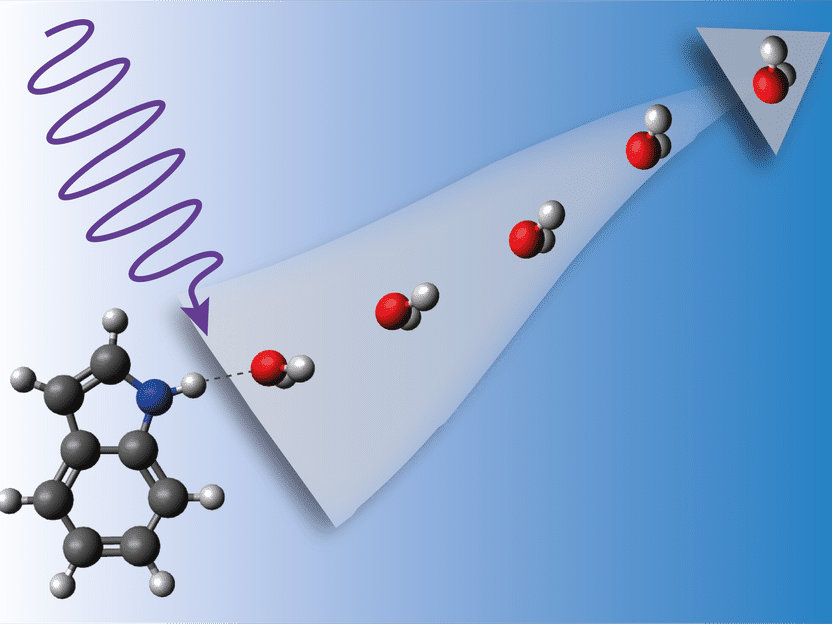
Cuando el complejo indol-agua es alcanzado por la luz ultravioleta, comienza a vibrar violentamente hasta que el agua se desprende.
Radboud-Universität, Jolijn Onvlee
"En nuestro organismo, las proteínas se encuentran generalmente en un medio acuoso, en el que cada una de ellas está rodeada de moléculas de agua", explica el autor principal, Jolijn Onvlee, que ahora trabaja como profesor adjunto en la Universidad Radboud de los Países Bajos. Las interacciones entre la proteína y las moléculas de disolvente (agua) que la rodean afectan al plegamiento de las proteínas y, por tanto, a su función. "En concreto, hemos estudiado la dinámica ultrarrápida inducida por la luz ultravioleta de modelos de proteínas en un entorno acuoso con un enfoque ascendente, utilizando un pequeño agregado del llamado cromóforo, una molécula que absorbe la luz y, por tanto, se excita, con una única molécula de agua unida", explica Onvlee.
Como sistema modelo, los científicos eligieron el compuesto aromático indol (C8H7N), que es el cromóforo del aminoácido triptófano y, por tanto, está presente en casi todas las proteínas. Para investigar las interacciones entre las proteínas y el disolvente que las rodea, los científicos unieron agua a las moléculas de indol. Sin embargo, el indol puede unirse a varias moléculas de agua. Para distinguir los compuestos de exactamente un indol y una molécula de agua, el equipo utilizó un deflector electrostático que dispersa los compuestos en distintas direcciones en función del número de moléculas de agua unidas.
Los científicos dispararon pulsos de un láser UV a los agregados de indol y agua. Estos agregados absorben la luz UV, tras lo cual se produce una dinámica compleja en escalas de tiempo de femtosegundos (cuatrillonésimas de segundo) y picosegundos (trillonésimas de segundo). Se utilizó un segundo láser para registrar los productos de reacción resultantes en un detector de imágenes. Cambiando el retardo entre los dos láseres, se podían tomar instantáneas de la dinámica ultrarrápida en diferentes etapas, revelando el curso de los acontecimientos. "Cuando la luz ultravioleta incide sobre el complejo, primero se produce la dinámica del estado excitado y, tras la relajación electrónica, el sistema empieza a vibrar enérgicamente", explica Küpper. "La molécula de indol se calienta totalmente". Finalmente, se desprende del agua.
"Gracias a la combinación del deflector electrostático y las imágenes resueltas en el tiempo, ahora podemos desentrañar estos procesos ultrarrápidos que tienen lugar en el complejo", dice Küpper. En última instancia, nos gustaría grabar una "película molecular" de resolución atómica en la que pudiéramos ver realmente la trayectoria del agua que abandona la molécula de indol. La presente investigación nos acerca un paso importante a la consecución de este objetivo."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Anuncios