Los fármacos caracterizados muestran efectos inesperados
Conocido y, sin embargo, inesperado: muchas sustancias activas influyen en la homeostasis del colesterol y, por lo tanto, posiblemente en una infección de SARS-CoV-2
Anuncios
Todo fármaco innovador comienza con la búsqueda de un principio activo que se dirija a los actores clave de los procesos relacionados con la enfermedad. Sin embargo, no existe un fármaco perfecto que afecte a la única diana del organismo: no hay efecto sin efectos secundarios, como también se describe en la mayoría de los prospectos de los medicamentos. Un grupo de químicos y biólogos dirigido por el profesor Herbert Waldmann y el doctor Slava Ziegler en el Instituto Max Planck de Fisiología Molecular de Dortmund ha combinado ahora diferentes estrategias para encontrar moléculas bioactivas y ha identificado un efecto inesperado para un grupo de sustancias activas ya caracterizadas: todas ellas modulan el metabolismo del colesterol, un problema casero, según parece.
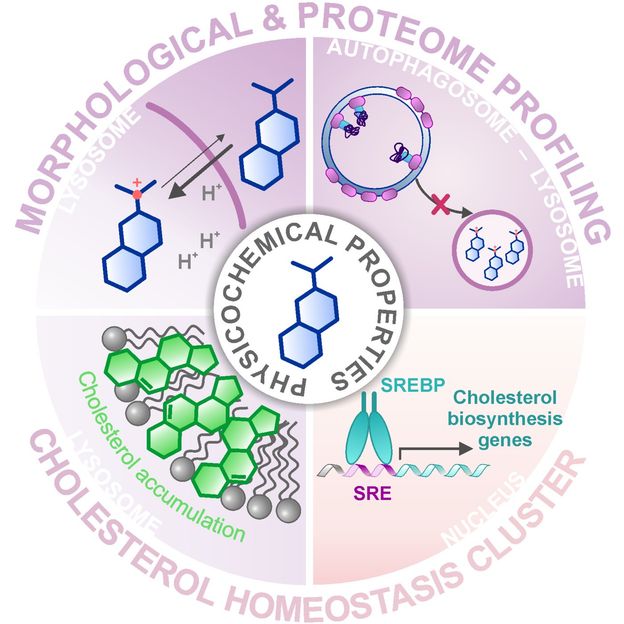
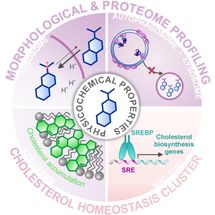
Aplicando el perfil morfológico y proteómico, se identificó un grupo de sustancias ya caracterizadas que modulan la homeostasis del colesterol.
MPI of Molecular Physiology
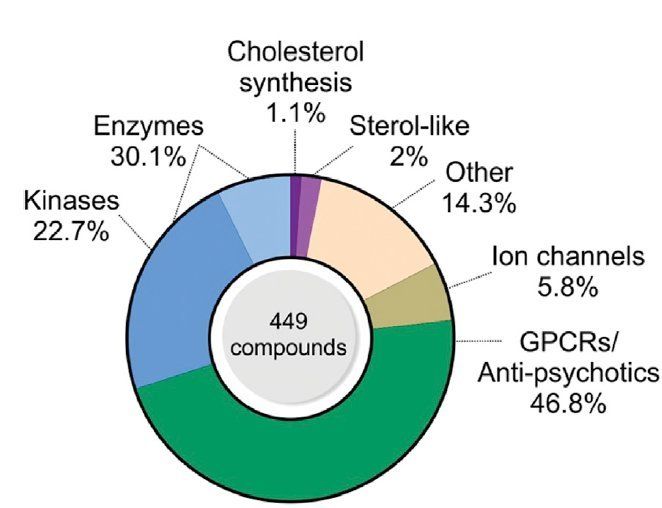
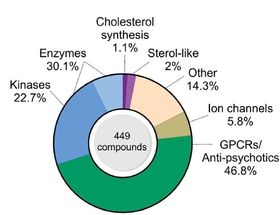
Cluster de bioactividad de 449 compuestos pertenecientes a diversas clases de objetivos identificados por el ensayo de pintura celular.
MPI of Molecular Physiology
Cuando Alexander Flemming descubrió en 1928 un moho en una placa de cultivo sobrecargada de bacterias, no esperaba encontrar uno de los principios activos más utilizados: la penicilina. Los descubrimientos accidentales y la identificación de principios activos de remedios tradicionales, como la morfina de la adormidera, han dado forma al descubrimiento de nuevos medicamentos durante mucho tiempo.
El descubrimiento moderno de medicamentos: del azar al sistema
Entretanto, se han producido importantes avances en química y biología molecular que permiten una búsqueda sistemática y selectiva de posibles sustancias activas en el descubrimiento moderno de fármacos. En primer lugar, los avances en el campo de la química orgánica y, sobre todo, en el de la química combinatoria, permitieron producir enormes bibliotecas de sustancias y comprobar su efecto farmacológico en pruebas de alto rendimiento. Los siguientes avances tecnológicos, como la secuenciación del genoma humano y el desarrollo de nuevos métodos de biología molecular, permitieron identificar los procesos celulares relacionados con las enfermedades y sus protagonistas moleculares. Esto allanó el camino hacia el descubrimiento moderno de fármacos, en el que se examinan grandes bibliotecas de moléculas de forma muy completa para comprobar su influencia en las moléculas objetivo relevantes, principalmente proteínas. Las sustancias identificadas, llamadas hits, se optimizan en su estructura química para dar lugar a estructuras que ya son eficaces en pequeñas dosis y se absorben y distribuyen bien en el organismo.
No hay efecto sin efectos secundarios
Este desarrollo de fármacos basado en dianas tiene mucho éxito a la hora de identificar nuevos candidatos a fármacos que impidan el funcionamiento de las proteínas objetivo o su interacción con otras proteínas. Sin embargo, los posibles fármacos candidatos rara vez son específicos y muy a menudo también actúan sobre proteínas relacionadas que tienen una función o estructura similar. "No es raro que un candidato a fármaco inicialmente prometedor muestre inesperadamente graves efectos secundarios en una fase posterior de su largo desarrollo, limitando o incluso impidiendo su uso clínico", afirma Slava Ziegler.
En busca de bioactividades desconocidas
Para rastrear los posibles efectos secundarios durante el desarrollo de un fármaco, los posibles candidatos a fármacos se examinan en ensayos para determinar su efecto sobre clases de proteínas conocidas, procesos biológicos y determinadas propiedades celulares. Sin embargo, estos ensayos sólo pueden reflejar la bioactividad esperada, ya que el número de moléculas diana conocidas en la célula es limitado. Los llamados enfoques de perfilado ofrecen ahora la posibilidad de detectar un espectro más amplio de actividad. Estas pruebas imparciales investigan la influencia sobre cientos de parámetros celulares o genéticos registrados en el perfil de una sustancia que se compara con los perfiles de sustancias de referencia con efectos conocidos.
Cuando los perfiles de los fármacos coinciden
En su último estudio, el grupo de Herbert Waldmann y Slava Ziegler combinó dos de estos enfoques de elaboración de perfiles para identificar sustancias bioactivas a partir de una biblioteca de unas 15.000 moléculas inspiradas en productos naturales y las comparó con los perfiles de compuestos activos conocidos. Aplicando el ensayo Cell Painting, en el que se tiñen áreas funcionales de la célula y luego se examinan al microscopio en busca de cambios, se identificó un gran grupo de sustancias con perfiles similares. Sin embargo, no fue posible predecir el modo de acción del clúster, ya que los compuestos de referencia asociados tenían diversas actividades o moléculas objetivo. Con una búsqueda posterior mediante perfiles del proteoma, en la que se examinaron las cantidades y, por tanto, la regulación de miles de proteínas, los investigadores pudieron reducir el clúster a una actividad común: la modulación de la homeostasis del colesterol, una actividad biológica inesperada para la mayoría de las sustancias de referencia del clúster.
Dos pájaros de un tiro: identificar nuevas bioactividades y efectos secundarios
Pero, ¿cómo es posible que sustancias con moléculas diana muy diferentes desencadenen el mismo efecto? Los investigadores revelaron que la mayoría de los compuestos del clúster se acumulan en el lisosoma, un orgánulo donde el colesterol se almacena temporalmente para su posterior función en la célula. El lisosoma tiene un valor de pH más bajo que el resto de la célula, y esto es crucial para el funcionamiento de las enzimas digestivas lisosomales que procesan las biomoléculas extrañas y las de la propia célula. En el lisosoma, las sustancias del clúster descrito aumentan el valor del pH y, por tanto, alteran la función de este orgánulo y, en particular, el equilibrio del colesterol de la célula. El hecho de que los compuestos se acumulen en el lisosoma no se debe a una molécula diana específica en el mismo, sino a sus propiedades químicas y físicas, que han obtenido gracias a su optimización estructural para mejorar la solubilidad.
"Curiosamente, la alteración del equilibrio del colesterol ya se ha relacionado con algunos fármacos comercializados, como los antipsicóticos", señala Tabea Schneidewind, primera autora del estudio. "Con la combinación de las dos estrategias de búsqueda, podemos matar dos pájaros de un tiro: desvelar efectos secundarios desconocidos e identificar nuevas sustancias activas y modos de acción", afirma Slava Ziegler.
Atacar la homeostasis del colesterol podría perturbar también las infecciones por el SARS-CoV-2
Influir en la homeostasis del colesterol parece ser una característica común de muchos compuestos y debería tenerse en cuenta al evaluar los efectos secundarios de las sustancias activas. Sin embargo, la actividad observada no es per se indeseable. En la actualidad, se están estudiando intensamente fármacos y compuestos con modos de acción conocidos para la inhibición de la infección del SARS-CoV-2 en las células huésped, y se han identificado muchos compuestos de nuestro grupo que suprimen este proceso. Curiosamente, el colesterol de la membrana y, por tanto, la homeostasis adecuada del colesterol son cruciales para la infección por Sars-CoV-2, como se ha demostrado en varios estudios. Nuestros datos explican muy probablemente la razón de la actividad de estos compuestos contra el virus: alteran la biosíntesis y la localización del colesterol en las células, lo que perjudica la infección por el Corona-Virus", afirma Slava Ziegler.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.