Salvar las células del hielo dañino
El hielo puede desgarrar las células en el crio-almacenamiento: Los polímeros pueden salvar el día
Anuncios
Las terapias celulares son muy prometedoras para revolucionar el tratamiento de los cánceres y las enfermedades autoinmunes. Pero esta industria multimillonaria requiere el almacenamiento a largo plazo de las células en condiciones criogénicas súper frías, mientras se asegura que seguirán funcionando al descongelarse. Sin embargo, estas frías temperaturas desencadenan la formación y el crecimiento del hielo, que puede perforar y desgarrar las células. Las investigaciones publicadas en el Journal of the American Chemical Society por los químicos de la Universidad de Utah Pavithra Naullage y Valeria Molinero proporcionan la base para diseñar polímeros eficientes que puedan prevenir el crecimiento de hielo que daña las células.

Imagen simbólica
Free-Photos, pixabay.com, CC0

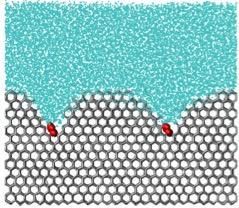
Una simulación de una molécula inhibidora de hielo. La molécula, en rojo, es como un peso en la superficie del cristal de hielo, curvándolo e impidiendo el crecimiento del cristal de hielo.
University of Utah

El anticongelante de la naturaleza
Las estrategias actuales para criopreservar las células y los órganos implican bañarlos con grandes cantidades de dimetilsulfóxido, una sustancia química tóxica que estropea la formación de hielo pero que estresa las células, disminuyendo sus posibilidades de supervivencia.
La naturaleza, sin embargo, ha encontrado una forma de mantener vivos a los organismos en condiciones de frío extremo: las proteínas anticongelantes. Los peces, insectos y otros organismos de sangre fría han desarrollado potentes glicoproteínas anticongelantes que se unen a los cristales de hielo y les impiden crecer y dañar las células.
El creciente ámbito de la terapéutica celular exige el desarrollo de potentes inhibidores de la recristalización del hielo que puedan competir en actividad con las glicoproteínas anticongelantes naturales pero que no tienen el costo y la toxicidad del dimetilsulfóxido. Esta demanda ha impulsado la síntesis de polímeros que imitan la acción de las glicoproteínas anticongelantes. Pero el inhibidor de recristalización del hielo sintético más potente encontrado hasta la fecha, el alcohol polivinílico (PVA), es un orden de magnitud menos potente que las glicoproteínas naturales.
"Los esfuerzos para identificar inhibidores más fuertes para el crecimiento del hielo parecen haberse estancado, ya que todavía no hay una comprensión molecular de los factores que limitan la eficiencia de la inhibición de la recristalización del hielo de los polímeros", dice Molinero.
Una variable de diseño de polímero oculta
¿Cómo evitan las moléculas que los cristales de hielo se hagan más grandes? Las moléculas que se unen fuertemente al hielo fijan su superficie - como piedras en una almohada - haciendo que el frente de hielo desarrolle una superficie curva alrededor de las moléculas. Esta curvatura desestabiliza el cristal de hielo, deteniendo su crecimiento. Las moléculas que permanecen unidas al hielo durante tiempos más largos que el tiempo que tardan en crecer los cristales de hielo consiguen evitar un mayor crecimiento y recristalización.
Molinero y Naullage utilizaron simulaciones moleculares en gran escala para dilucidar los fundamentos moleculares de cómo la flexibilidad, la longitud y la funcionalización de los polímeros controlan su unión al hielo y su eficiencia para evitar el crecimiento del hielo. Su estudio muestra que el tiempo de unión de las moléculas en la superficie del hielo está controlado por la fuerza de su unión al hielo junto con la longitud del polímero y la rapidez con que se propagan en la superficie del hielo.
"Encontramos que la eficiencia de los polímeros flexibles para detener el crecimiento del hielo está limitada por la lenta propagación de su unión al hielo", dice Molinero.
El estudio disecciona los diversos factores que controlan la unión de los polímeros flexibles al hielo y que explican la brecha en la potencia del PVA y las glicoproteínas anticongelantes naturales. En resumen, cada bloque de glicoproteínas anticongelantes se adhiere más fuertemente al hielo que el PVA, y también se ven favorecidas por su estructura molecular secundaria que segrega los bloques aglutinantes y no aglutinantes para permitirles adherirse más rápidamente al hielo y detener su crecimiento.
"Hasta donde sabemos, este trabajo es el primero en identificar el tiempo de propagación de la unión como una variable clave en el diseño de polímeros flexibles eficientes de unión al hielo", dice Naullage. "Nuestro estudio prepara el escenario para el diseño de novo de polímeros flexibles que pueden cumplir o incluso superar la eficiencia de las glicoproteínas anticongelantes y tener un impacto en la investigación biomédica".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.








































