Descoberta a função de um bloco de construção do VIH anteriormente misterioso
Investigadores obtêm novos conhecimentos sobre a forma como a camada de matriz do VIH-1 amadurece
Os investigadores do Instituto Max Planck de Bioquímica descobriram o mecanismo subjacente a uma etapa importante do ciclo de vida do VIH. Em colaboração com equipas das Universidades de Heidelberg e Yale, descobriram que o enigmático "péptido espaçador 2", um dos componentes virais, desempenha um papel fundamental na conversão de partículas imaturas do VIH-1 em partículas infecciosas. Os resultados do estudo foram publicados na revista Nature .
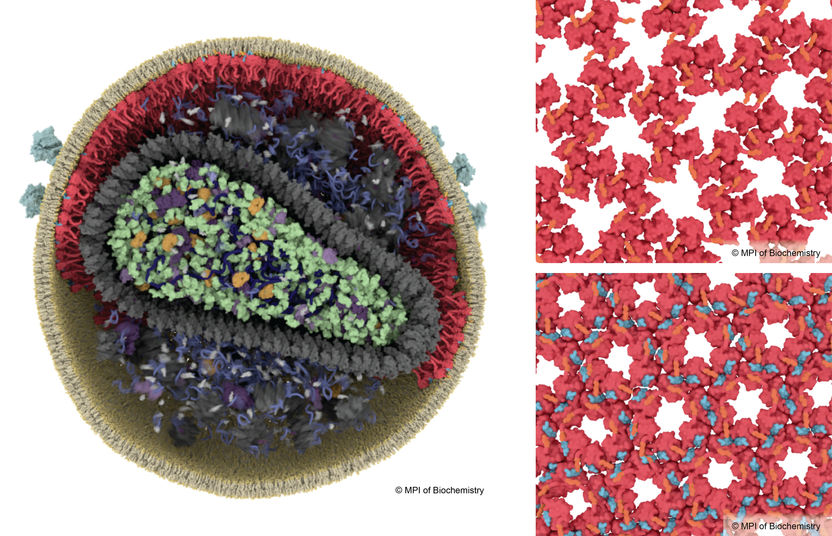
Para que o VIH se torne infecioso, tem de passar por um processo de maturação. No VIH imaturo, as proteínas da matriz (vermelho) formam uma rede solta (em cima à direita), enquanto no VIH maduro a formação de uma rede estável é desencadeada pela proteína SP2 (azul, em baixo à direita).
Margot Riggi, MPI of Biochemistry
As partículas do VIH-1 (vírus da imunodeficiência humana) são libertadas das células infectadas numa forma imatura e não infecciosa. O principal material de construção de uma partícula de vírus são cerca de 2000 cópias de uma proteína longa e em forma de bastão chamada Gag. Para se tornar infecioso, o VIH tem de passar por um processo de maturação. Este processo envolve a protease do VIH-1 (uma enzima viral), que corta a Gag em seis proteínas mais pequenas, incluindo o capsídeo e as proteínas da matriz. Isto leva a um extenso rearranjo estrutural dos componentes do vírus.
Durante muitos anos, os cientistas têm investigado as transformações estruturais do capsídeo viral que envolve o genoma viral. Em contrapartida, sabe-se muito menos sobre a matriz viral - o invólucro proteico exterior diretamente por baixo da membrana lipídica que envolve o vírus. Os investigadores liderados por John Briggs, diretor e biólogo estrutural do Instituto Max Planck de Bioquímica, descobriram agora como as proteínas da matriz se reorganizam durante a maturação de uma partícula infecciosa.
Os investigadores utilizaram microscópios crio-electrónicos de última geração para visualizar as partículas do vírus e depois utilizaram a análise de imagens assistida por computador para criar modelos 3D muito detalhados das proteínas do vírus. Contrariamente às suas expectativas, descobriram que o rearranjo da matriz é desencadeado pelo "péptido espaçador 2", que se liga à matriz e a rearranja. O péptido espaçador 2 é outro dos seis blocos de construção que são produzidos pelo corte do Gag, mas cuja função era anteriormente desconhecida. Ao ligar o péptido espaçador 2 à proteína da matriz, o vírus pode fundir-se mais rapidamente com as células hospedeiras para ser infetado. O trabalho foi realizado em conjunto com parceiros da Universidade de Heidelberg e da Universidade de Yale, nos EUA.
John Briggs explica: "No nosso laboratório, obtivemos os primeiros dados estruturais sobre a matriz do vírus em 2021, mas não sabíamos o que causa a reestruturação da matriz à medida que o vírus amadurece. Neste novo estudo, produzimos vistas 3D muito mais detalhadas da camada da matriz, que foram importantes para compreender os processos de remodelação viral.
James Stacey e Dominik Hrebík, os dois primeiros autores do estudo, explicam as suas conclusões. James explica: "A matriz do vírus tem uma cavidade na sua forma madura. Sabíamos que algo se ligava aí, mas pensávamos que era uma molécula lipídica da membrana. Agora conseguimos demonstrar que se trata do péptido espaçador 2. Isto levanta a questão de saber se esta cavidade poderá ser um alvo para moléculas de fármacos no futuro". Dominik acrescenta: "Até agora, a função do péptido espaçador 2 não era conhecida. Graças à microscopia crioelectrónica de alta resolução, verificámos que este péptido se liga diretamente às proteínas da matriz após a sua libertação e une as proteínas no vírus maduro".
John Briggs resume: "O VIH-1 é provavelmente o vírus mais bem estudado, mas ainda há passos importantes na sua replicação que ainda não compreendemos".
Observação: Este artigo foi traduzido usando um sistema de computador sem intervenção humana. A LUMITOS oferece essas traduções automáticas para apresentar uma gama mais ampla de notícias atuais. Como este artigo foi traduzido com tradução automática, é possível que contenha erros de vocabulário, sintaxe ou gramática. O artigo original em Alemão pode ser encontrado aqui.
Publicação original
James C. V. Stacey, Dominik Hrebík, Elizabeth Nand, Snehith Dyavari Shetty, Kun Qu, Marius Boicu, Maria Anders-Össwein, Pradeep D. Uchil, Robert A. Dick, Walther Mothes, Hans-Georg Kräusslich, Barbara Müller, John A. G. Briggs; "The conserved HIV-1 spacer peptide 2 triggers matrix lattice maturation"; Nature, 2025-2-26