El equipo de reparación de Moss también trabaja en humanos
"Si pudiéramos corregir sitios defectuosos en el código genético con métodos de edición de ARN, esto también ofrecería potencialmente puntos de partida para el tratamiento de enfermedades hereditarias"
Para que todo funcione bien en las células vivas, la información genética debe ser correcta. Pero, por desgracia, los errores en el ADN se acumulan con el tiempo debido a las mutaciones. Las plantas terrestres han desarrollado un peculiar modo de corrección: no mejoran directamente los errores del genoma, sino que lo hacen de forma elaborada en cada transcripción individual. Investigadores de la Universidad de Bonn han trasplantado esta maquinaria de corrección del musgo Physcomitrium patens a células humanas. Sorprendentemente, el corrector empezó a funcionar también allí, pero según sus propias reglas. Los resultados se han publicado ahora en la revista "Nucleic Acids Research".
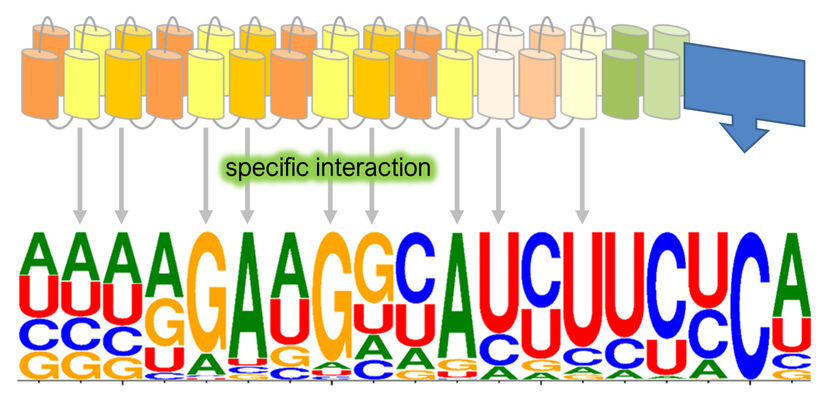
El editor PPR56, que sólo actúa en las mitocondrias del musgo, edita más de 900 posiciones diferentes en los transcritos nucleares de las células humanas.
Elena Lesch/University of Bonn
En las células vivas hay mucho tráfico, como en una gran obra de construcción: En las plantas terrestres, los planos en forma de ADN se almacenan no sólo en el núcleo celular, sino también en las centrales eléctricas de la célula (mitocondrias) y en las unidades de fotosíntesis (cloroplastos). Estos planos contienen las instrucciones de construcción de las proteínas que permiten los procesos metabólicos. ¿Pero cómo se transmite la información de los planos en las mitocondrias y los cloroplastos? Se hace creando transcripciones (ARN) de las partes deseadas del plano. Esta información se utiliza para producir las proteínas necesarias.
Los errores se acumulan con el tiempo
Sin embargo, este proceso no se desarrolla con total normalidad. Con el tiempo, las mutaciones han hecho que se acumulen errores en el ADN que deben corregirse para obtener proteínas que funcionen perfectamente. De lo contrario, el suministro de energía en las plantas se colapsaría. A primera vista, la estrategia de corrección parece bastante burocrática: en lugar de mejorar los deslices directamente en el plano -el ADN-, se limpian en cada uno de los numerosos transcritos mediante los llamados procesos de edición del ARN.
En comparación con la impresión tipográfica, sería como corregir a mano cada libro individual, en lugar de mejorar las planchas de impresión. "No sabemos por qué las células vivas hacen este esfuerzo", dice la Dra. Mareike Schallenberg-Rüdinger, del Instituto de Botánica Celular y Molecular (IZMB) de la Universidad de Bonn. "Presumiblemente, estas mutaciones aumentaron a medida que las plantas se extendieron del agua a la tierra durante la evolución".
En 2019, el equipo del IZMB dirigido por el Prof. Dr. Volker Knoop logró trasplantar procesos de edición de ARN del musgo Physcomitrium patens a la bacteria Escherichia coli. Se demostró que las proteínas de reparación del musgo también pueden modificar el ARN de estas bacterias.
Ahora, los investigadores del Instituto de Botánica Celular y Molecular, junto con el equipo dirigido por el Prof. Dr. Oliver J. Gruss, del Instituto de Genética de la Universidad de Bonn, han dado un paso más: Han transferido la maquinaria de edición de ARN del musgo a líneas celulares humanas estándar, incluyendo células renales y cancerosas, por ejemplo. "Nuestros resultados demostraron que el mecanismo de corrección de la planta terrestre también funciona en las células humanas", informa la primera autora, Elena Lesch. "Esto era desconocido hasta ahora".
Pero eso no es todo: las máquinas de edición de ARN PPR56 y PPR65, que sólo actúan en las mitocondrias del musgo, también introducen cambios de nucleótidos en los transcritos de ARN del núcleo celular en las células humanas.
Más de 900 objetivos
Sorprendentemente para el equipo de investigación, la PPR56 realiza cambios en más de 900 puntos de ataque en las dianas de las células humanas. En el musgo, en cambio, este corrector de ARN sólo es responsable de dos sitios de corrección". Hay muchos más transcritos de ARN nuclear en las células humanas que transcritos mitocondriales en el musgo", explica la Dra. Mareike Schallenberg-Rüdinger. "En consecuencia, también hay muchos más objetivos que los editores pueden atacar". Aunque los editores siguen un código concreto, en esta fase todavía no es posible predecir con exactitud dónde realizarán los cambios las máquinas de edición en las células humanas.
Sin embargo, la abundancia de objetivos de edición de ARN en las células humanas también ofrece la oportunidad de averiguar más sobre los mecanismos básicos de los correctores en estudios posteriores. Esto podría ser la base de métodos para inducir un cambio muy específico en el ARN de las células humanas mediante un corrector. "Si pudiéramos corregir sitios defectuosos en el código genético con métodos de edición de ARN, esto también ofrecería potencialmente puntos de partida para el tratamiento de enfermedades hereditarias", dice Schallenberg-Rüdinger, mirando hacia el futuro. "Queda por ver si eso funcionará".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.