Erlanger Forschung beschleunigt Analyse von Krebsgenen
Wissenschaftler des Universitätsklinikums Erlangen haben einen weltweit neuen Test entwickelt, mit dem die krebsfördernden Wirkungen von Genen schnell und in großer Zahl analysiert werden können. Die Erlanger Forscher konnten mit dem Test auf Grundlage der so genannten "systembiologischen Zellchip-Analyse" erstmals ein Virus entschlüsseln, das als Auslöser eines bösartigen Tumors - des Kaposi-Sarkoms - gilt.

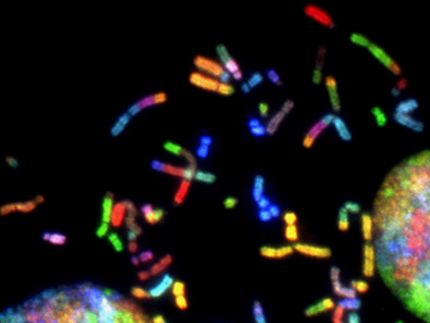
Virusersatzteillager auf Chip: mit der Zell-Chip-Technologie können auf der Fläche eines 50 Cent-Stücks 256 zu untersuchende Eiweiße geordnet wie in einem Ersatzteillager in Tumorzellen produziert werden. Bisher waren hierzu Kulturen auf einer Fläche notwendig, die mindestens der von zwei 100 Euro-Scheinen entsprach. Die mit der Zell-Chip-Analyse erreichte Kostenreduktion entspricht der Flächenreduktion. Demzufolge erlaubt diese neue Technologie wesentlich schneller und kostengünstiger die krankheitsrelevanten Funktionen von Genen zu bestimmen. Das Bild zeigt einen Fluoreszenznachweis der verschiedenen Eiweiße.
Experimentelle Chirurgie am Uni-Klinikum Erlangen
"Wir sind jetzt in der Lage, in kurzer Zeit sehr viele unterschiedliche Facetten der tumorigenen Wechelswirkungen eines Virus mit seiner Wirtszelle zu analysieren", sagte Prof. Dr. Stürzl aus der Abteilung Molekulare und Experimentelle Chirurgie der Chirurgischen Klinik des Uni-Klinikums Erlangen. Die systembiologische Zellchip-Analyse ist weltweit gegenwärtig nur noch an vier weiteren Forschungszentren in Heidelberg, Finnland, Japan und den USA möglich.
Das Forschungsergebnis der Erlanger Wissenschaftsarbeit ist jetzt im Journal of Virology erschienen. Der Herausgeber des Journals hebt den Erlanger Ansatz im Vorwort als "richtungsweisend für die Analyse der Wechselwirkung" von Viren mit Zellen hervor. "Wenn wir wissen, welche genetischen Bausteine Krebs begünstigen, sind wir dem Ziel sehr nahe, Krebs zu verhindern oder deutlich effektiver zu therapieren", sagte Prof. Stürzl.
Die Forschungsarbeit beschäftigt sich mit dem humanen Herpesvirus-8. Er ist Auslöser des Kaposi-Sarkoms, eines malignen Tumors, der vor allem in Zentralafrika sehr häufig auftritt. Bisher war nicht bekannt, welche der 86 bekannten Gene des Virus die Tumorentstehung steuern. Dies lag unter anderem daran, dass tumorigene Wirkungen oft auf dem Zusammenwirken mehrerer Gene beruhen und die hohe Zahl der hierfür notwendigen Untersuchungen mit herkömmlichen Verfahren nicht bewältigt werden kann.
Mit einem neuen systembiologischen Ansatz gelang es den Forschern der Abteilung Molekulare und Experimentelle Chirurgie in Zusammenarbeit mit einem Forschungsteam des Virologischen Instituts des Uni-Klinikums (PD Dr. Frank Neipel) erstmals alle Bestandteile des humanen Herpesvirus-8 einzeln und in unterschiedlichen Kombinationen auf einem einzigen Chip in eukaryontischen Zellen zur synthetisieren. Diese Zellchip-Analyse stellt nach Art eines Ersatzteillagers alle Komponenten des Virus bereit und ermöglichte die Durchführung von mehr als 14.000 Analysen zur Wirkung viraler Gene in eukaryontischen Zellen.
In Folge dieser Untersuchungen konnten zwei neue herpesvirale Regulatorproteine identifiziert werden, die eine wichtige Rolle bei der Entstehung des Kaposi-Sarkoms spielen könnten. Künftige Untersuchungen zielen darauf ab, die identifizierten Proteine als molekulare Angriffspunkte zur Behandlung des Kaposi-Sarkoms einzusetzen.
Originalveröffentlichung: Konrad et al.; Journal of Virology 2009, 83, 2563-2574
Meistgelesene News
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Antibody Stabilizer von CANDOR Bioscience
Protein- und Antikörperstabilisierung leicht gemacht
Langzeitlagerung ohne Einfrieren – Einfache Anwendung, zuverlässiger Schutz

DynaPro NanoStar II von Wyatt Technology
NanoStar II: DLS und SLS mit Touch-Bedienung
Größe, Partikelkonzentration und mehr für Proteine, Viren und andere Biomoleküle

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.