Metallorganische Verbindungen als neue Pharmaka?
Cobalthaltiger Aspirin-Komplex mit Antitumor-Potenzial
Trotz beachtlicher Fortschritte in der modernen Chemotherapie herrscht nach wie vor ein großer Bedarf an innovativen Antitumorwirkstoffen. Ein neuer Ansatz ist die Modulierung der pharmakologischen Eigenschaften etablierter Wirkstoffe durch metallorganische Fragmente. Wie ein Team von Wissenschaftlern aus Berlin, Bochum, Innsbruck (Österreich) und Leiden (Niederlande) in der Zeitschrift Angewandte Chemie berichtet, zeigen beispielsweise Cobalt-Aspririn-Komplexe ein interessantes Potenzial als Zytostatika.
Die meisten der heute verwendeten Arzneistoffe sind rein organische Verbindungen. Stimuliert durch den enormen Erfolg der anorganischen Verbindung Cisplatin in der Tumortherapie ist das Interesse an Metallkomplexen gestiegen. Metallkomplexe können in Zellen Reaktionen eingehen, die mit konventionellen organischen Substanzen nicht realisierbar sind.
Aspirin (Acetylsalicylsäure, ASS) zählt zur Gruppe der nichtsteroidalen Antirheumatika (NSAR), die v.a. entzündungshemmend und schmerzstillend wirken. Die pharmakologischen Effekte der NSAR beruhen auf der Hemmung von Enzymen der Cyclooxygenase-Famile (COX). Diese Enzyme spielen aber nicht nur eine zentrale Rolle bei Entzündungsprozessen, sondern scheinen auch beim Wachstum von Tumoren involviert zu sein. NSAR rücken damit als neuartige Zytostatika in den Blickpunkt. Die Antitumor-Wirkung ließe sich im Fall von Aspirin möglicherweise verbessern, indem es an ein metallorganisches Fragment gebunden wird.
Im Rahmen der durch die Deutsche Forschungsgemeinschaft (DFG) geförderten Forschergruppe „Biologische Funktion von Organometallverbindungen“ stellte das Team fest, dass „Co-ASS“, ein Hexacarbonyldicobalt-Aspirin-Komplex, die COX-Aktivität in anderer Weise inhibiert als Aspirin. Während die Wirkung von Aspirin auf der Acetylierung eines Serinrestes im aktiven Zentrum der COX beruht, greift Co-ASS diese Seitenkette nicht an, acetyliert dafür aber mehrere andere Stellen. Möglicherweise wird dadurch der Eingang zum aktiven Zentrum des Enzyms blockiert. Die Folge ist ein verändertes Wirkungsspektrum.
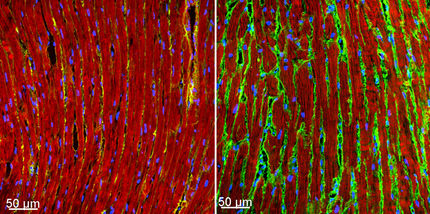
In Experimenten mit Zebrafischembryos konnte nachgewiesen werden, dass Co-ASS nicht nur das Zellwachstum, sondern im Gegensatz zu Aspirin auch die Entstehung kleiner Blutgefäße (Angiogenese) hemmt. Tumore sind auf eine Versorgung durch neugebildete Blutgefäße angewiesen und können durch eine Hemmung der Angiogenese regelrecht ausgehungert werden. Co-ASS moduliert zudem auch weitere tumorrelevante Stoffwechselwege. So wird durch den Komplex das Enzym Caspase aktiviert, das in Prozesse involviert ist, die zur Apoptose (programmierter Zelltod) führen.
Originalveröffentlichung: Ingo Ott et al.; "Modulierung der biologischen Eigenschaften von Aspirin durch Bildung eines Bioorganometallderivats"; Angewandte Chemie 2009, 121, No. 6, 1180–1184
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren
Pharmaceutical Substances von Thieme Verlag
Entdecken Sie industrielle Synthesewege für 2.600 APIs
Ihr Recherchetool für Synthesen, Patente und Anwendungen – Pharmaceutical Substances

KNAUER IJM NanoScaler von KNAUER
Effiziente Formulierung von Lipid-Nanopartikeln für RNA-basierte Therapien
Optimieren Sie die Wirkstoffverkapselung von 1 ml bis zu Hunderten von Millilitern mit minimalem Wirkstoffeinsatz

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.