Membranproteine künstlich hergestellt
Bakterielle Produktionsmaschinerie im Reagenzglas imitiert/Selektive Markierung großer Proteine für NMR
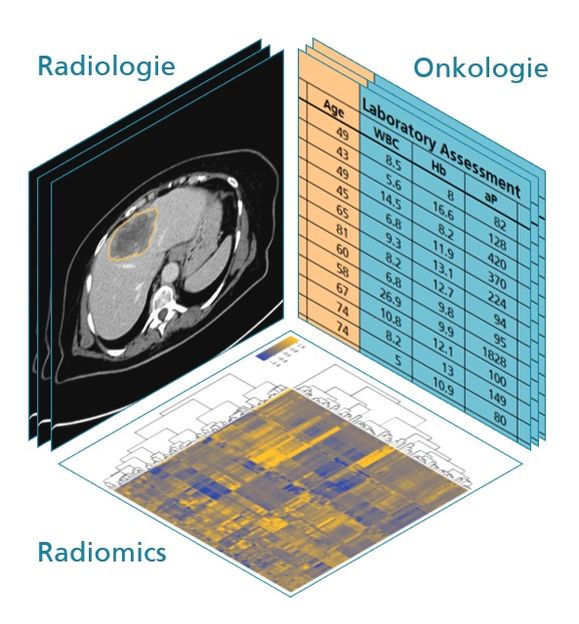
Die Proteine in Zellmembranen gehören, trotz ihrer großen Bedeutung als Schnittstelle zwischen der Zelle und ihrer Umgebung, zu den bisher am wenigsten erforschten Eiweißen. Der Grund dafür ist eine umhüllende Schicht aus Fettmolekülen sowie ihre Unlöslichkeit in Wasser. Beides erschwert ihre Untersuchung mit den bisher gebräuchlichen biophysikalischen Methoden. Insbesondere ist jedoch die Herstellung von Membranproteinen äußerst problematisch, denn man kann sie oft nicht, wie die wasserlöslichen Proteine, von Bakterien herstellen lassen. Biochemikern am Institut für Biophysikalische Chemie der Universität Frankfurt ist es nun gelungen, eine neue Methode zur Herstellung von Membranproteinen zu etablieren. Damit lassen sich die Eiweiße in genügend großen Mengen für eine Untersuchung herstellen. Die Frankfurter Forscher erwarten wichtige Impulse für die Pharmaforschung, denn etwa 60 Prozent aller Medikamente wirken auf Membranproteine.
Der Kern der Technik beruht auf dem Nachbau der bakteriellen Produktionsmaschinerie im Reagenzglas, wie die Forscher in den "Proceedings der National Academy of Sciences" berichten. Das als zellfreie Proteinsynthese bekannte Verfahren wurde bereits in den 1980er Jahren entwickelt, aber immer nur für wasserlösliche Eiweiße angewandt. Dr. Frank Bernhard vom Institut für Biophysikalische Chemie konnte nun zeigen, dass sich dieses Verfahren hervorragend zur Herstellung sehr vieler Membranproteine verwenden lässt. Die Methode erlaubt aber auch zusätzlich ganz neue Wege bei der Ermittlung der dreidimensionalen Struktur von Membranproteinen zu gehen. So haben Biophysiker in den Arbeitsgruppen von Prof. Volker Dötsch (Institut für Biophysikalische Chemie, Principal Investigator des Exzellenzclusters Macromolecular Complexes) und Prof. Peter Güntert (Institut für Biophysikalische Chemie und Frankfurt Institute for Advanced Studies, FIAS) ein neues Verfahren entwickelt, mit dessen Hilfe auch größere Membranproteine zukünftig leichter untersucht werden können.
Diese Methode beruht darauf, bestimmte Bereiche der Proteine für die Untersuchung mittels kernmagnetischer Resonanzspektroskopie (NMR) selektiv sichtbar zu machen. Voraussetzung hierfür ist der Einbau bestimmter NMR-aktiver Isotope. Das neu entwickelte Verfahren nutzt die große Flexibilität der zellfreien Proteinsynthese aus, nur bestimmte Bausteine der Eiweiße mit diesen NMR-aktiven Isotopen zu markieren, den Rest aber unmarkiert zu lassen. So lassen sich jetzt auch größere Membranproteine untersuchen, deren NMR Analyse bisher meist durch zu große Komplexität der Spektren behindert wurde. Mithilfe dieser Methode konnten nun erste Strukturinformationen eines Teils des Membranproteins Presenilin-1 erhalten werden, das eines der Schlüsseleiweiße bei der Entstehung der Alzheimerschen Krankheit ist. Weitere Anwendungen der entwickelten Technik auf die Strukturanalyse von zentralen Eiweißen aus dem menschlichen Herz-Kreislaufsystem werden derzeit am Institut für Biophysikalische Chemie erprobt.
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Antibody Stabilizer von CANDOR Bioscience
Protein- und Antikörperstabilisierung leicht gemacht
Langzeitlagerung ohne Einfrieren – Einfache Anwendung, zuverlässiger Schutz

DynaPro NanoStar II von Wyatt Technology
NanoStar II: DLS und SLS mit Touch-Bedienung
Größe, Partikelkonzentration und mehr für Proteine, Viren und andere Biomoleküle

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte
Brevetoxine
Spucke verrät, wie wir altern - Forscher hoffen, dass der Speichel dazu verwendet werden könnte, frühe Hinweise auf Gebrechlichkeit, Demenz und andere Gesundheitsprobleme zu liefern