Stress wirkt sich auf kleinster Zellebene aus: Neuer Steuermechanismus in P-Bodies entdeckt
Unterdrückung der Translation in menschlichen Zellen durch microRNA kann bei Stress wieder aufgehoben werden
In den Zellen ist die Boten-RNA dafür zuständig, die Bauanleitung für die einzelnen Proteine von der DNA im Zellkern zu den Ribosomen ins Zytoplasma zu transportieren, wo die Proteinsynthese stattfindet. Auf dem Weg vom Zellkern ins Zytoplasma kann die Boten-RNA durch sehr kleine RNA-Moleküle, sogenannte microRNAs, gebunden werden mit der Folge, dass die Proteinsynthese verhindert wird. "Wir haben bisher geglaubt, dass die Boten-RNA praktisch komplett ausgeschaltet wird und sozusagen stirbt, wenn microRNAs an sie bindet", erläutert Prof. Dr. med. Ellen Closs vom Institut für Pharmakologie der Johannes Gutenberg-Universität Mainz. Die Mainzer Zellforscher haben nun zusammen mit Kollegen aus Basel herausgefunden, dass dieser Prozess wider Erwarten umkehrbar ist und die Boten-RNA beispielsweise unter Stress wieder freigesetzt wird. Die Forschungsergebnisse wurden in Cell publiziert (Cell 125, 1111-1124, 2006).
Vor einigen Jahren haben Zellbiologen entdeckt, dass jede Zelle microRNAs enthält, die vermutlich zur Feinregulierung beispielsweise von Wachstumsprozessen dienen. "Die microRNA entscheidet, ob Boten-RNA tatsächlich in Proteine umgebaut wird", erklärt Closs. Die kleinen micro-RNA-Moleküle mit einer Länge von etwa 22 Basenpaaren agieren üblicherweise in "negativer" Form: sie docken an einer bestimmten Stelle der Boten-RNA an und verhindern dadurch den Translationsprozess, bei dem an den Ribosomen die Boten-RNA abgelesen und entsprechend dem genetischen Code die Proteine synthetisiert werden. Eine microRNA kann die Translation von zahlreichen - manchmal über 100 - Boten-RNAs unterdrücken und eine einzige Boten-RNA kann von mehreren micro-RNAs reguliert werden. Aktuelle Schätzungen gehen davon aus, dass ungefähr ein Drittel der menschlichen Gene der Steuerung durch microRNAs unterliegt - ein erstaunlich hoher Anteil.
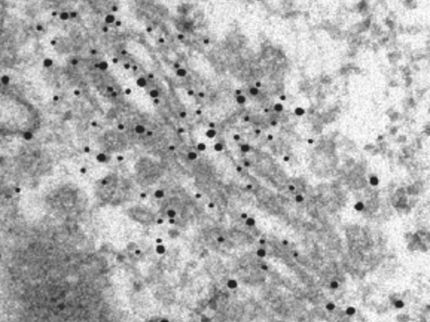
Was aber passiert mit der Boten-RNA, wenn sie "ausgeschaltet" wird? Nach bisherigen Erkenntnissen erfolgt ihre Stilllegung in einem bestimmten Bereich des Zytoplasmas, der als P-Body bezeichnet wird. In den P-Bodies - sie wurden vor drei Jahren entdeckt - wird nicht nur Boten-RNA abgebaut, um die Einzelteile später für den Aufbau von neuer Boten-RNA verfügbar zu haben, sondern Boten-RNA wird hier für die spätere Proteinsynthese auch zwischengelagert. Wie die Forschergruppen um Closs und Witold Filipowicz vom Friedrich Miescher Institute for Biomedical Research herausgefunden haben, sind die P-Bodies nicht Endstation für Boten-RNA, sondern im Gegenteil kann Boten-RNA aus einem P-Body wieder zur "aktiven Translationsgruppe" zurückkehren, wenn ein entsprechender Stimulus ergeht.
Die Untersuchungen dazu erfolgten anhand einer Boten-RNA, die für den Aminosäuretransporter CAT-1 kodiert, also die Struktur für den Aufbau dieses Transporters übermittelt. Diese Boten-RNA (CAT-1 mRNA) wird durch die microRNA miR-122 gesteuert. Die Autoren der Studie fanden heraus, dass die unterdrückte CAT-1 mRNA in P-Bodies gespeichert wird, unter Aminosäuremangel oder oxidativem Stress jedoch wieder entweichen kann. "Das ist eine völlig neue Erkenntnis: microRNA kann die Boten-RNA auch wieder loslassen", so die Mainzer Forscherin Ellen Closs. "Es gibt also einen Mechanismus, der in der Zelle vorliegt und unter bestimmten Situationen wieder reaktiviert werden kann. Das macht die gesamte Regulation durch microRNAs noch interessanter." Sie schließt dabei nicht aus, dass der entdeckte Prozess nicht nur für die CAT-1-Boten-RNA gilt und damit für die Steuerung des Transports der Aminosäure Arginin in die Leber- bzw. andere Körperzellen verantwortlich ist. "Vermutlich gilt der von uns entdeckte Ablauf auch für andere Boten-RNAs", so Closs. Die Hypothese soll später in weiteren Studien mit anderen Botenstoffen untersucht werden.
Meistgelesene News
Weitere News aus dem Ressort Wissenschaft
Diese Produkte könnten Sie interessieren

Antibody Stabilizer von CANDOR Bioscience
Protein- und Antikörperstabilisierung leicht gemacht
Langzeitlagerung ohne Einfrieren – Einfache Anwendung, zuverlässiger Schutz

DynaPro NanoStar II von Wyatt Technology
NanoStar II: DLS und SLS mit Touch-Bedienung
Größe, Partikelkonzentration und mehr für Proteine, Viren und andere Biomoleküle

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Ab sofort nichts mehr verpassen: Unser Newsletter für Biotechnologie, Pharma und Life Sciences bringt Sie jeden Dienstag und Donnerstag auf den neuesten Stand. Aktuelle Branchen-News, Produkt-Highlights und Innovationen - kompakt und verständlich in Ihrem Posteingang. Von uns recherchiert, damit Sie es nicht tun müssen.