Neues Diagnosetool optimiert artfremde Organtransplantationen
Diagnosetool optimiert artfremde Organtransplantationen
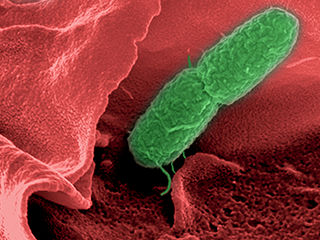
Zuckermoleküle stellen im Körper wichtige Signale mit einem hohen Informationsgehalt dar und sind an vielen biologischen Prozessen wie der Anheftung von Bakterien an Wirtszellen oder der Bildung von Biofilmen beteiligt. Die Rezeptoren, die diese Zucker erkennen können, sind spezielle Proteine – die Lektine. Forscher des Helmholtz-Instituts für Pharmazeutische Forschung Saarland (HIPS), einem Standort des Helmholtz-Zentrums für Infektionsforschung (HZI), haben jetzt ein besonderes Lektin beim Bakterium Photorhabdus luminescens identifiziert. Es hat eine besonders hohe Spezifität für die Zuckerstruktur „α-Gal“, die auf Zellen von Schweinen und Neuweltaffen gebildet wird.
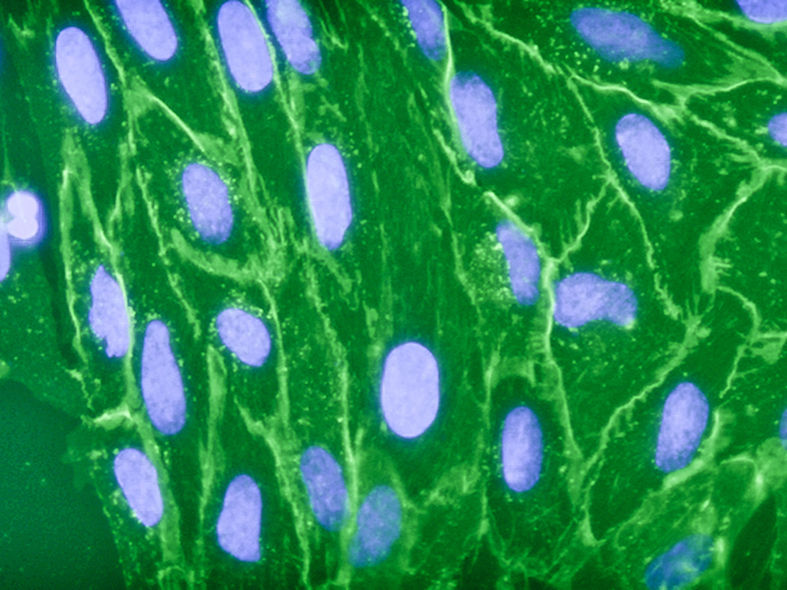
Flourescein-markierte Lektine erkennen Zucker auf Schweinezellen.
Beshr et al. 2017
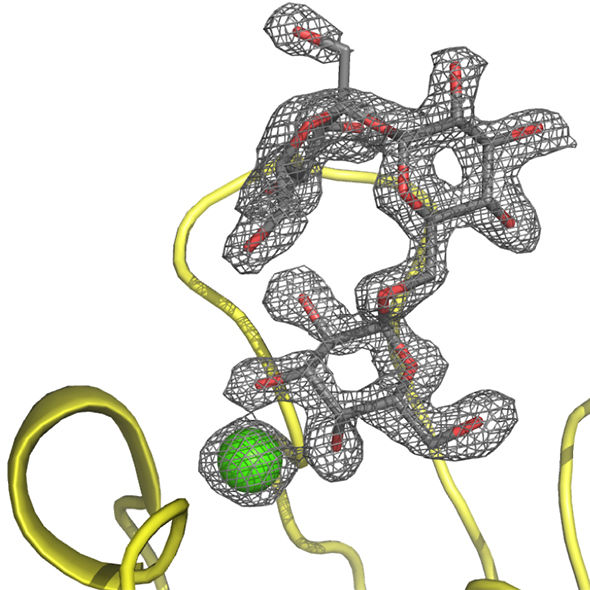
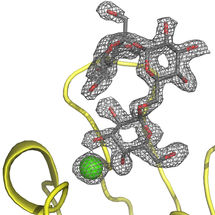
PIIA im Komplex mit dem Kohlenhydrat Raffinose.
Beshr et al. 2017
Die neuen Erkenntnisse haben eine große Bedeutung für Gewebetransplantationen vom Schwein auf den Menschen: Dafür müssen die transplantierten Zellen gentechnisch verändert werden, um eine heftige Immunreaktion auf α-Gal, das auch Xenoantigen genannt wird, zu vermeiden. Das neu entdeckte Lektin könnte zukünftig als Diagnosetool und zur Qualitätskontrolle eingesetzt werden.
Zuckererkennende Proteine, die Lektine, sind als Virulenzfaktoren bei zahlreichen Bakterien, wie den hartnäckigen Problemkeimen Pseudomonas aeruginosa, weit verbreitet. Sie erleichtern es den Mikroorganismen, sich an den Wirt anzuheften, um ihn zu infizieren. Dies motivierte Dr. Alexander Titz, der die Nachwuchsgruppe „Chemische Biologie der Kohlenhydrate“ des HZI und am Deutschen Zentrums für Infektionsforschung leitet, Lektine von verschiedenen Bakterien miteinander zu vergleichen: „Uns interessierte, ob es weitere Lektine bei anderen Bakterienarten mit einer hohen Spezifität für spezielle Zucker gibt.“ Dazu durchforsteten die Forscher um Titz Sequenzdatenbanken und suchten – ausgehend vom Lektin der Pseudomonaden – nach weiteren zuckerbindenden Proteinen. Sie wurden fündig: Eine sehr enge Sequenzhomologie der Proteine fanden sie beim Bakterium Photorhabdus luminescens.
Die Photorhabdus-Bakterien leben symbiotisch in Fadenwürmern und befallen größere Organismen. „Das Photorhabdus-Lektin weist überraschenderweise eine sehr hohe Spezifität für die Zuckerstruktur α-Gal auf, die bei Schweinen und Neuweltaffen zu finden ist“, sagt Alexander Titz. „Wir sind zwar fündig geworden, aber uns interessierte, wie das genau funktioniert.“
Licht ins Dunkel brachte die Kooperation mit Dr. Jesko Köhnke, Leiter der HIPS-Nachwuchsgruppe „Strukturbiologie Biosynthetischer Enzyme“. „Wir konnten die Kristallstruktur des neuen Lektins – gebunden an verschiedene Zucker – aufklären und damit seine Bindeeigenschaften verstehen“, sagt Köhnke.
Die Fragestellung der beiden Arbeitsgruppen, die sich eigentlich aus der Grundlagenforschung ergab, hat nun überraschenderweise zu einer sehr kliniknahen Anwendung als Diagnosetool geführt. Der spezielle Zucker α-Gal, den das Photorhabdus-Lektin erkennt, spielt eine wichtige Rolle bei Organtransplantationen von artfremden Geweben auf den Menschen.
Durch den Mangel an menschlichen Organspenden werden häufig auch Gewebe vom Schwein, zum Beispiel Herzklappen, transplantiert. Schweinezellen haben normalerweise α-Gal auf ihrer Oberfläche. Dies wird vom menschlichen Immunsystem erkannt und führt zu heftigen Abwehrreaktionen des Körpers. Durch moderne Methoden der Gentechnik sind Schweinezellen entstanden, die kein α-Gal mehr auf ihrer Oberfläche haben. Doch der Erfolg dieser Methoden muss überwacht werden: Als Qualitätskontrolle könnte in diesem Zusammenhang das Photorhabdus-Lektin eingesetzt werden, um zu kontrollieren, ob wirklich kein α-Gal mehr vorhanden ist. Bisher wurde dafür ein Agens der afrikanischen Pflanze Griffonia simplicifolia eingesetzt, welches allerdings kompliziert aus der Pflanze isoliert werden muss. Das hier neu beschriebene Lektin lässt sich vergleichsweise einfach und günstig herstellen und wurde zu diesen Zwecken erfolgreich von der Forschungsgruppe um Prof. Eckhard Wolf an der Tierärztlichen Fakultät der Ludwig-Maximilians-Universität München getestet.
Die HIPS-Forscher schließen auch einen breiteren Einsatz des Diagnosetools für α-galaktosylierte Zucker nicht aus. „Das ABO-Blutgruppensystem des Menschen ist ebenfalls über Zucker definiert. Hier könnte das Lektin von Photorhabdus auch als neues Typisierungssystem eingesetzt werden“, sagt Titz.