Kristalle im rosaroten Röntgenlicht
Proteinkristalle effizienter und schneller untersuchen
Ein neu entwickelter Versuchsaufbau ermöglicht die Röntgenstrukturanalyse von Biomolekülen wie beispielsweise Proteinen mit viel weniger Probenmaterial und kürzeren Belichtungszeiten als zuvor. Durch die Verwendung breitbandiger Röntgenstrahlung lassen sich Proteinkristalle an sogenannten Synchrotron-Strahlungsquellen erheblich effizienter und schneller untersuchen. Allerdings war dies bisher aufgrund der hohen Streustrahlung nur mit sehr großen Kristallen möglich. Mit dem neu entwickelten Versuchsaufbau, der die unerwünschte Streustrahlung erheblich reduziert, konnten Wissenschaftler nun erstmals das Verfahren der seriellen Kristallographie mit breitbandiger Synchrotronstrahlung durchführen. Das internationale Forscherteam unter Leitung von DESY-Wissenschaftler Alke Meents präsentiert die Ergebnisse in der Fachzeitschrift „Nature Communications“.

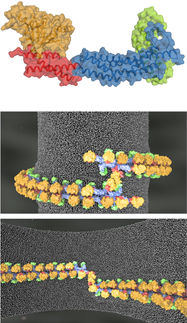
Der neu entwickelte Aufbau reduziert die störende Streustrahlung weitestgehend, indem der Pink-Beam-Röntgenstrahl durch dünne Metallröhrchen geleitet wird und so die Röntgenkamera vom Streulicht abschirmt. Zudem wird die Luft um die Probe zum großen Teil durch Heliumgas ersetzt.
DESY, Julian Bergtholdt

Beugungsbild eines Proteinkristalls mit polychromatischer Röntgenstrahlung. Im Vergleich zu Aufnahmen mit ‘einfarbigem’ monochromatischem Röntgenlicht enhält das Streubild viel mehr Information, und es werden dadurch viel weniger Kristalle für eine Strukturbestimmung benötigt.
DESY, Max Wiedorn
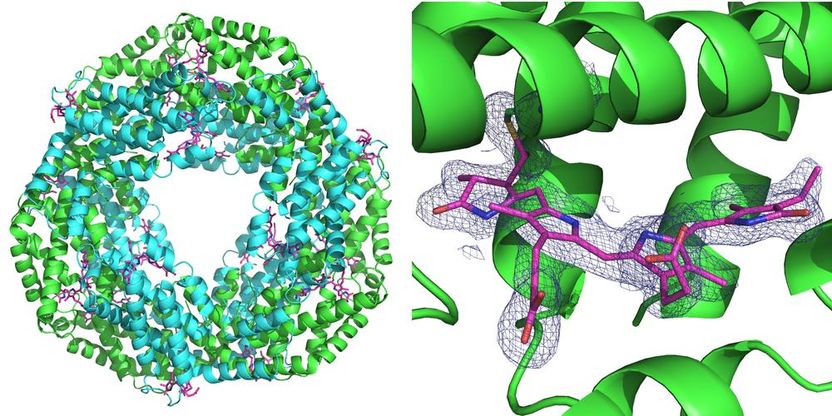
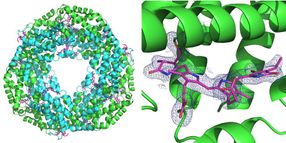
Links: Die biologisch aktive Struktur des untersuchten Proteins Phycocyanin, das unter anderem an der Photosynthese bei Blaualgen beteiligt ist, besteht aus einem Ring von sechs Doppelmolekülen (Heterodimeren). An jedes Heterodimer können drei Phycocyanobilin-Moleküle (pink) binden. Rechts: Das blaue Gitter repräsentiert die Elektronendichte eines Phycocyanobilin-Moleküls. Beide Strukturen wurden errechnet aus nur 52 Einzelbildern, aufgenommen mit dem Pink Beam der Advanced Photon Source (APS) an der BioCARS-Beamline. Die Daten haben eine Auflösung von 0,21 Nanometern (millionstel Millimetern).
DESY, Julia Lieske


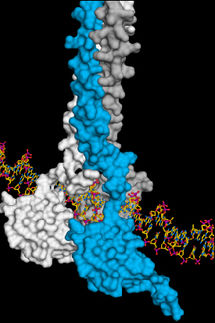
Die Röntgenkristallographie ist das „Arbeitspferd“ der Proteinstrukturanalyse: Für diese Technik werden Kristalle des zu untersuchenden Protein gezüchtet und dann mit Röntgenstrahlung – zum Beispiel aus einem Synchrotron – untersucht. Synchrotrone sind kreisförmige Teilchenbeschleuniger, die sehr helles Röntgenlicht erzeugen. Das Röntgenlicht wird von den Proteinkristallen auf charakteristische Weise abgelenkt, und aus dem resultierenden Beugungsmuster lässt sich die innere Struktur des Kristalls und damit des Proteins atomgenau berechnen.
Im Unterschied zur konventionellen Röntgenkristallographie, bei der meist ein einzelner oder relativ wenige große Proteinkristalle untersucht werden, durchleuchtet die serielle Kristallographie hundert bis hunderttausende sehr kleine Proteinkristalle. Die gewonnenen Informationen werden anschließend zu einem Datensatz zusammengesetzt, aus dem die Kristallstruktur bestimmt werden kann. An Röntgenlasern (XFELs) wird die Methode schon vielfach angewendet. Durch deren sehr kurze Röntgenblitze ist es dort zudem möglich, chemische und Enzym-Reaktionen zeitaufgelöst zu untersuchen.
„Serielle Kristallographie lässt sich auch gut an Synchrotronstrahlungsquellen anwenden. Allerdings dauern die Messungen hier durch die Verwendung von monochromatischem Röntgenlicht mit einer bestimmten Farbe und der daraus resultierenden geringeren Intensität der Röntgenstrahlung länger,“ erklärt Henry Chapman, leitender Wissenschaftler bei DESY und Koautor der Veroeffentlichung. Die Forscher verwenden also am Synchrotron üblicherweise nur einen kleinen Teil des erzeugten Lichts für die Untersuchung „Zudem werden für einen vollständigen Datensatz deutlich mehr Kristalle – oft mehrere zehntausend – benötigt. Da die Belichtungszeiten am Synchrotron relativ lang sind, konnten viele Reaktionen, die schnell ablaufen, bisher nur an Röntgenlasern zeitaufgelöst untersucht werden“, sagt Chapman.
Durch Verwendung des sogenannten Pink Beam lässt sich die serielle Kristallographie auch am Synchrotron mit sehr kurzen Belichtungszeiten umsetzen. Denn statt eines schmalen Wellenlängenbereichs wird hierbei polychromatische, also „mehrfarbige“ Röntgenstrahlung verwendet. Dieser Pink Beam enthält ein relativ breites Spektrum und ist dadurch viel intensiver. Mit dem Pink Beam lassen sich daher auch sehr schnelle Reaktionen an Synchrotronquellen untersuchen. Zudem lassen sich die Experimente wesentlich schneller durchführen, da durch die Verwendung des breiten Spektrums viel weniger Kristalle für eine Strukturbestimmung benötigt werden als bei der Verwendung vom monochromatischer Röntgenstrahlung mit nur einer „Farbe“.
Bisher konnten jedoch noch keine serielle Kristallographie mit dem Pink Beam durchgeführt werden, da bei diesen Untersuchungen die auftretende unerwünschte Streustrahlung die Messergebnisse erheblich beeinträchtigt hat. „Die Streustrahlung entsteht dadurch, dass das Röntgenlicht zur Untersuchung der Probe nicht nur von den Molekülen im Kristall, sondern auch am Probenhalter oder der Luft, die die Probe umgibt, gestreut wird“, erklärt Max Wiedorn, DESY-Koautor der Studie. „Bei Experimenten mit dem Pink Beam ist das eigentliche Messsignal schwächer, da es sich auf die verschiedenen ‚Farben’ verteilt. Daher hat der Streuuntergrund hier einen deutlich negativeren Effekt auf das Messergebnis als bei vergleichbaren Messungen mit monochromatischer Strahlung.“
Die Forscher haben daher einen neuen Messaufbau entwickelt, mit dem die störende Streustrahlung weitestgehend unterdrückt wird. Dazu verwenden sie einerseits einen Probenhalter aus Silizium, der das Röntgenlicht nicht störend streut, und sorgen andererseits dafür, dass sich extrem wenig Luft im Weg des Röntgenstrahls befindet. Unmittelbar vor und hinter der Probe wird der Röntgenstrahl dazu von einem dünnen Metallröhrchen umschlossen, das verhindert, dass die auftretende Streustrahlung auf die Röntgenkamera trifft. Zudem wird die Luft direkt an der Probe weitestgehend durch einen Strom von Heliumgas verdrängt, welches viel weniger Streustrahlung erzeugt als Luft. Durch die Unterdrückung der Streustrahlung ist es den Forschern nun erstmals gelungen, die dreidimensionale Struktur von zwei Proteinen mit serieller Kristallographie im Pink Beam sehr genau zu bestimmen. Die entsprechenden Messungen wurden an der BioCARS-Messstation an der Synchrotronstrahlungsquelle Advanced Photon Source (APS) in den USA durchgeführt.
„Ein großer Vorteil der Methode liegt darin, dass mit ihr sehr genaue Strukturuntersuchungen von Proteinen durchgeführt werden können, aber nur ein Bruchteil des Probenmaterials benötigt wird“, betont DESY-Forscher Meents vom Center for Free Electron Laser Science (CFEL), einer Kooperation von DESY, Universität Hamburg und der Max-Planck-Gesellschaft. „Andersherum lassen sich durch die sehr geringe benötigte Probenmenge und die Schnelligkeit der Methode sehr viele Untersuchungen in kurzer Zeit durchführen, wie zum Beispiel in der Pharmaforschung, wo untersucht wird, welche möglichen Wirkstoffe an ein Protein binden, das an einer Krankheit beteiligt ist.“
Zudem lassen sich die Messungen bei Raumtemperatur durchführen, wodurch sich strukturelle Änderungen, wie sie zum Beispiel bei der Bindung eines Wirkstoffs an ein Zielprotein auftreten, in Zukunft auch zeitabhängig untersuchen lassen. Dabei erreicht die neue Methode eine sehr hohe zeitliche Auflösung von 100 Pikosekunden (100 billionstel Sekunden), was mit der bisher eingesetzten monochromatischen Röntgenstrahlung am Synchrotron nicht möglich war.
An der Studie waren auch Forscher der Universität Hamburg, der Universität Chicago, der Medizinischen Hochschule Hannover, das Argonne National Laboratory und des BioXFEL Science and Technology Center der National Science Foundation in den USA beteiligt.
Originalveröffentlichung
"Pink-beam serial crystallography"; A. Meents, M.O. Wiedorn, V. Srajer, R. Henning, I. Sarrou, J. Bergtholdt, M. Barthelmess, P.Y.A. Reinke, D. Dierksmeyer, A. Tolstikova, S. Schaible, M. Messerschmidt, C.M. Ogata, D.J. Kissick, M.H. Taft, D.J. Manstein, J. Lieske, D. Oberthuer, R.F. Fischetti, H.N. Chapman; Nature Communications; 2017