Ausgründer entwickeln Medikamente gegen Alzheimersche Krankheit
Neuer Wirkmechanismus entwickelt
Die Entwicklung neuartiger Therapien und Medikamente zur Behandlung beispielsweise der Alzheimer-Krankheit ist der Schwerpunkt einer Ausgründung aus dem Forschungszentrum Jülich und der Heinrich-Heine-Universität Düsseldorf. Die Priavoid GmbH mit dem Gründer Prof. Dieter Willbold und seinem Team hat vor wenigen Tagen ihre Arbeit aufgenommen. Die Wissenschaftler haben einen Wirkstoffkandidaten zur Behandlung der Alzheimer-Krankheit entwickelt, zu welchem nun die präklinischen Tests abgeschlossen sind. Unterstützt wurden sie u. a. vom Forschungszentrum Jülich, dem Helmholtz Validierungs-Fonds, der Universität Düsseldorf und der Volkswagenstiftung.

Das Priavoid Gründungsteam mit Prof. Dieter Willbold (2. v.l.) und Dr. Ralph Zahn (2. v.r.).
Copyright: Forschungszentrum Jülich / Priavoid GmbH / Oleksandr Brener
Priavoid ist ein biopharmazeutisches Unternehmen, das sich auf die Entwicklung neuartiger Therapien für Patienten mit Erkrankungen des Zentralnervensystems konzentriert. Dabei stehen neurologische Erkrankungen im Fokus, die von fehlgefalteten und aggregierten Proteinen verursacht werden.
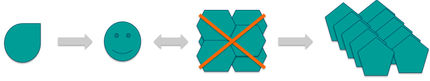
Die Alzheimer-Krankheit tritt auf, wenn harmlose Proteinmoleküle, sogenannte Monomere, zu schädlichen toxischen Oligomeren verklumpen, die die Verbindungen zwischen Nervenzellen und letztlich auch die Nervenzellen selbst schädigen. Die Monomere werden ständig im Menschen produziert, ohne zur Krankheit zu führen. Die toxischen Oligomere bilden sich selten und zufällig, doch über längere Zeiträume mit immer höherer Wahrscheinlichkeit. Das ist vermutlich der Grund, warum das Alter eines Menschen der größte Risikofaktor für Alzheimer ist.
Priavoid hat einen Wirkstoffkandidaten zur Behandlung der Alzheimer-Krankheit entwickelt, welcher alle erforderlichen präklinischen Sicherheits- und Toxizitätstests absolviert hat und nun vor einer Zulassung für die "Klinische Phase-I" steht. In dieser Phase wird das Medikament an gesunden Freiweilligen getestet, um es auf unerwünschte Nebenwirkungen zu prüfen. Die Behandlungsstrategie von PRI-002 liegt darin, dass die toxischen Oligomere durch den Wirkstoffkandidaten eliminiert werden. Die orale Verabreichung von PRI-002 führte bei Mäusen mit alzheimerähnlichen Symptomen zu einer kognitiven Leistungsverbesserung.
"Viele Forschungsgruppen sowie die pharmazeutische Industrie versuchen, die Produktion der Monomere zu reduzieren, um die Wahrscheinlichkeit der Oligomer-Bildung präventiv zu verringern", erklärt Dieter Willbold, Aufsichtsrat der Priavoid GmbH und Direktor am Institut für Strukturbiochemie. "Einige wenige andere Ansätze versuchen ebenfalls, die Oligomere ins Visier zu nehmen, und zwar mit Antikörpern, die zwar an Oligomere binden, diese aber dadurch nicht direkt zerstören, sondern auf Komponenten des Immunsystems hoffen müssen, die die Antikörper-markierten Oligomere möglicherweise abbauen. Unsere Therapie-Strategie ist jedoch völlig anders. Mit unserem speziell entwickelten Wirkstoffkandidaten zielen wir auf bereits ausgebildete Oligomere. Wir eliminieren sie direkt, ohne dass wir uns auf die Hilfe des Immunsystems verlassen müssen."
Dr. Ralph Zahn, Geschäftsführer der Priavoid GmbH meint dazu: "Die positiven Ergebnisse aller bisherigen Studien haben uns darin bestärkt, den nächsten Schritt in Richtung einer klinischen Studie zu unternehmen." Bis zur möglichen Zulassung eines Medikaments vergehen jedoch im Durchschnitt 7 Jahre vom Start einer Phase I bis zur Marktzulassung.
Meistgelesene News
Themen
Organisationen
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.
Meistgelesene News
Weitere News von unseren anderen Portalen
Zuletzt betrachtete Inhalte

Sevion Therapeutics - San Diego, USA

Wenn runzlige Falten gut sind: Schrumpelig aussehende Bakterien sind am besten an ihren Wirtsorganismus angepasst

Primm GmbH - Dübendorf, Schweiz

Eppendorf Austria GmbH - Wien, Österreich

Chemiker nutzen Treibhausgas zur Herstellung eines Wirkstoffs gegen Schlafkrankheit - Mit Flow-Chemie Fluoroform sinnvoll nutzen