Maßgeschneiderte Nanopartikel gegen Krebs gesucht
Forschungsteam erforscht Wirkung von Zinkperoxid auf Krebszellen
Elektronische Bauteile, Beschichtungen oder Arzneimittel – Nanopartikel, kleiner als das menschliche Haar, können ganz unterschiedliche Eigenschaften und damit vielseitige Anwendungsmöglichkeiten haben. Die jeweilige Funktion hängt vor allem von der Größe der Partikel ab. Eine interdisziplinäre Forschungsgruppe, darunter Mitglieder des Forschungsschwerpunktes Nanowissenschaften und Oberflächenforschung und des Exzellenzclusters Entzündungsforschung der Christian-Albrechts-Universität zu Kiel (CAU), hat eine Methode entwickelt, um Partikel aus Zinkperoxid maßgeschneidert herzustellen. So können sie gezielt Einfluss auf ihre Eigenschaften nehmen, wie zum Beispiel die Schädigung von Krebszellen. Erste Ergebnisse, die jetzt in der Fachzeitschrift Nature Communications erschienen sind, machen langfristig einen Einsatz in der Krebstherapie denkbar.
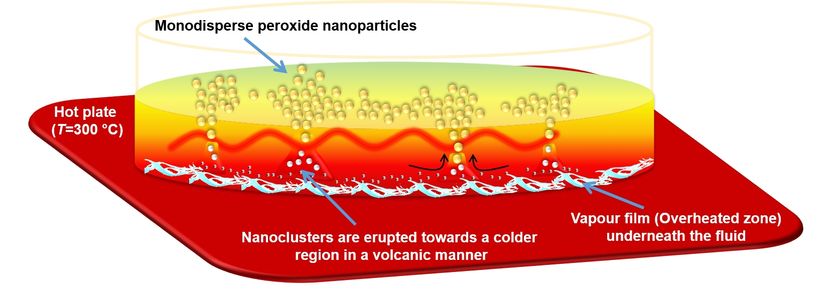
Die Nanopartikel werden in einem Wasserbad auf einer Heizplatte bei einer Temperatur von 300 Grad hergestellt. Hierbei wirken Mechanismen des sogenannten Leidenfrost-Effekts, die auch bei Unterwasservulkanen entstehen. In der wärmeren Region am Boden des Wasserbads (rot) bilden sich die Partikel. Anschließend steigen sie in die höhere, kältere Region (gelb) auf, wo sie wachsen und sich zu einheitlichen Gruppen zusammenschließen.
Copyright: Mady Elbahri
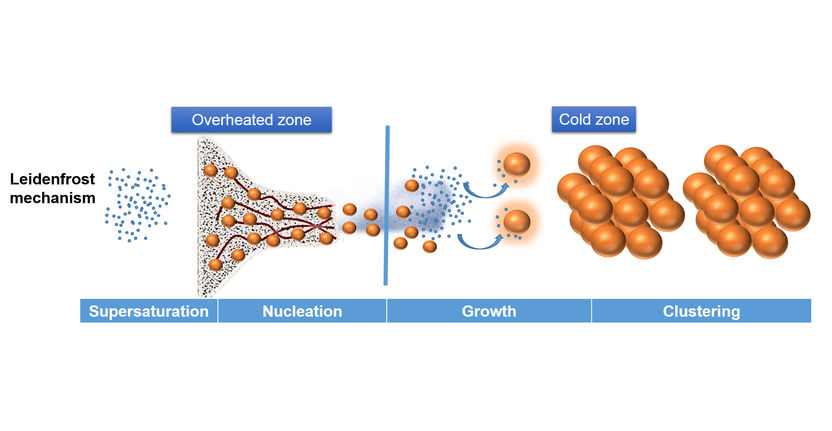
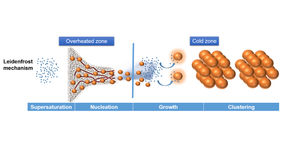
Erst die Trennung der beiden Phasen der Partikelentstehung und des Partikelwachstums in den verschiedenen Regionen des Wasserbades, ermöglicht es den Forschenden, die Größe der Partikel genau festzulegen.
Copyright: Mady Elbahri

Unter dem Transmissionselektronenmikroskop ist es zu erkennen: Bei den entstandenen Partikeln handelt es sich um Kugeln aus Zinkperoxid. Da alle gleich groß sind (hier: 680 Nanometer), haben sie alle dieselbe Wirkung: Sie schädigen Krebszellen und lassen langfristig einen therapeutischen Einsatz denkbar erscheinen.
Copyright: Mady Elbahri
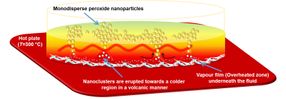

Für ihre neue Methode zur Herstellung von Nanopartikeln machen sich die Forschenden den sogenannten Leidenfrost-Effekt zu Nutze: Fällt ein Wassertropfen auf eine Oberfläche, die sehr viel heißer ist als der Siedepunkt des Wassers, beginnt er gewissermaßen zu schweben, bis er vollständig verdampft ist. Der Wassertropfen kann dabei als Mikro-Reaktor dienen, in dem sich kleine Nanopartikel bilden. Der Materialwissenschaftler und Chemiker Mady Elbahri beschäftigt sich seit Jahren mit der nach diesem Prinzip benannten „Leidenfrost-Chemie“. „Von meinen bisherigen Forschungen in der Materialwissenschaft wusste ich, dass die Größe von Partikeln entscheidend ist für ihre Fähigkeiten“, sagt Elbahri. „Diese Idee wollte ich übertragen auf die Herstellung von Zinkperoxid-Kugeln im Nanomaßstab.“ Als Mitglied des Sonderforschungsbereichs 677 „Function by Switching“ forscht Elbahri seit 2009 als Professor für Nanochemistry and Nanoengineering an der CAU und seit kurzem auch an der Aalto University in Helsinki.
Zinkperoxid gilt – noch mehr als einfaches Zinkoxid – als besonders effektiver Sauerstofflieferant. Das macht es zu einem interessanten Material für die Behandlung von Krankheiten wie zum Beispiel Krebs. Für Zinkoxid liegen bereits Untersuchungen vor, die zeigen, dass es den Anteil an reaktivem Sauerstoff in Zellen übermäßig erhöht und mit dieser „Sauerstoff-Übersättigung“ zu ihrem Tod führt. Um Zinkperoxid-Partikel in einer bestimmten Größe gezielt herstellen zu können, schauten sich die Forschenden genauer an, wie der Leidenfrost-Effekt speziell unter Wasser wirkt, etwa bei Vulkanaktivitäten in der Tiefsee. Diese Prinzipien übertrugen sie auf ihre Arbeit im Labor. Für die Herstellung der Partikel nutzten sie statt eines einzelnen Wassertropfens ein Wasserbad auf einer Herdplatte. Auf den Boden gaben sie eine Lösung aus Zinkazetat und Wasserstoffperoxid. Dort ist es besonders heiß und es herrscht eine hohe Konzentration an Ionen – ideale Bedingungen für die Bildung von Partikeln. Die entstandenen Partikel stiegen anschließend in den kühleren Bereich des Wasserbades auf, wo sie sich zu Gruppen zusammenschlossen und alle auf dieselbe Größe wuchsen. Erst die Trennung der zwei Phasen Partikelbildung und Partikelwachstum macht es möglich, gleichgroße Teilchen in großer Zahl kontrolliert herzustellen. Über die Zusammensetzung der Zinkazetatlösung variierten die Forschenden die Partikelgröße in sieben Stufen von 70 bis 680 Nanometer.
„Wir konnten in unseren Versuchen nachweisen, dass Nanopartikel aus Zinkperoxid Krebszellen schädigen und diese Wirkung – neben den Krebszellenarten und der Konzentration der Nanopartikel – tatsächlich vor allem von ihrer Größe abhängt“, fasst Elbahri zusammen. Ihre neue Methode zur Herstellung der Partikel habe außerdem den Vorteil, dass sie im Gegensatz zu konventionellen Verfahren ganz ohne chemische Zusätze auskomme, schließlich finde sie ausschließlich im Wasser statt, so Elbahri weiter. „Damit erfüllt sie eine wichtige Voraussetzung für den therapeutischen Einsatz.“
Um sicherzugehen, dass es sich bei den derart kleinen Partikeln wirklich um kugelförmiges Zinkperoxid handelt, wurden die Proben im Transmissionselektronenmikroskop an der Technischen Fakultät der CAU untersucht. Die bei dieser Methode eingesetzten Elektronen zersetzen das Material allerdings unter der Freigabe von Sauerstoff. Durch ultraschnelle Elektronenbeugung konnte dennoch nachgewiesen, dass es sich um Zinkperoxid handelt. Lorenz Kienle, Professor für Synthese und Realstruktur, erklärt einen interessanten Nebenaspekt der Untersuchung: „Durch die Freigabe des Sauerstoffs zerfallen die kugelförmigen Zinkperoxid-Partikel in kleinere Zinkoxid-Teilchen, die sich zu Hohlkugeln anordnen. Diese spontane Änderung ihrer Gestalt konnten wir erstmals in einzelnen Sequenzen beobachten. Frühere Erkenntnisse zum Bildungsmechanismus von Zinkoxid-Hohlkugeln konnten wir damit korrigieren.“
Im Labor von Dieter Adam, Professor im Kieler Sonderforschungsbereich 877 „Proteolysis as a Regulatory Event in Pathophysiology“ und Mitglied im Exzellenzcluster Entzündungsforschung, wurden die biologischen Untersuchungen durchgeführt. Adam ist Teil des Kiel Oncology Network der CAU, das unter anderem die Entwicklung von Tumoren erforscht. „Die ersten Versuche mit der neuen Synthetisierungsmethode haben gezeigt, dass es sich bei Zinkperoxid um ein sehr spannendes Material für potenzielle medizinische Anwendungen handelt. Das ist ein vielversprechender Anfang für weitere Studien, die zu einer Verbesserung von Krebstherapien beitragen könnten“, ordnet er die Ergebnisse ein. Nächste Untersuchungsschritte sind, die genauen Mechanismen hinter der Zellschädigung für verschiedene Tumorarten zu erforschen.