Die clevere Zelle
Forscher entschlüsseln molekularen Mechanismus, der das Schwarmverhalten von Bakterienpopulationen hemmt
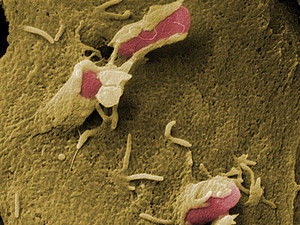
Bakterien sind in der Natur zumeist weniger Individualisten, sondern liegen als multizelluläre Kollektive vor. Sie können ihr Verhalten koordinieren, und manche Arten können sich wie ein Schwarm fortbewegen. In der Nachwuchsgruppe Biologische Chemie an der Universität Konstanz wird untersucht, wie Organismen dieses Bakterienverhalten manipulieren, vor allem aber hemmen können. Gruppenleiter Dr. Thomas Böttcher und sein Team mit der Doktorandin Sina Rütschlin haben die Biosynthese eines solchen Schwarminhibitors untersucht und kamen zum Ergebnis: Die Produktion des Schwarminhibitors hängt von spezifischen Substratverhältnissen in der Bakterienzelle ab. Dies hat darüber hinaus einen bedeutsamen evolutionären Aspekt: Die Arbeitsgruppe konnte damit zeigen, wie die Bakterienzellen mit wenig Aufwand verschiedenste Naturstoffe herstellen können. Die Ergebnisse könnten in Zukunft zur Überwindung von Infektionskrankheiten und zur Bekämpfung von Antibiotika-Resistenzen beitragen.
Durch das Schwarmverhalten werden Bakterien Antibiotika gegenüber erheblich toleranter. Es kann vorkommen, dass selbst eine zehn- bis hundertfach erhöhte Konzentration nichts gegen sie ausrichtet. In seiner Postdoc-Zeit in den USA konnte Thomas Böttcher zwei Bakterienstämme aus einer Rotalgenprobe isolieren: Vibrio alginolyticus, der rasch schwärmt, und Shewanella algae, der diese Fortbewegung hemmt und dabei den Expansionsdrang seines Konkurrenten einschränkt. Shewanella algae erzielt diese Wirkung über ein sogenanntes Siderophor, das der Stamm produziert und mit dem die Bakterienzellen Eisen aus der Natur aufnehmen können.
Die Frage lautete nun: Wie wird das Siderophor hergestellt? Bei der Sequenzierung des Bakteriums wurde ein Gen-Cluster gefunden, das als mögliche zelluläre Fabrik für das Siderophor infrage kam. „Unser Hauptbefund war, dass, anders als ursprünglich vermutet, das Enzym das entscheidende Siderophor nicht aufgrund seiner hohen Spezifität herstellt, sondern dass es hauptsächlich an den Substratverhältnissen in der Zelle liegt, welche Produkte hergestellt werden“, sagt der Chemiker, der Mitglied des Zukunftskollegs der Universität Konstanz ist. Dabei zeigte sich, dass das fragliche Enzym eigentlich eine Spezifität für einen völlig anderen Metaboliten (Stoffwechselprodukt) hätte. Die Zelle kann ihre Bausteine offenbar so regulieren, dass sie einen Metaboliten als Hauptprodukt herstellt, der vom Enzym selbst gar nicht bevorzugt würde, aber der Zelle einen wichtigen Vorteil verschafft.
„Die Bakterienzelle stellt die Substrate so ein, dass gleichzeitig drei Metaboliten als Produkte entstehen. Dies ermöglicht eine gewisse Variabilität und erlaubt eine Vielfalt von Metaboliten möglichst ökonomisch herzustellen“, erklärt Thomas Böttcher. Dies macht eine schnelle evolutionäre Anpassung möglich.
Dass sich nicht die Selektivität des Enzyms auf ein Hauptprodukt eingestellt hat, sondern die Produktion unterschiedlicher Metaboliten auf der Substratebene reguliert wird, hat Konsequenzen. Das bisherige Vorgehen, Gensequenzen aus Umweltproben in ein gut handhabbares Labor-Bakterium einzupflanzen, kann dazu führen, dass komplett artifizielle Produkte entstehen. Es ist entscheidend, den Substrat-Pool zu kennen, um beurteilen zu können, was am Ende herauskommt.
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft

Holen Sie sich die Life-Science-Branche in Ihren Posteingang
Mit dem Absenden des Formulars willigen Sie ein, dass Ihnen die LUMITOS AG den oder die oben ausgewählten Newsletter per E-Mail zusendet. Ihre Daten werden nicht an Dritte weitergegeben. Die Speicherung und Verarbeitung Ihrer Daten durch die LUMITOS AG erfolgt auf Basis unserer Datenschutzerklärung. LUMITOS darf Sie zum Zwecke der Werbung oder der Markt- und Meinungsforschung per E-Mail kontaktieren. Ihre Einwilligung können Sie jederzeit ohne Angabe von Gründen gegenüber der LUMITOS AG, Ernst-Augustin-Str. 2, 12489 Berlin oder per E-Mail unter widerruf@lumitos.com mit Wirkung für die Zukunft widerrufen. Zudem ist in jeder E-Mail ein Link zur Abbestellung des entsprechenden Newsletters enthalten.