Stammzell-Transplantation: Aktivierung von Signalwegen schützt vor gefährlicher Immunreaktion
Stammzelltransplantationen können Leben retten, etwa bei Leukämie. Ohne Risiken sind diese Behandlungen jedoch nicht. Eine mögliche Komplikation ist die Graft-versus-Host-Reaktion, bei der aus den Stammzellen Immunzellen entstehen, die den Körper angreifen. Ein Team der Technischen Universität München (TUM) hat molekulare Mechanismen identifiziert, die in Zukunft Erkrankte vor der gefährlichen Reaktion schützen könnten. Der Schlüssel, um die Graft-versus-Host-Reaktion zu verhindern, liegt im Darm.
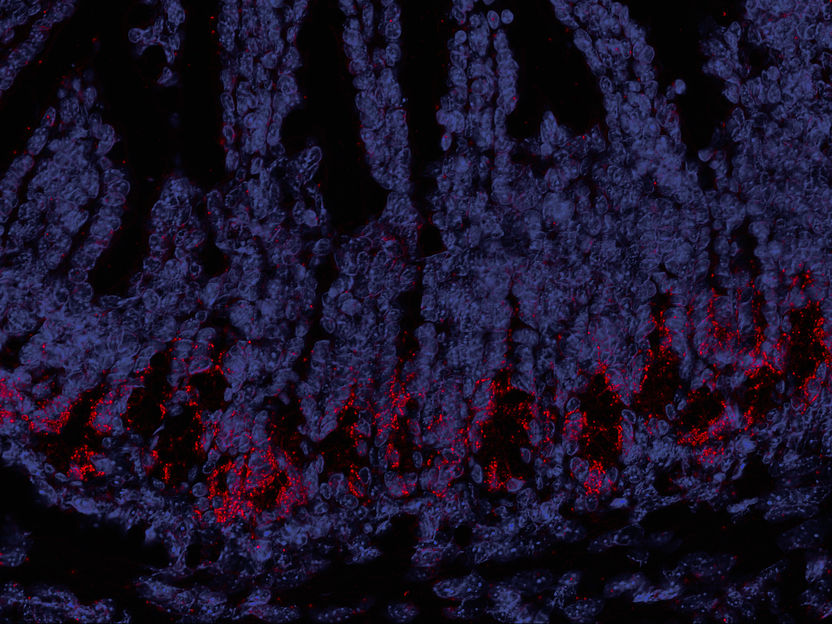
Schnittbild eines Mäusedarms: OLFM4-Stammzellen (rot) sind wichtig für die Regeneration des Epithels. Während der Behandlung im Vorfeld einer Stammzelltransplantation werden sie oft zerstört.
Poeck / TUM
Damit fremde Stammzellen sich im Körper vermehren und beispielsweise gesunde Blutkörperchen produzieren, muss zunächst einmal Platz für sie geschaffen werden. Zu diesem Zweck werden vorhandene Zellen im Knochenmark vor einer Transplantation mit Medikamenten oder Strahlung zerstört.
Eines der Risiken dabei ist die Graft-versus-Host-Reaktion (etwa: Transplantat-gegen-Empfänger-Reaktion). Sie tritt ungefähr bei der Hälfte der Behandlungen auf. Vereinfacht gesagt bilden sich dabei aus den transplantierten Stammzellen sogenannte T-Lymphozyten. Diese Abwehrzellen sollen eigentlich schädliche Eindringlinge wie Bakterien bekämpfen, kommen aber auf die falsche Spur und beginnen, den ohnehin schon geschwächten Körper der Patienten anzugreifen.
Ein internationales Team um Privatdozent Dr. Hendrik Poeck und Dr. Tobias Haas, Leiter einer Forschungsgruppe an Klinik und Poliklinik für Innere Medizin III, Hämatologie und Onkologie des Klinikums rechts der Isar der TUM, und Professor Marcel van den Brink am Memorial Sloan Kettering Cancer Center (MSKCC) in New York, schildert im Fachjournal „Science Translational Medicine“, wie man diesen Prozess verhindern könnte.
Auslöser im Darm
Von den Angriffen durch die T-Zellen sind meist Haut, Leber und insbesondere der Magen-Darm-Trakt betroffen. Im Darm nimmt die Graft-versus-Host-Reaktion auch ihren Anfang. Durch die Medikamente und die Bestrahlung wird die Schleimschicht im Darm, das Epithel, beschädigt. Stresssignale, die absterbende Epithelzellen aussenden, und Darmbakterien, die aufgrund des fehlenden Epithels an ehemals keimfreie Stellen des Darms gelangen, lösen gewissermaßen einen Großalarm und die Aktivierung von aggressiven Spender-T-Zellen aus. „Könnte man das Epithel schützen oder schnell wiederherstellen, würde das Risiko einer Abwehrreaktion deutlich sinken“, sagt Hendrik Poeck. „Bisher gibt es aber kaum Behandlungsstrategien, die auf eine Epithelregeneration abzielen.“
Die Wissenschaftler um Poeck haben mit RIG-I und STING zwei körpereigene Proteine untersucht, die vor allem für ihre Rolle bei der Abwehr von Bakterien oder Viren bekannt sind. „Wir konnten erstmals zeigen, dass beide auch für eine regenerative Wirkung genutzt werden können“, sagt Julius Fischer, Erstautor der Studie. Beide Proteine sind Teil von Signalketten, die dafür sorgen, dass Interferon-I (IFN-I) produziert wird. IFN-I startet eine Vielzahl an Immunreaktionen, kann aber darüber hinaus dafür sorgen, dass Epithelzellen schneller ersetzt werden.
Der richtige Zeitpunkt
Seit einiger Zeit ist bekannt, dass sich der RIG-I-Signalweg mithilfe des Stoffes Triphosphat-RNA (3pRNA) gezielt auslösen lässt. Poeck und sein Team konnten anhand von Mäusen zeigen, dass sich mithilfe von 3pRNA das Epithel tatsächlich schützen lässt. Dabei kam es auf den richtigen Zeitpunkt an: Nur wenn der Stoff genau einen Tag vor dem Beginn der Bestrahlung und Medikamentengabe verabreicht wurde, war eine Schutzfunktion messbar. „Wir vermuten, dass es schon am ersten Tag nach Beginn der Behandlung nicht mehr ausreichend intakte Epithelzellen im Darm gibt, in denen der RIG-I/IFN-Signalweg noch wirken könnte“, erläutert Tobias Haas. Obwohl nach einer Behandlung mit 3pRNA aus den gespendeten Stammzellen weniger aktivierte T-Zellen entstanden, wurde die positive Wirkung der Therapie gegen die Leukämie nicht messbar eingeschränkt.
„Sowohl RIG-I Agonisten wie 3pRNA als auch STING Agonisten befinden sich zurzeit in der klinischen Entwicklung“, sagt Hendrik Poeck. Für beide zeichne sich eine vielfältige Anwendung ab, insbesondere im Bereich der Tumortherapie. „Unsere Studie zeigt, dass auch regenerative Prozesse durch selektive Aktivierung dieser Signalwege eingeleitet werden könnten“, erläutert Poeck die Forschungsergebnisse seines Teams. Eine zukünftige Verabreichung dieser selektiven Agonisten an Patienten, die für eine allogene Stammzelltransplantation in Frage kommen, erscheint somit durchaus denkbar. Zuvor müssen jedoch noch weitere Studien zur genauen Wirkweise dieser Agonisten durchgeführt werden, um eine Applikation im Menschen zu ermöglichen“.