Mobile Goldfinger
Wanderwellen-Ionenmobilitäts-Massenspektrometrie klärt Goldfinger-Strukturen auf
Goldhaltige Medikamente werden schon Jahrhunderten verwendet, z.B. bei rheumatischer Arthritis. Zudem scheinen sie eine Wirksamkeit gegen Krebs und HIV zu zeigen. Einer der Wirkmechanismen könnte darauf basieren, dass Goldionen Zinkionen aus sogenannten Zinkfingern verdrängen, schleifenförmigen Nucleinsäure-bindenden Proteindomänen. Amerikanische Forscher haben solche „Goldfinger“ jetzt durch Massenspektrometrie charakterisiert. Wie sie in der Zeitschrift Angewandte Chemie berichten, gelang es ihnen, die genauen Bindestellen für das Gold zu identifizieren.
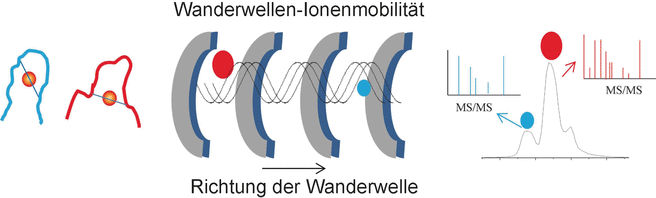
© Wiley-VCH
„Das Zinkion in Zinkfingern bindet an vier Schwefel- oder Stickstoffatome der Cystein- und Histidingruppen des Proteins“, erläutert Nicholas P. Farrell von der Virginia Commonwealth University (Richmond, USA). „Goldionen binden an zwei Aminosäurereste und verändern so die Konformation des Proteins. Die „Goldfinger“ sind nicht mehr in der Lage, Nucleinsäuren zu binden, was von therapeutischem Interesse sein kann.“
Obwohl verschiedene mögliche Bindestellen für Metallionen existieren, liegen Metalloproteine meist bevorzugt in einer Variante vor. Wo die spezifischen Bindestellen sind, ließ sich in einer Mischung verschiedener Konformere bisher nicht bestimmen. Farrell und sein Team nahmen sich jetzt zwei Goldfinger genau unter die Lupe. Farrell: „Bei Ersatz des Zinks im Zinkfinger Nr. 3 des allgemeinen Transkriptionsfaktors Sp1 entsteht nur eine Goldfinger-Variante. Sie enthält eine lineare Cys-Au-His-Bindung.“ Im Fall des Nucleocapsid-Proteins von HIV, das eine kritische Rolle bei der Replikation der Viren spielt, führt Einführen von Gold in Zinkfinger 2 des Proteins (NCp7-F2) zu drei verschiedenen Goldfinger-Spezies mit linearen Cys-Au-Cys-Motiven, von denen eine deutlich vorherrscht.
Der Erfolg der Forscher basiert auf einer speziellen Analyse-Technik, der Wanderwellen-Ionenmobilitäts-Massenspektrometrie (TWIM-MS). Vereinfacht gesagt werden dabei Analytmoleküle ionisiert und die Ionen durch ein elektrisches Feld in einem Gas beschleunigt. Durch Kollisionen mit den Gasmolekülen werden die Ionen immer wieder abgebremst – große, voluminöse Moleküle stärker als kleine oder kompaktere, da sie häufiger kollidieren. So lassen sich auch Isomere unterscheiden und trennen, die zwar gleiche Massen haben, aber unterschiedliche Geometrien und damit unterschiedliche Mobilitäten. Die nach Mobilität getrennten Ionen können dann durch Kollisionen fragmentiert (CID) und die Fragmente erneut massenspektrometrisch untersucht werden. So lassen sich kürzere, aber immer noch an Gold gebundene Peptide charakterisieren.
„Auf diese Weise ist es uns gelungen, die spezifischen Bindestellen und -modi der Gold-modifizierten Zinkfinger NCp7-F2 und Sp1-F3 zu identifizieren“, so Farrell. „Die Ionenmobilitäts-Massenspektrometrie liefert damit wichtige Informationen über die Formveränderungen, die durch einen Austausch des Zinks in Zinkfingerproteinen ausgelöst werden, sowie die Selektivität und Reaktivität einer solchen Reaktion. Davon könnte die Suche nach neuen Metall-basierten antiviralen und Antitumorwirkstoffen profitieren.“
Originalveröffentlichung
Weitere News aus dem Ressort Wissenschaft
Meistgelesene News
Weitere News von unseren anderen Portalen
Verwandte Inhalte finden Sie in den Themenwelten
Themenwelt Massenspektrometrie
Die Massenspektrometrie ermöglicht es uns, Moleküle aufzuspüren, zu identifizieren und ihre Struktur zu enthüllen. Ob in der Chemie, Biochemie oder Forensik – Massenspektrometrie eröffnet uns ungeahnte Einblicke in die Zusammensetzung unserer Welt. Tauchen Sie ein in die faszinierende Welt der Massenspektrometrie!
Themenwelt Massenspektrometrie
Die Massenspektrometrie ermöglicht es uns, Moleküle aufzuspüren, zu identifizieren und ihre Struktur zu enthüllen. Ob in der Chemie, Biochemie oder Forensik – Massenspektrometrie eröffnet uns ungeahnte Einblicke in die Zusammensetzung unserer Welt. Tauchen Sie ein in die faszinierende Welt der Massenspektrometrie!



















































