Im Kampf gegen Alzheimer kann das Down-Syndrom wichtige Hinweise enthalten
Auf den ersten Blick scheinen das Down-Syndrom (DS) und die Alzheimer-Krankheit (AD), zwei schwere Hirnanomalien, wenig gemeinsam zu haben. Das Down-Syndrom ist eine Erbkrankheit, deren Ursache schon lange bekannt ist - eine Verdreifachung des Chromosoms 21. Im Gegensatz dazu verfügt die überwiegende Mehrheit der Alzheimer-Fälle (über 95 Prozent) nicht über eine eindeutige genetische Quelle. Stattdessen wird die Krankheit, die in der Regel erst im späten Lebensalter klinisch auftritt, durch eine verwirrende Konstellation von Faktoren verursacht. Während diese seit über 100 Jahren im Mittelpunkt intensiver Studien stehen, sind nur wenige schlüssige Antworten ans Licht gekommen.
In neuen Forschungen untersuchen Antonella Caccamo und ihre Kollegen eine Reihe von kritischen Faktoren, die die beiden Krankheiten zu verbinden scheinen. Das aktuelle Projekt wird DS als Fenster zu den zugrunde liegenden Mechanismen nutzen, die zu einer Alzheimer-Pathologie führen können. Mit diesem komplementären Ansatz wird ihr 3,1 Millionen Dollar NIH-Zuschuss die Auswirkungen eines kritischen Proteinkomplexes namens mTOR untersuchen.
Im gesunden Gehirn ist mTOR an einer Reihe von wesentlichen physiologischen Prozessen beteiligt. mTOR ist ein Regulator der Proteinsynthese und -abbau. Es spielt eine entscheidende Rolle für das Zellwachstum, die Langlebigkeit und die Bildung des Zytoskeletts, das lebende Zellen mit ihrer Form und Struktur versorgt, und mTOR ist entscheidend für die Aufrechterhaltung des richtigen Energiegleichgewichts in vielen Geweben im ganzen Körper. mTOR ist auch an der synaptischen Plastizität, der neuronalen Erholung und der Erhaltung des Gedächtnisses beteiligt.
Caccamo ist Forscher im ASU-Banner Neurodegenerative Disease Research Center. Ein Großteil ihrer Forschung konzentriert sich auf die Untersuchung von molekularen Veränderungen im Gehirn des Down-Syndroms, um ein neues Licht auf die Alzheimer-Krankheit zu werfen.
"Das ultimative Ziel meiner Forschung ist es, neue und klinisch übersetzbare Ziele zu identifizieren und so die Entwicklung neuer Therapien für AD zu unterstützen", sagt Caccamo.
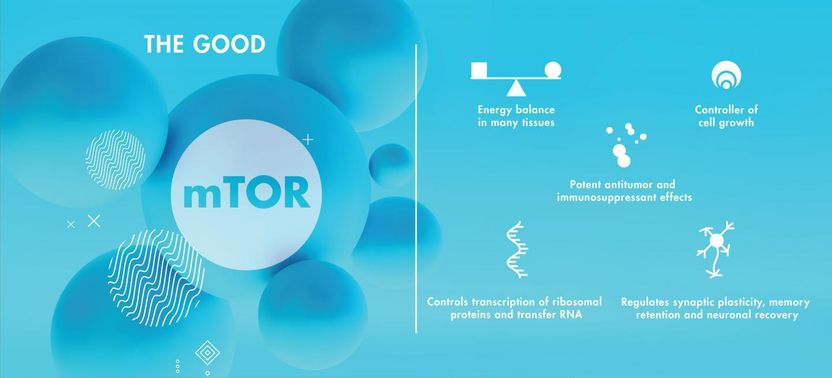
mTOR ist ein Proteinkomplex, der viele wichtige Funktionen im Körper erfüllt.
Shireen Dooling
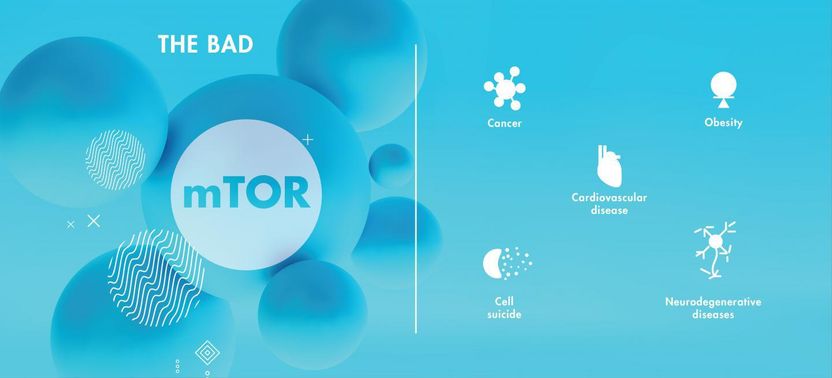
Die Hyperaktivität von mTOR wurde mit einer Reihe von Nebenwirkungen in Verbindung gebracht und ist an der Neurodegeneration beteiligt, die sowohl mit dem Down-Syndrom als auch mit Alzheimer verbunden ist.
Graphic by Shireen Dooling


Von mTOR lernen
Eine Störung des MTOR-Signalwegs wurde bei Krankheiten wie Krebs, Fettleibigkeit und Herz-Kreislauf-Erkrankungen festgestellt. Die Dysregulation von mTOR spielt auch eine wichtige Rolle bei Diabetes und Alterung, zwei bekannten Risikofaktoren für die Alzheimer-Krankheit. Unregelmäßigkeiten in der mTOR-Funktion stehen im Zusammenhang mit anderen neurodegenerativen Erkrankungen und führen nachweislich zu zwei unterschiedlichen Neuropathologien: Ablagerungen im Gehirn von Ablagerungen von Plaques, die aus dem Protein Amyloid beta (Aβ) bestehen, und Anhäufungen eines anderen Proteins - bekannt als Tau -, das sich in neuronalen Zellkörpern aggregiert und neurofibrilläre Verflechtungen bildet.
Plaques und Verflechtungen sind die klassischen Markenzeichen der Alzheimer-Krankheit. Interessanterweise kommen sie auch im Gehirn praktisch aller Patienten mit Down-Syndrom vor, von denen etwa 60 Prozent bis zum Alter von 60 Jahren die Alzheimer-Krankheit entwickeln. Interessanterweise befindet sich APP (Amyloid-Vorläuferprotein), ein Protein, das bei der Spaltung Beta-Amyloid erzeugt (Aβ), das giftige Protein, das sich im AD- und DS-Gehirn ansammelt, auf Chromosom 21, dem gleichen Chromosom, das beim Down-Syndrom verdreifacht wird.
Könnte eine Störung des lebenswichtigen MTOR-Signalwegs Hinweise auf die Entstehung von Plaques und Verflechtungen und den Beginn einer Demenz bei DS- und AD-Patienten liefern? Ist die mTOR-Dysregulation auch mit einer bestimmten Form des Zelltods verbunden, der sogenannten Nekroptose, die ebenfalls in der AD- und DS-Pathologie verwickelt ist? Vor allem aber kann die Untersuchung der molekularen Treiber der AD-Pathologie bei DS-Patienten ein neues Fenster in die frühen Mechanismen öffnen, die der Entwicklung der sporadischen Alzheimer-Krankheit zugrunde liegen, der Form der Krankheit, die häufig bei alternden Erwachsenen auftritt? Dies sind einige der wichtigen Fragen, die die neue Studie von Caccamo behandeln soll.
Unerbittliche Geißel
Die Alzheimer-Krankheit ist nach wie vor die einzige führende Todesursache, der es an Mitteln zur Behandlung, Prävention oder Heilung mangelt. Die Krankheit ist unerbittlich in ihrer systematischen Zerstörung der Gehirnfunktion, in der Zerstörung von Erinnerungen, in der Reinigung von Erinnerungen und in der Entziehung des Gehirns, was letztendlich zum Tod führt - typischerweise innerhalb von 8-10 Jahren nach der klinischen Diagnose, obwohl sich Alzheimer in einigen Fällen bis zu 20 Jahre hinziehen kann. Die emotionale Belastung von Patienten, Pflegepersonal und Gesellschaft ist immens und nimmt rapide zu.
Darüber hinaus liegt die erschütternde wirtschaftliche Belastung derzeit allein in den USA bei Hunderten von Milliarden Dollar und wird bis 2050 auf über eine Billion Dollar geschätzt. Der Bedarf an tragfähigen Behandlungen und Präventionsstrategien könnte nicht akuter sein.
Heute wissen die Forscher, dass der Beginn der Alzheimer-Krankheit Jahrzehnte vor dem Auftreten ihrer verräterischen Anzeichen beginnt. Einige sind sogar so weit gegangen zu sagen, dass AD in der Regel als eine Krankheit des hohen Alters angesehen wird, aber es kann auch mit der Pubertät in Verbindung gebracht werden, wenn die ersten Wegweiser der Krankheit in das scheinbar gesunde Gehirn gepflanzt werden. Viele in diesem Bereich glauben, dass die beste Hoffnung, die ominöse Trajektorie der Krankheit zu stoppen, darin besteht, kausale Mechanismen im frühesten Stadium zu identifizieren und wirksame Interventionsmöglichkeiten zu entwickeln, bevor das Gehirn irreparabel beschädigt wird.
Caccamo ist der Ansicht, dass die mTOR-Dysregulation ein solcher früher Mechanismus sein könnte, der zu einer AD-Pathologie bei alternden Erwachsenen und DS-Patienten führt. Die Forschung hat gezeigt, dass mTOR in bestimmten Hirnregionen sowohl bei AD- als auch bei DS-Patienten hyperaktiv ist. mTOR-Hyperaktivität ist weiterhin mit Tau-Pathologie und niedrigen Werten von TSC2 verbunden, einem kritischen Genprodukt, von dem angenommen wird, dass es die mTOR-Hyperaktivität in Schach hält. Schließlich deuten vorläufige Daten aus Caccamos Forschung darauf hin, dass der Zellverlust bei DS-Patienten zum Teil auf Nekroptose zurückzuführen ist, eine einzigartige Form des Zellselbstmords im Zusammenhang mit der Dysregulation von mTOR.
Diese Kombination von Faktoren hat zu der zentralen Hypothese der neuen Studie geführt: Die Funktionsstörung des TSC2-Komplexes führt zu einer Erhöhung der mTOR-Aktivität in DS, was zu einer AD-ähnlichen Neurodegeneration durch Induktion von Nekroptose führt.
Flüsse und Seitenarme der Alzheimer-Pathologie
Das neue Projekt von Caccamo mit dem Titel "Identify common mechanisms of neurodegeneration between Alzheimer's disease and Down syndrome" befasst sich mit diesen Fragen an mehreren Fronten. Das erste Ziel des Projekts ist es, die molekularen Mechanismen zu identifizieren, die der mTOR-Hyperaktivität bei DS zugrunde liegen. Hier wird die Verbindung von dysfunktionalem TSC2 mit mTOR-Hyperaktivität untersucht. Was könnte die Downregulation von TSC2 verursachen, die zu einer mTOR-Hyperaktivität führt? Drei Möglichkeiten werden experimentell untersucht: das Vorhandensein epigenetischer Veränderungen in TSC2 und mTOR, die Veränderung der Fluktuationsrate des TSC2-Proteins und neu entdeckter Proteine, die ebenfalls zur Destabilisierung der empfindlichen TSC2/mTOR-Achse beitragen können.
Das zweite Ziel der Studie ist es, die Rolle des hyperaktiven mTOR bei der Entwicklung von AD-ähnlichen Phänomenen in DS zu bestimmen. Hier wird die Hypothese eines hyperaktiven mTOR, der zu AD-Pathologien führt, insbesondere Aβ Plaques und neurofibrilläre Verflechtungen, mit Ts65Dn-Mäusen untersucht, einem genetischen Modell des Down-Syndroms. Die vorläufigen Ergebnisse von Caccamo zeigen, dass die mTOR-Hyperaktivität einem Anstieg der Aβ- und Tau-Werte sowie einer Degeneration von cholinergen Neuronen bei Mäusen vorausgeht. Durch subtiles Erhöhen oder Verringern der mTOR-Signalisierung wird die Studie die Auswirkungen der Reduktion von mTOR auf Aβ und Tau-Werte sowie die Degeneration von Neuronen in den Mäusen testen. Weiterhin werden erhöhte mTOR-Werte untersucht, um festzustellen, ob solche Veränderungen die AD-ähnliche Pathologie und kognitive Defizite erhöhen. Schließlich wird die Studie zusätzliche Proteine identifizieren, die unter die Regulierung von hyperaktivem mTOR in DS fallen.
Obwohl der Tod von Nervenzellen sowohl im Alzheimer- als auch im DS-Gehirn eine gut erkennbare Erscheinung ist, die mit einer Beeinträchtigung der kognitiven Leistungsfähigkeit verbunden ist, sind die Mechanismen, die zum Zelltod führen, noch nicht gut verstanden. Das dritte Ziel der neuen Studie ist die Untersuchung, wie die mTOR-Hyperaktivität zum neuronalen Verlust beiträgt. Frühere Arbeiten von Caccamo und anderen deuten darauf hin, dass eine Form des programmierten Zelltods, die als Nekroptose bekannt ist, zu der Neurodegeneration beiträgt, die typischerweise bei AD-Hirnen beobachtet wird.
In der dritten Phase der neuen Studie wird die Hypothese untersucht, dass hyperaktives mTOR dazu beiträgt, diesen Neurodegenerationsprozess durch die Aktivierung von Nekroptosepfaden im Gehirn in Gang zu setzen. Zur Überprüfung dieser Hypothese werden systematisch modulierende mTOR-Aktivität und Nekroptosesignalisierung in Mausneuronen verwendet. Neben einem besseren Verständnis der Mechanismen, die zum Zelltod bei DS und AD führen, wird die Forschung dazu beitragen, mögliche therapeutische Ziele für diese beiden tragischen Leiden aufzuklären.
Aus solchen Tiefenstudien, die sich mit dem tiefgreifenden Einfluss von mTOR auf das Gehirn, die Krankheit und die Gesundheit befassen, können die Forscher viel lernen. Zusätzlich zu seiner Relevanz für neurodegenerative Erkrankungen kann die entscheidende Rolle von mTOR im Alterungsprozess neue Erkenntnisse über andere grundlegende Fragen der Neurowissenschaften liefern.