Krebsmedikamente lernen, sich zu verstecken
Europäischer Forschungsrat fördert Wilfried Weber mit einem ERC Proof of Concept Grant
Wirkstoffe für die Krebstherapie verbessern: Für das Projekt „Hide and Seek with Cancer Drugs“ erhält der Freiburger Professor für Synthetische Biologie Wilfried Weber eine Förderung von etwa 150.000 Euro. Die finanziellen Mittel stellt der Europäische Forschungsrat (ERC) im Rahmen eines Proof of Concept Grants bereit. Dieser wird an Wissenschaftler vergeben, deren Forschungsvorhaben der ERC bereits gefördert hat und die das Innovationspotenzial einer Idee nutzen sowie ihre Entdeckung in Richtung Marktreife entwickeln wollen. Ziel von Webers Projekt ist es, die Verträglichkeit und Effizienz von Zytostatika, die bei Chemotherapien zur Behandlung von Krebs Anwendung finden, zu verbessern. Die Laufzeit der Förderung beträgt 18 Monate.
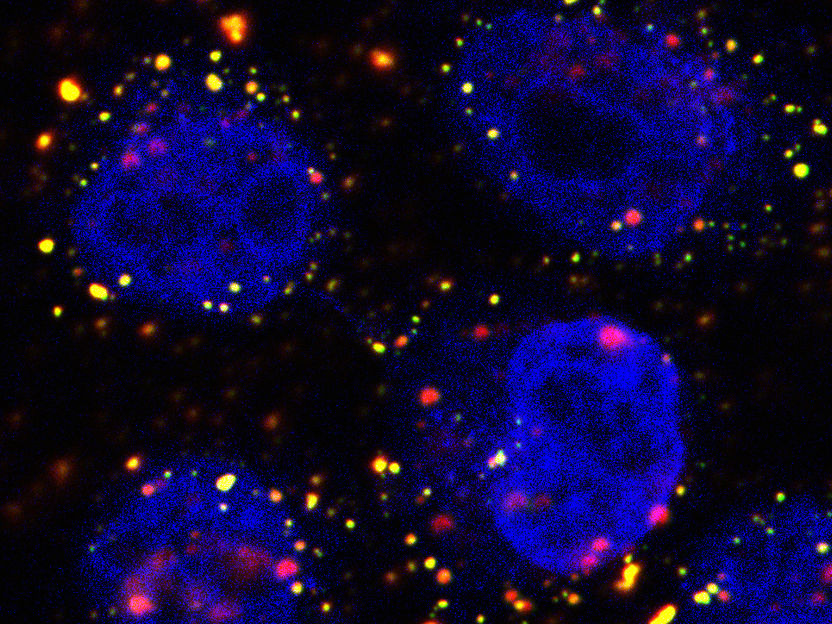
HeLa-Zellen (Zellkerne blau markiert), eine bestimmte Art von Krebszellen, mit Liposomen (grün, gelb und rot), die einen Wirkstoff einschließen sollen. Die Zellen haben einige der Liposomen aufgenommen.
Balder Rebmann

Prof. Dr. Wilfried Weber.
Thomas Kunz/BIOSS

Zytostatika töten Zellen ab, die schnell wachsen und sich teilen. Dazu gehören bösartig entartete Krebszellen, aber etwa auch Zellen des Magen-Darm-Trakts oder der Haarwurzeln. Dies ruft einige der schweren Nebenwirkungen hervor, die Zytostatikatherapien mit sich bringen. Die Wissenschaftler wollen die Effekte von Zytostatika auf gesunde Zellen verringern, indem sie die Substanzen vor der Anwendung an Patienten in kleine Nanobehälter, so genannte Liposomen, einschließen. An die Oberfläche der Nanobehälter binden sperrige Moleküle, die verhindern, dass Liposomen mit Zellen interagieren und diese den Wirkstoff aufnehmen können. „Die Nanobehälter erhalten somit eine Art Tarnkappe, die dafür sorgt, dass sich die Wirkstoffe im Körper verstecken können“, sagt Weber. „Erst wenn die Patienten eine weitere, harmlose Substanz einnehmen, verlieren die Zytostatika ihre Tarnkappe: Die Oberfläche der Liposomen wird freigegeben und die Tumorzellen können die Zytostatika finden und aufnehmen.“
Eine solche Freisetzung soll jedoch erst dann erfolgen, wenn sich die Liposomen samt Zytostatika dort angereichert haben, wo ihre zerstörerische Wirkung tatsächlich erwünscht ist: im Tumorherd. Dabei hilft ein Makel von Tumoren. Auch Krebszellen sind auf eine Blutversorgung angewiesen, um ihren Sauerstoff- und Nährstoffbedarf zu decken. Deshalb setzen sie Stoffe frei, die es begünstigen, dass sich neue Blutgefäße bilden. Die Blutgefäße innerhalb von Tumoren sind häufig jedoch von minderer Qualität und undicht, sodass kleine Partikel aus der Blutbahn ins umliegende Gewebe übertreten. In Kombination mit einem schlechteren Flüssigkeitsabfluss aus bösartig entartetem Gewebe ergibt sich, dass sich der im Blut transportierte Wirkstoff direkt am Zielort anreichert. Die Förderung ermöglicht den Forschenden unter anderem, die Anwendbarkeit ihrer Methode hinsichtlich des weit verbreiteten Zytostatikums Doxorubicin im Tiermodell zu testen, nachdem Experimente in Zellkulturen viel versprechende Ergebnisse erzielt haben.
Wilfried Weber ist Professor für Synthetische Biologie an der Fakultät für Biologie der Albert-Ludwigs-Universität und Principal Investigator des Freiburger Exzellenzclusters BIOSS Centre for Biological Signalling Studies. An dem Projekt beteiligt sind zudem Balder Rebmann, Doktorand in Webers Arbeitsgruppe, sowie Dr. Gerhard Pütz vom Institut für Klinische Chemie und Laboratoriumsmedizin des Universitätsklinikums Freiburg. Das EU-Büro der Freiburg Research Services und die Zentralstelle für Technologietransfer der Albert-Ludwigs-Universität haben den Antrag begleitet. Das Vorhaben basiert auf Ergebnissen des Forschungsprojekts „CompBioMat – Computing Biomaterials“, für das Weber mit einem ERC Starting Grant gefördert wurde.